Clear Sky Science · zh
通过刚性 AI 设计支架的 Trimbody 实现小蛋白的原子分辨率冷冻电镜结构测定
观察最小的构件
蛋白质是维持细胞生命的微型机器,但许多蛋白质体积过小,难以用当今最强大的成像工具清晰观测。本文介绍了“Trimbody”,一种巧妙的基于蛋白的辅助系统,使这些微小靶标在冷冻电子显微镜下显得更大且更刚性,从而让科学家能够以近原子分辨率观察它们。该方法有望加速基础生物学研究和基于纳米抗体的药物开发,尤其适用于那些此前因尺寸过小或过于柔性的药物靶点而难以成像的情况。
为何小蛋白难以被观测
冷冻电子显微学(cryo-EM)通过让研究者在近天然冷冻状态下观察大型生物分子,革新了结构生物学。然而,当蛋白质小于约50–100千道尔顿(蛋白常用的质量单位)时,它们在图像中会被噪声淹没,轮廓模糊,缺乏计算程序组装清晰三维模型所需的显著特征。已有策略试图通过将小蛋白连接到更大的伙伴来“增重”,但许多此类体系构建复杂、略显松散,或仅适用于有限的一类靶点。科学家需要一种简单、稳健的方法,使小蛋白在冷冻电镜下显得更大、更明亮且坚固可靠。
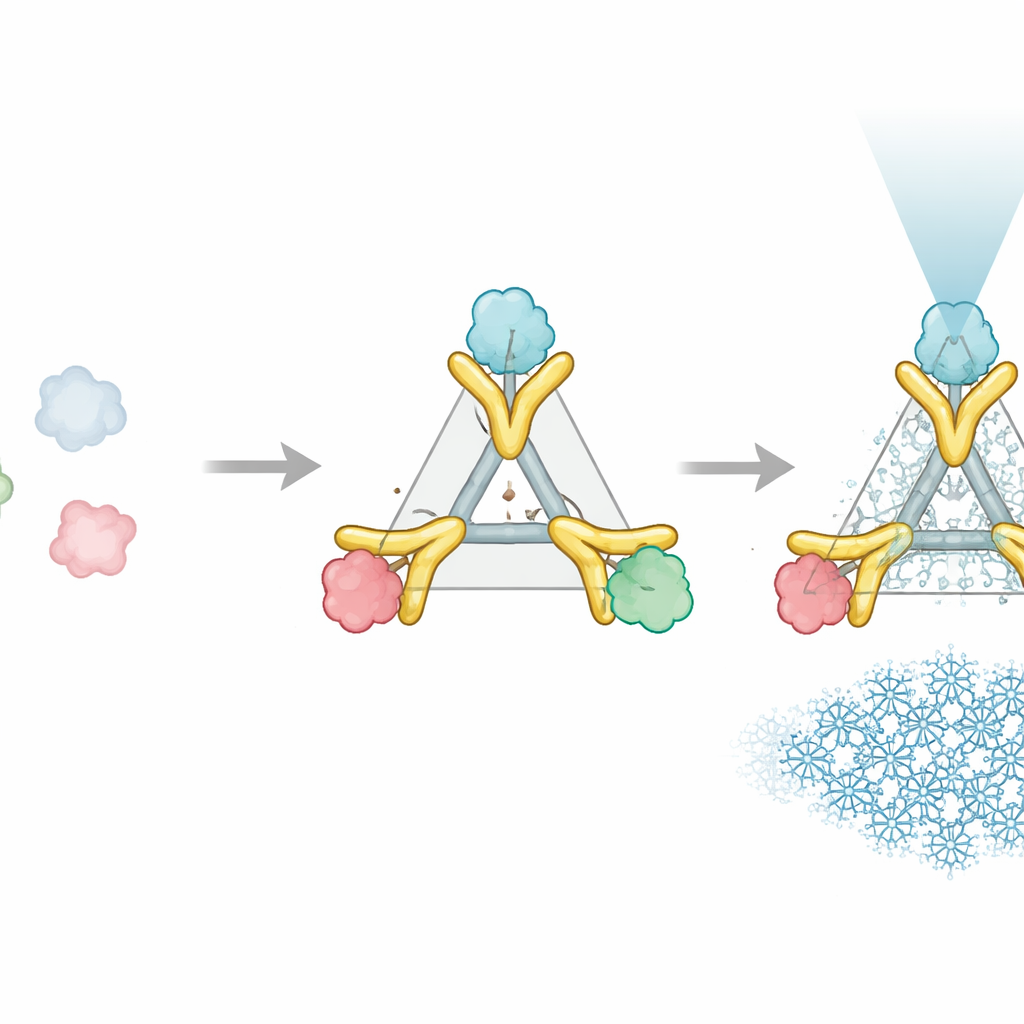
如刚性把手般由两部分构成的辅助体
Trimbody 系统仅用两部分工程化组件就解决了这一问题,它们围绕感兴趣的蛋白互相咬合。第一部分是三聚体支架——一个形成稳定刚性核心的三臂蛋白组装体。第二部分是定制的纳米抗体,一种能紧密结合选定靶标的小型抗体片段。该纳米抗体通过特制的“TAIL”结构域延长以抓握支架,而由 AI 设计的“H3”螺旋束则从内部稳定支架本身。上述改造如同支撑架和横梁,将纳米抗体与支架锁定为一个刚性整体。当三个纳米抗体—靶标对分别附着在支架的三臂上时,这个原本很小的蛋白便表现为显著更大、具有对称性且显微镜易于识别的结构。
将 Trimbody 付诸测试
为验证 Trimbody 的实际效果,作者将其应用于几种截然不同的小蛋白。他们成像了与人类免疫相关的蛋白(Galectin-10)、常用作实验室标记的绿色荧光蛋白、与癌症相关分子 Nectin-4 的前端结构域,以及将乳糖跨膜运输的细菌膜转运体。在每一种情况下,Trimbody 复合体在冷冻电镜栅格上形成了干净、行为良好的颗粒,并产生了约 2.3–2.6 埃的高分辨三维重构——足以分辨大多数氨基酸侧链。对仅含纳米抗体—靶标区域的聚焦计算细化提供了更清晰的视图,揭示了如柔性环、埋藏的化学基团和先前难以捕捉的结合表面等细微特征。重要的是,对于已有晶体结构的蛋白,基于 Trimbody 的冷冻电镜模型与之高度一致,表明该辅助支架并未扭曲靶标的天然形状。
设计性刚性与广泛兼容性
Trimbody 的一大优势在于其刚性是经过周密设计的。H3 结构域形成了三向的螺旋支撑,将伸出的结合模块锁定在三聚体底座上,同时 TAIL 结构域及其四螺旋连接子在纳米抗体与支架之间形成第二个锚点。结合强度测量表明,这种双重锚定使纳米抗体—支架的结合增强了约四个数量级,大大减少了会模糊冷冻电镜图像的不必要运动。作者还分析了大量既有的纳米抗体—蛋白结构,评估 Trimbody 可能产生立体冲突(即支架与蛋白本体碰撞)的频率。调查结果表明,对于大多数纳米抗体与靶标,通过调整少数框架残基并用标准生化方法检测复合体形成即可实现兼容性。
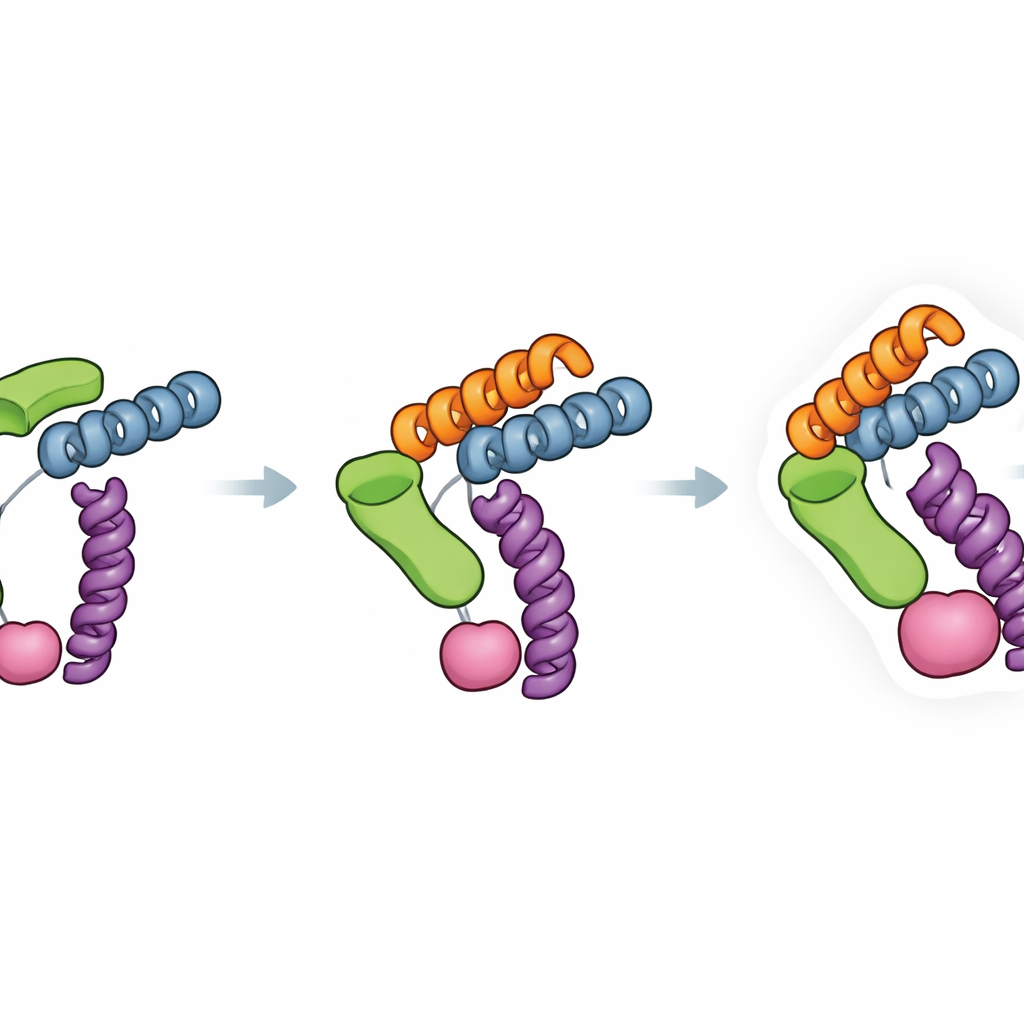
为微小靶标打开更清晰的窗口
通俗地说,Trimbody 像一个精密制作的把手,让显微镜能够“抓住”并对齐非常小的蛋白而不致抖动。由于它仅依赖两种可在细菌中方便生产的融合蛋白,该方法既具成本效益又便于许多实验室采用。通过将多种纳米抗体—靶标对转变为刚性、适宜冷冻电镜的复合体,Trimbody 提供了一条通用途径,可以对此前过小或难以研究的蛋白获取原子级别的视野。这一能力可加速对疾病相关蛋白的理解,并促进基于结构的快速纳米抗体药物与诊断工具开发。
引用: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
关键词: 冷冻电子显微镜, 纳米抗体支架, 蛋白质结构, AI 设计蛋白质, 小型膜蛋白