Clear Sky Science · de
Trimbody mit starren, von KI entworfenen Gerüsten ermöglicht kryo-EM-Strukturbestimmung von kleinen Proteinen in atomarer Auflösung
Die kleinsten Bausteine sichtbar machen
Proteine sind die winzigen Maschinen, die unsere Zellen am Leben erhalten, doch viele von ihnen sind zu klein, um mit den leistungsfähigsten Bildgebungswerkzeugen heute klar dargestellt zu werden. Diese Arbeit stellt „Trimbody“ vor, einen cleveren proteinbasierten Helfer, der diese winzigen Ziele unter dem Kryo-Elektronenmikroskop größer und steifer erscheinen lässt und so Forschern ermöglicht, sie in nahezu atomarer Detailauflösung zu sehen. Die Methode verspricht, die Grundlagenforschung und die Entwicklung nanobody-basierter Arzneimittel zu beschleunigen, insbesondere für Wirkziele, die zuvor zu klein oder zu flexibel waren, um sie gut zu vermessen.
Warum kleine Proteine schwer zu sehen sind
Die Kryo-Elektronenmikroskopie (kryo-EM) hat die Strukturbiologie revolutioniert, weil sie es erlaubt, große Biomoleküle in einem annähernd nativen, eingefrorenen Zustand darzustellen. Wenn Proteine jedoch kleiner als etwa 50–100 Kilodalton werden (eine gängige Größeneinheit für Proteine), verschwinden sie im Bildrauschen. Ihre Konturen sind schwach ausgeprägt, und ihnen fehlen markante Merkmale, die Computerprogramme zum Aufbau scharfer dreidimensionaler Modelle benötigen. Bestehende Strategien versuchen, diese kleinen Proteine „aufzubohren“, indem sie sie an größere Partner anhängen, doch viele dieser Systeme sind kompliziert herzustellen, etwas schlaff oder nur für einen engen Zielkreis geeignet. Es wurde eine einfache, robuste Methode benötigt, um kleine Proteine für die kryo-EM groß, hell und stabil erscheinen zu lassen.
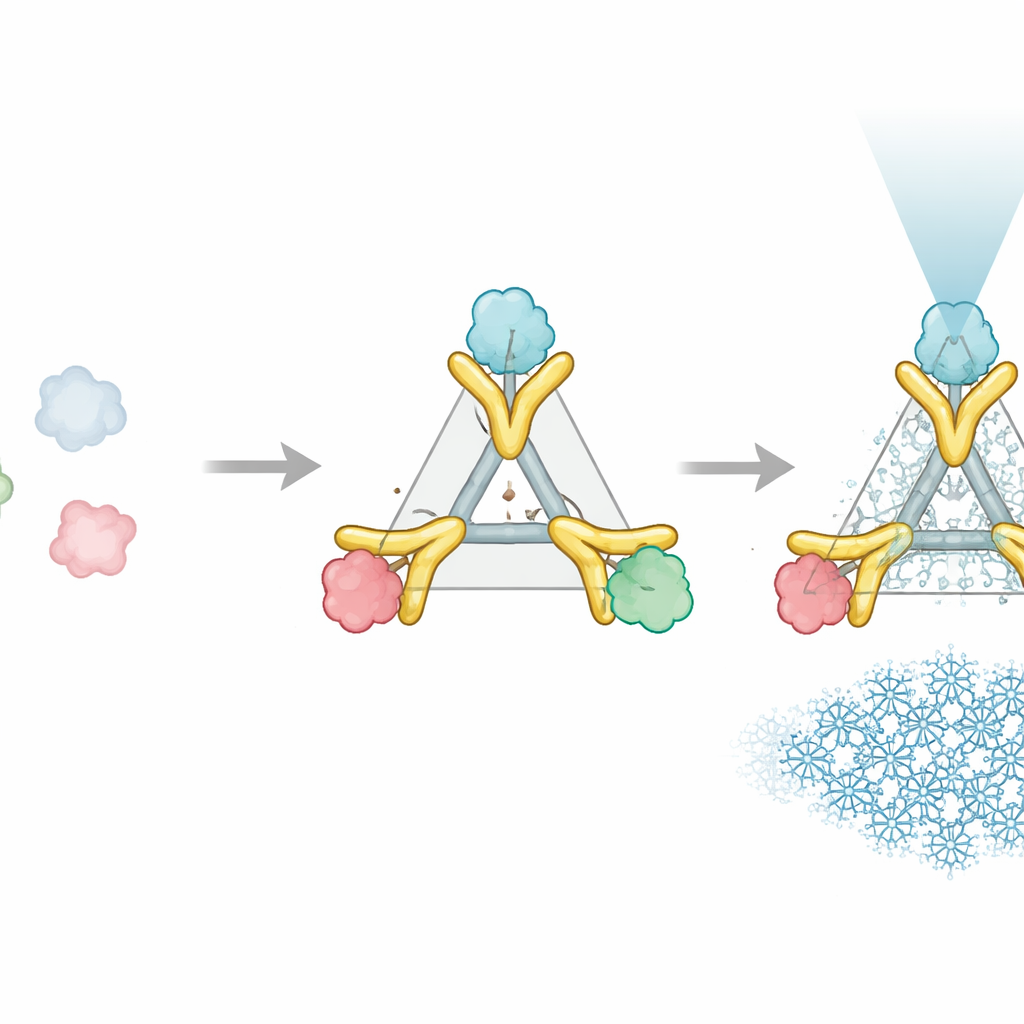
Ein zweiteiliger Helfer, der wie ein starrer Griff wirkt
Das Trimbody-System löst dieses Problem mit nur zwei konstruierten Komponenten, die sich um das Zielprotein legen. Der erste Teil ist ein trimeres Gerüst—eine dreiarmsige Proteinassemblierung, die einen stabilen, starren Kern bildet. Der zweite Teil ist ein maßgeschneiderter Nanobody, ein winziges Antikörperfragment, das fest an das gewählte Zielprotein bindet. Dieser Nanobody wird durch eine speziell entworfene „TAIL“-Domäne verlängert, die das Gerüst greift, während ein von KI entworfener „H3“-Helixbündel das Gerüst von innen stabilisiert. Zusammengenommen wirken diese Ergänzungen wie Verstrebungen und Querstreben, die den Nanobody und das Gerüst zu einer einzigen starren Einheit verriegeln. Wenn drei Nanobody–Ziel-Paare an die drei Arme des Gerüsts binden, verhält sich das zuvor winzige Protein wie ein Teil eines großen, symmetrischen und leicht erkennbaren Objekts im Mikroskop.
Trimbody auf die Probe gestellt
Um zu prüfen, ob Trimbody in der Praxis funktioniert, wendeten die Autorinnen und Autoren es auf mehrere sehr unterschiedliche kleine Proteine an. Sie bildeten ein humanes immunrelevantes Protein (Galectin-10), ein häufig im Labor verwendetes grünes Fluoreszenzprotein, die N-Terminal-Domäne des krebsassoziierten Moleküls Nectin-4 und einen bakteriellen Membrantransporter, der Laktose über Zellmembranen transportiert. In jedem Fall bildete der Trimbody-Komplex saubere, gutartige Partikel auf kryo-EM-Rastern und lieferte hochaufgelöste dreidimensionale Rekonstruktionen mit Auflösungen von etwa 2,3–2,6 Å—fein genug, um die meisten einzelnen Seitenketten von Aminosäuren zu unterscheiden. Eine fokussierte rechnerische Verfeinerung nur des Nanobody–Ziel-Bereichs ergab noch klarere Ansichten und zeigte subtile Merkmale wie flexible Schleifen, vergrabene chemische Gruppen und Bindungsflächen, die zuvor schwer einzufangen waren. Wichtig ist, dass sich Trimbody-basierte kryo-EM-Modelle bei Proteinen mit vorhandenen Kristallstrukturen eng mit diesen deckten, was zeigt, dass das Helfergerüst die natürliche Form des Ziels nicht verzerrt.
Gezielte Steifigkeit und breite Kompatibilität
Eine wesentliche Stärke von Trimbody liegt in der gezielten Entwicklung seiner Steifigkeit. Die H3-Domäne bildet eine dreifache helikale Verstrebung, die das herausragende Bindemodul mit der trimeren Basis verriegelt, während die TAIL-Domäne und ihr vierhelixiger Linker eine zweite Verankerung zwischen Nanobody und Gerüst schaffen. Messungen der Bindungsstärke zeigten, dass diese doppelte Verankerung die Nanobody–Gerüst-Verbindung um etwa vier Größenordnungen verbesserte und unerwünschte Bewegungen, die kryo-EM-Bilder verwischen können, stark reduzierte. Die Autorinnen und Autoren analysierten zudem viele vorhandene Nanobody–Protein-Strukturen, um zu prüfen, wie oft Trimbody auf sterische Konflikte stoßen würde—Situationen, in denen das Gerüst mit dem Protein selbst kollidiert. Ihre Untersuchung legt nahe, dass sich das System für die meisten Nanobodies und Ziele durch Anpassung einer kleinen Reihe von Framework-Residuen und Standard-Biochemie-Tests zur Komplexbildung kompatibel machen lässt.
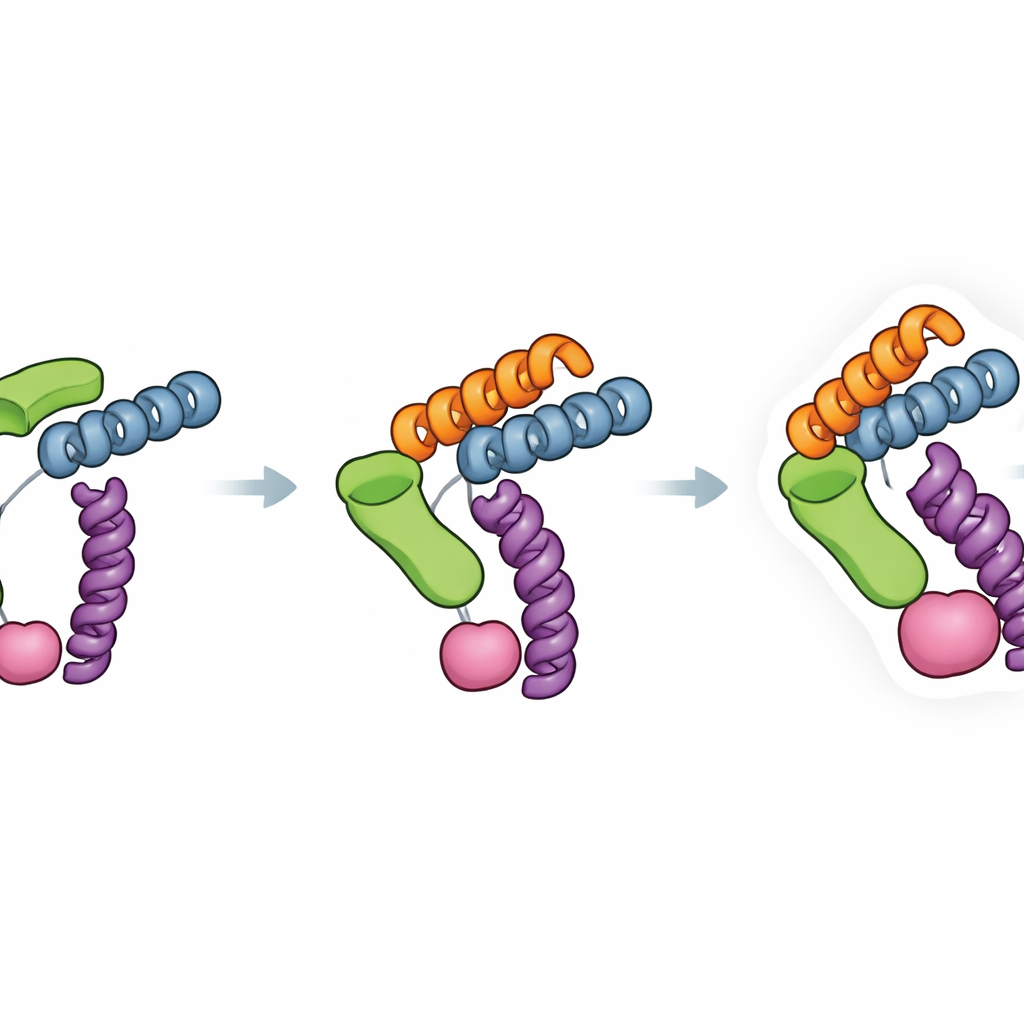
Ein klareres Fenster auf winzige Ziele
Alltäglich gesprochen wirkt Trimbody wie ein präzise gefertigter Griff, mit dem Mikroskope sehr kleine Proteine „anfassen“ und ausrichten können, ohne dass sie ins Wackeln geraten. Da es nur auf zwei Fusionsproteinen beruht, die sich unkompliziert in Bakterien produzieren lassen, ist der Ansatz sowohl kosteneffektiv als auch für viele Labore zugänglich. Indem eine große Vielfalt von Nanobody–Ziel-Paaren in steife, kryo-EM-freundliche Komplexe verwandelt wird, bietet Trimbody einen allgemeinen Weg zu atomaren Ansichten von Proteinen, die zuvor zu klein oder zu schwer fassbar waren, um sie zu untersuchen. Diese Fähigkeit kann das Verständnis krankheitsrelevanter Proteine beschleunigen und die strukturgeleitete Entwicklung von Nanobody-basierten Therapeutika und Diagnostika unterstützen.
Zitation: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Schlüsselwörter: Kryo-Elektronenmikroskopie, Nanobody-Gerüste, Proteinstruktur, KI-entworfene Proteine, kleine Membranproteine