Clear Sky Science · sv
Trimbody med styva AI‑designade stommar möjliggör kryo‑EM‑strukturbestämning i atomupplösning av små proteiner
Att se de minsta byggstenarna
Proteiner är de små maskiner som håller våra celler vid liv, men många av dem är för små för att kunna avbildas tydligt med dagens mest kraftfulla bildtekniker. Denna artikel presenterar ”Trimbody”, en elegant proteinhjälpare som får dessa små mål att se större och mer styva ut i kryoelektronmikroskopet, vilket gör det möjligt för forskare att se dem i nästan atomär detalj. Metoden lovar att påskynda grundläggande biologi och utvecklingen av nanobody‑baserade läkemedel, särskilt för läkarmål som tidigare varit för små eller för flexibla för att avbildas bra.
Varför små proteiner är svåra att se
Kryoelektronmikroskopi (kryo‑EM) har revolutionerat strukturell biologi genom att låta forskare visualisera stora biologiska molekyler i ett när‑naturligt fryst tillstånd. När proteiner däremot blir mindre än ungefär 50–100 kilodalton (en vanlig storhetsenhet för proteiner) blir de svåra att skilja från bildbrus. Deras konturer är svaga och de saknar tydliga kännetecken som datorprogram behöver för att bygga skarpa tredimensionella modeller. Existerande strategier försöker ”tjäna upp” dessa små proteiner genom att fästa dem vid större partners, men många av dessa system är komplicerade att bygga, något lösa eller fungerar bara för en snäv uppsättning mål. Forskare har behövt ett enkelt, robust sätt att få små proteiner att se stora, ljusa och stenhårda ut för kryo‑EM.
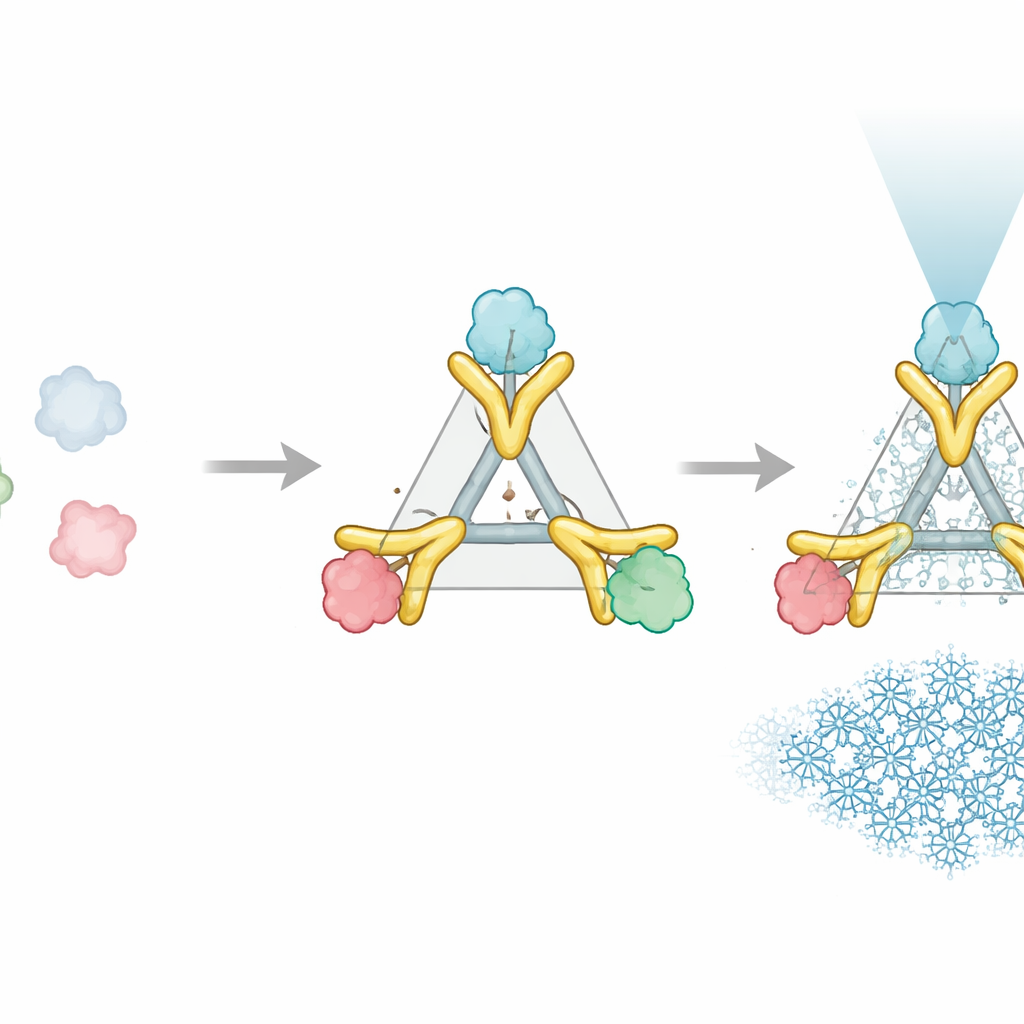
En tvådelad hjälpare som fungerar som ett styvt handtag
Trimbody‑systemet löser detta problem med bara två konstruerade delar som klickar ihop runt proteinet av intresse. Den första delen är en trimert stomme—en trearmad proteinassemblé som bildar en stabil, styv kärna. Den andra delen är en skräddarsydd nanobody, en liten antikroppsfragment som binder starkt till ett valt proteint mål. Denna nanobody förlängs med en specialdesignad ”TAIL”‑domän som greppar stommen, medan en AI‑designad ”H3” helixbunt stabiliserar stomme inifrån. Tillsammans fungerar dessa tillägg som stag och tvärbalkar och låser nanobodyn och stommen till en enda styv enhet. När tre nanobody–målkopplingar fäster vid stommens tre armar beter sig det tidigare lilla proteinet nu som en del av ett stort, symmetriskt och lättigenkännbart objekt i mikroskopet.
Att testa Trimbody
För att se om Trimbody fungerar i praktiken applicerade författarna det på flera mycket olika små proteiner. De avbildade ett mänskligt immunsystemrelaterat protein (Galectin‑10), ett grönt fluorescerande protein som ofta används som markör i laboratorium, den framre domänen av den cancerassocierade molekylen Nectin‑4, och en bakterie‑membrantransportör som förflyttar laktos över cellmembran. I varje fall bildade Trimbody‑komplexet rena, väluppförande partiklar på kryo‑EM‑galler och gav mycket detaljerade tredimensionella rekonstruktioner med upplösningar runt 2,3–2,6 ångström—tillräckligt fint för att urskilja de flesta enskilda sidokedjor hos aminosyror. Fokuserad beräkningsmässig förfining enbart på nanobody–målregionen gav ännu klarare vyer och blottlade subtila detaljer som flexibla slingor, begravda kemiska grupper och bindningsytor som tidigare var svåra att fånga. Viktigt är att för proteiner med befintliga kristallstrukturer stämde de Trimbody‑baserade kryo‑EM‑modellerna väl överens med dem, vilket visar att hjälparstommen inte förvränger målets naturliga form.
Designad styvhet och bred kompatibilitet
En central styrka hos Trimbody ligger i hur medvetet dess styvhet har konstruerats. H3‑domänen bildar ett trefaldigt helixstag som låser den utstickande bindmodulen till den trimera basen, medan TAIL‑domänen och dess fyrhelix‑länkare skapar ett andra ankarställe mellan nanobodyn och stommen. Mätningar av bindningsstyrka visade att denna dubbla förankring förbättrade nanobody–stomme‑kopplingen med ungefär fyra storleksordningar, vilket kraftigt minskar oönskade rörelser som kan sudda ut kryo‑EM‑bilder. Författarna analyserade också många befintliga nanobody–proteinstrukturer för att kontrollera hur ofta Trimbody skulle råka ut för steriska krockar—situationer där stommen skulle stöta i proteinet självt. Deras undersökning antyder att för de flesta nanobodyer och mål kan systemet göras kompatibelt genom att justera en liten uppsättning ramverksresiduer och testa komplexbildning med standardbiokemiska analyser.
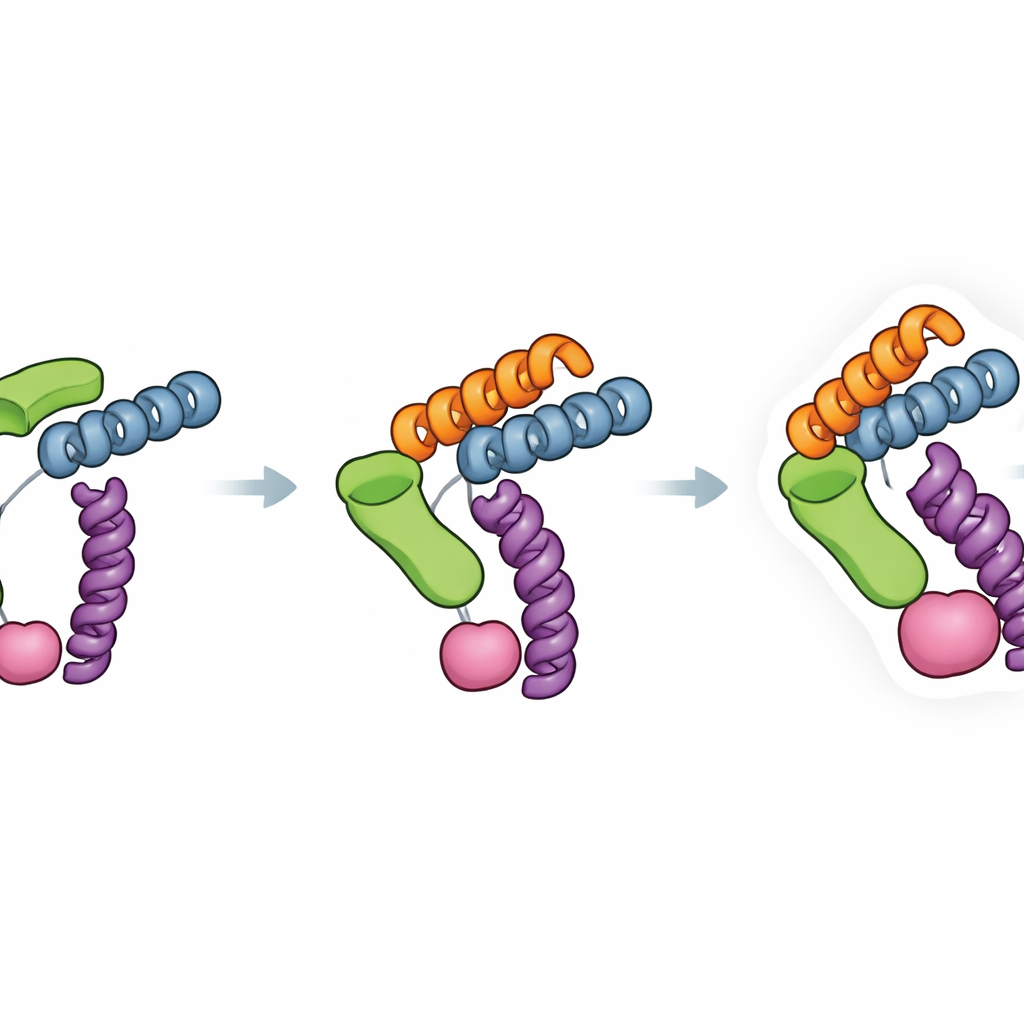
Att öppna ett klarare fönster mot små mål
I vardagliga termer fungerar Trimbody som ett precisionshandtag som låter mikroskop ”gripa” och orientera mycket små proteiner utan att de skakar. Eftersom det bygger på bara två fusionsproteiner som är enkla att producera i bakterier är tillvägagångssättet både kostnadseffektivt och tillgängligt för många laboratorier. Genom att förvandla en mängd olika nanobody–målpar till styva, kryo‑EM‑vänliga komplex erbjuder Trimbody en generell väg till atomnivåvyer av proteiner som tidigare varit för små eller för flyktiga för att studeras. Denna kapacitet kan påskynda förståelsen av sjukdomsrelaterade proteiner och stödja snabbare, strukturstyrd utveckling av nanobody‑baserade läkemedel och diagnostik.
Citering: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Nyckelord: kryoelektronmikroskopi, nanobody‑stommar, proteinstruktur, AI‑designade proteiner, små membranproteiner