Clear Sky Science · it
Trimbody con impalcature rigide progettate con IA consente la determinazione strutturale in crio-EM a risoluzione atomica di proteine piccole
Osservare i più piccoli mattoni della vita
Le proteine sono le macchine minuscole che mantengono in vita le nostre cellule, ma molte di esse sono troppo piccole per essere viste chiaramente con gli strumenti di imaging attualmente più potenti. Questo articolo presenta “Trimbody”, un assistente proteico intelligente che rende questi obiettivi minuscoli più grandi e rigidi al microscopio crio-elettronico, permettendo agli scienziati di osservarli a dettaglio quasi atomico. Il metodo promette di accelerare la biologia di base e lo sviluppo di farmaci a base di nanobody, specialmente per bersagli terapeutici che in precedenza erano troppo piccoli o troppo flessibili per essere immaginati con precisione.
Perché le proteine piccole sono difficili da vedere
La crio-microscopia elettronica (crio-EM) ha rivoluzionato la biologia strutturale permettendo ai ricercatori di visualizzare grandi molecole biologiche in uno stato congelato vicino al naturale. Tuttavia, quando le proteine diventano più piccole di circa 50–100 kilodalton (una unità di massa comune per le proteine), diventano difficili da distinguere dal rumore nelle immagini. I loro contorni sono deboli e mancano di caratteristiche marcate che i programmi informatici utilizzano per assemblare modelli tridimensionali nitidi. Le strategie esistenti cercano di “ingrassare” queste piccole proteine attaccandole a partner più grandi, ma molti di questi sistemi sono complicati da costruire, un po’ flessibili o funzionano solo per un insieme ristretto di bersagli. Gli scienziati avevano bisogno di un modo semplice e robusto per far apparire le piccole proteine grandi, luminose e solide per la crio-EM.
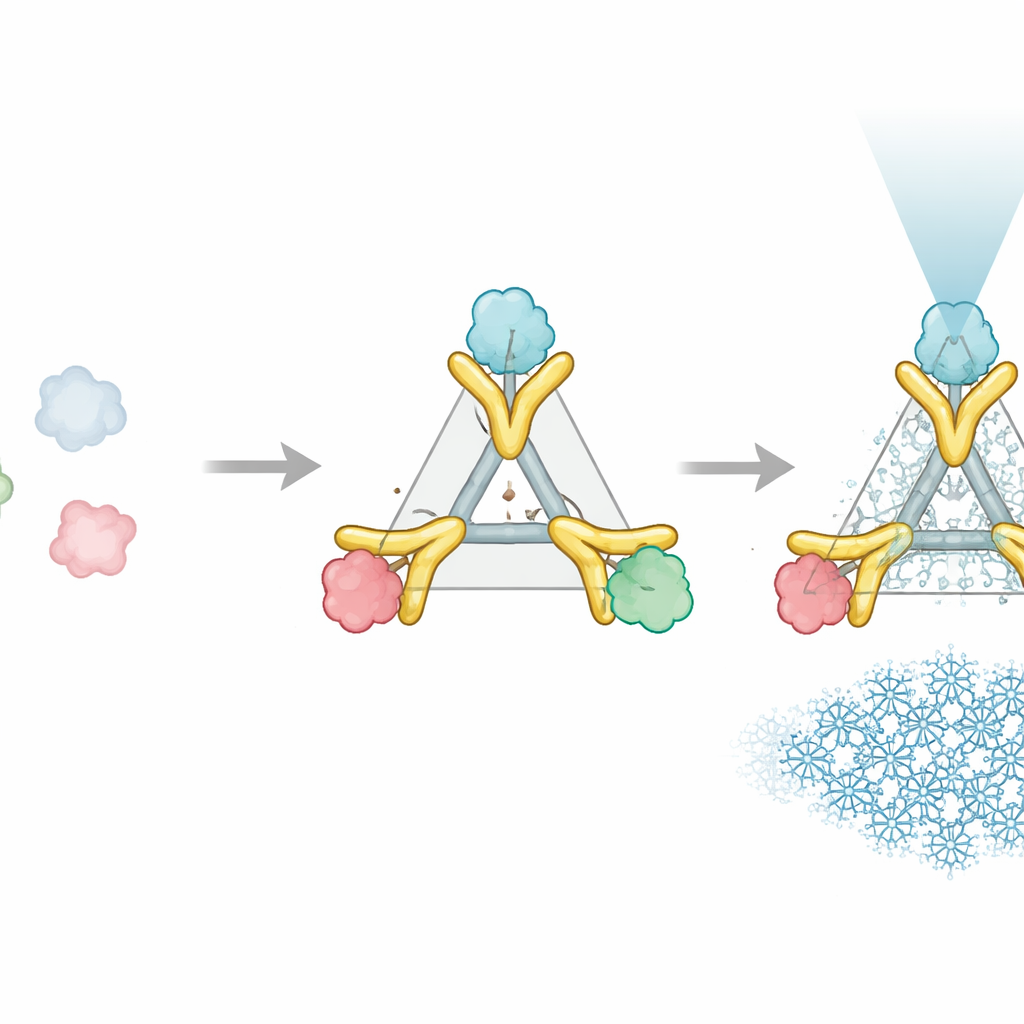
Un aiuto in due parti che funziona come una maniglia rigida
Il sistema Trimbody risolve questo problema con soli due componenti ingegnerizzati che si incastrano attorno alla proteina di interesse. La prima parte è un’impalcatura trimetrica—un assemblaggio proteico a tre bracci che forma un nucleo stabile e rigido. La seconda parte è un nanobody personalizzato, un piccolo frammento di anticorpo che si lega saldamente al bersaglio scelto. Questo nanobody è esteso con un dominio “TAIL” appositamente progettato che aggancia l’impalcatura, mentre un fascio elicoidale “H3” progettato con IA stabilizza l’impalcatura dall’interno. Insieme, questi elementi funzionano come staffe e traverse, bloccando il nanobody e l’impalcatura in un’unità singola e rigida. Quando tre coppie nanobody–bersaglio si attaccano ai tre bracci dell’impalcatura, la proteina precedentemente minuscola si comporta ora come parte di un oggetto grande, simmetrico e facilmente riconoscibile al microscopio.
Mettere alla prova il Trimbody
Per verificare se Trimbody funziona nella pratica, gli autori lo hanno applicato a diverse proteine piccole e molto diverse tra loro. Hanno immaginato una proteina umana legata al sistema immunitario (Galectin-10), una proteina fluorescente verde spesso usata come marcatore di laboratorio, il dominio frontale della molecola associata al cancro Nectin-4, e un trasportatore di membrana batterico che muove il lattosio attraverso le membrane cellulari. In ciascun caso, il complesso Trimbody ha formato particelle pulite e ben comportate sulle griglie di crio-EM e ha prodotto ricostruzioni tridimensionali altamente dettagliate con risoluzioni intorno a 2,3–2,6 angstrom—abbastanza fini da distinguere la maggior parte delle catene laterali degli amminoacidi. Un raffinamento computazionale mirato solo sulla regione nanobody–bersaglio ha fornito viste ancora più chiare, rivelando caratteristiche sottili come anse flessibili, gruppi chimici sepolti e superfici di legame che prima erano difficili da catturare. Importante, per le proteine con strutture cristalline esistenti, i modelli cri0-EM basati su Trimbody corrispondevano strettamente a queste, dimostrando che l’impalcatura ausiliaria non deforma la forma naturale del bersaglio.
Rigidità progettata e ampia compatibilità
Un punto di forza chiave di Trimbody risiede in come è stata progettata deliberatamente la sua rigidità. Il dominio H3 forma una staffa elicoidale a tre vie che blocca il modulo di legame sporgente alla base trimetrica, mentre il dominio TAIL e il suo linker a quattro eliche creano un secondo ancoraggio tra il nanobody e l’impalcatura. Le misurazioni della forza di legame hanno mostrato che questo ancoraggio doppio ha migliorato l’attacco nanobody–impalcatura di circa quattro ordini di grandezza, riducendo notevolmente i movimenti indesiderati che possono sfocare le immagini crio-EM. Gli autori hanno inoltre analizzato molte strutture nanobody–proteina esistenti per verificare con quale frequenza Trimbody incontrerebbe collisioni steriche—situazioni in cui l’impalcatura urterebbe la proteina stessa. La loro indagine suggerisce che, per la maggior parte dei nanobody e dei bersagli, il sistema può essere reso compatibile modificando un piccolo insieme di residui del framework e testando la formazione del complesso con saggi biochimici standard.
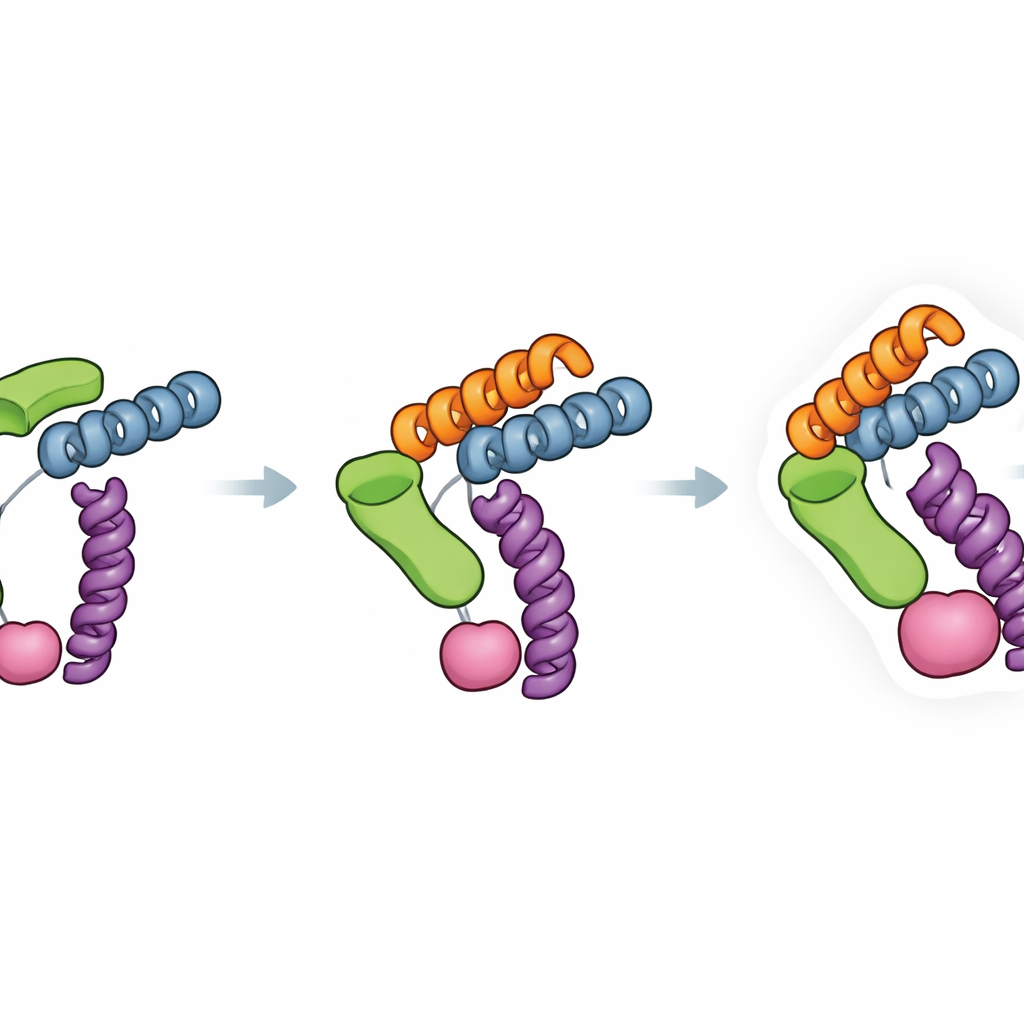
Aprire una finestra più chiara sui bersagli minuscoli
In termini pratici, Trimbody agisce come una maniglia di precisione che permette ai microscopi di “afferrare” e allineare proteine molto piccole senza scuoterle. Poiché si basa su sole due proteine di fusione facili da produrre in batteri, l’approccio è sia conveniente che accessibile a molti laboratori. Trasformando una vasta gamma di coppie nanobody–bersaglio in complessi rigidi e compatibili con la crio-EM, Trimbody offre una strada generale verso viste a livello atomico di proteine che in precedenza erano troppo piccole o troppo elusive per essere studiate. Questa capacità può accelerare la comprensione delle proteine correlate a malattie e supportare uno sviluppo più rapido, guidato dalla struttura, di farmaci e diagnostici a base di nanobody.
Citazione: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Parole chiave: crio-microscopia elettronica, impalcature per nanobody, struttura proteica, proteine progettate con IA, piccole proteine di membrana