Clear Sky Science · ru
Trimbody с жёсткими каркасами, разработанными ИИ, позволяет определять структуры малых белков методом крио-ЭМ с атомным разрешением
Наблюдая мельчайшие строительные блоки
Белки — это крошечные машины, которые поддерживают жизнь клетки, но многие из них слишком малы, чтобы их можно было чётко увидеть современными мощными инструментами. В этой работе представлен «Trimbody», умный белковый помощник, который делает эти крошечные мишени визуально больше и более жёсткими в крио-электронном микроскопе, позволяя учёным рассматривать их почти с атомной детализацией. Метод обещает ускорить фундаментальную биологию и разработку препаратов на основе нанотел, особенно для лекарственных целей, которые ранее были слишком малы или слишком гибки для качественной визуализации.
Почему малые белки трудно увидеть
Крио-электронная микроскопия (крио-ЭМ) произвела революцию в структурной биологии, позволив исследовать крупные биомолекулы в состоянии близком к нативному, замороженными. Однако когда белки становятся меньше примерно 50–100 килодальтонов (общее единичное обозначение массы для белков), их трудно отличить от шума на изображениях. Их контуры слабо выражены, и им не хватает характерных признаков, которые необходимы программам для сборки чётких трёхмерных моделей. Существующие стратегии пытаются «увеличить объём» таких белков, присоединяя их к крупным партнёрам, но многие из этих систем сложны в сборке, относительно подвижны или работают только для узкого круга мишеней. Учёным требовался простой и надёжный способ сделать малые белки большими, яркими и твёрдыми для крио-ЭМ.
Двухчастный помощник, действующий как жёсткая ручка
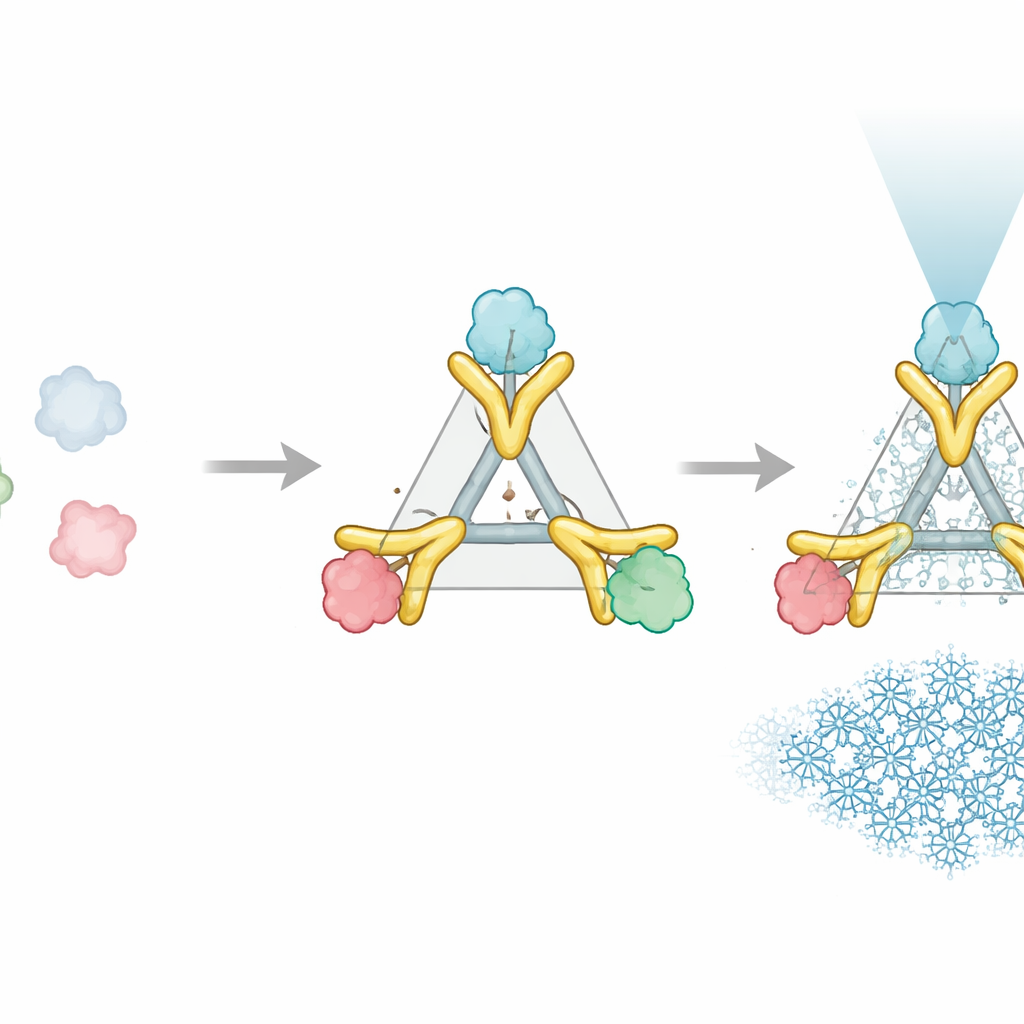
Система Trimbody решает эту проблему всего двумя спроектированными компонентами, которые защёлкиваются вокруг целевого белка. Первый компонент — тримерный каркас, трёхлучевая белковая сборка, образующая стабильное, жёсткое ядро. Второй компонент — индивидуальная нанотело (nanobody), крошечная фрагментарная антитела, которая плотно связывается с выбранной мишенью. Это нанотело удлиняется специально разработанным доменом «TAIL», который захватывает каркас, а внутри каркаса стабилизирует сам каркас спиральный пучок «H3», созданный с помощью ИИ. Эти дополнения вместе действуют как распорки и перекладины, фиксируя нанотело и каркас в единую жёсткую единицу. Когда три пары «нанотело–мишень» прикрепляются к трем рукояткам каркаса, ранее крошечный белок начинает вести себя как часть крупного, симметричного и легко узнаваемого объекта в микроскопе.
Проверка Trimbody в деле
Чтобы оценить работоспособность Trimbody на практике, авторы применили его к нескольким очень разным малым белкам. Они снимали человеческий иммунный белок (Galectin-10), зелёный флуоресцентный белок, часто используемый как лабораторный маркер, передний домен молекулы Nectin-4, связанной с раком, и бактериальный мембранный транспортёр, перемещающий лактозу через мембраны. В каждом случае комплекс Trimbody формировал чистые, однородные частицы на крио-ЭМ решётках и давал высокодетализированные трёхмерные реконструкции с разрешением около 2,3–2,6 ангстрема — достаточно, чтобы различить большинство боковых цепей аминокислот. Сфокусированная вычислительная доработка только в области нанотело–мишень дала ещё более чёткие картины, выявив тонкие детали, такие как гибкие петли, погружённые химические группы и поверхности связывания, которые ранее было трудно зафиксировать. Важно, что для белков с уже известными кристаллическими структурами моделированные на основе Trimbody крио-ЭМ структуры были тесно согласованы с ними, демонстрируя, что вспомогательный каркас не искажает естественную форму мишени.
Спроектированная жёсткость и широкая совместимость
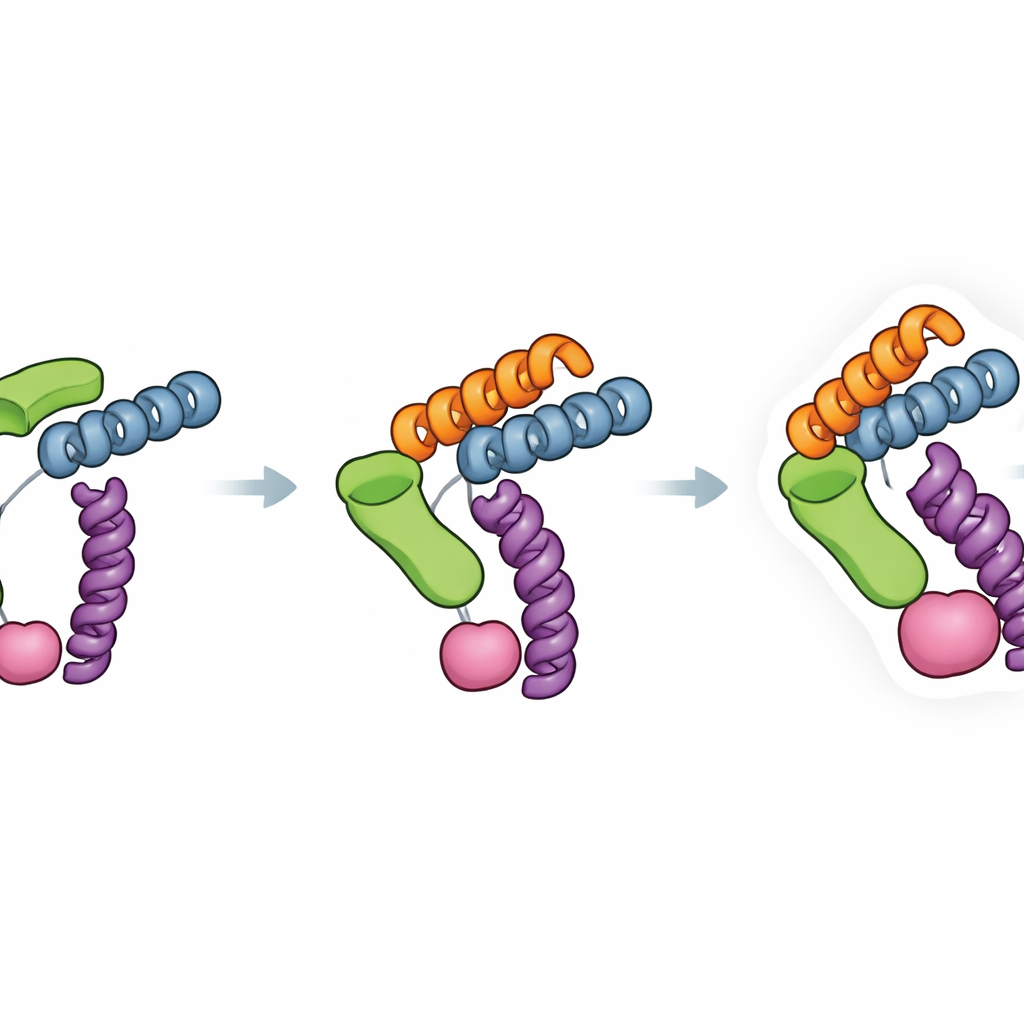
Ключевая сила Trimbody заключается в том, насколько целенаправленно была разработана его жёсткость. Домен H3 образует трёхстороннюю спиральную распорку, которая фиксирует выступающий модуль связывания с тримерной основой, в то время как домен TAIL и его четвёртиспиральный линкер создают вторую точку крепления между нанотело и каркасом. Измерения силы связывания показали, что такое двойное якорение улучшает прикрепление нанотело к каркасу примерно на четыре порядка величины, значительно снижая нежелательную подвижность, размывающую изображения крио-ЭМ. Авторы также проанализировали множество существующих структур пар нанотело–белок, чтобы оценить, как часто Trimbody столкнётся со стерическими препятствиями — ситуациями, когда каркас будет мешать самому белку. Их обзор показывает, что для большинства нанотел и мишеней систему можно сделать совместимой, скорректировав небольшой набор остовных остатков и проверив образование комплекса стандартными биохимическими тестами.
Открывая более чёткое окно на крошечные мишени
В повседневном понимании Trimbody действует как точно изготовленная ручка, позволяющая микроскопам «схватить» и выровнять очень малые белки без дрожания. Поскольку он опирается всего на два белковых слияния, которые просто производить в бактериях, подход является экономичным и доступным для многих лабораторий. Превращая широкий набор пар «нанотело–мишень» в жёсткие, пригодные для крио-ЭМ комплексы, Trimbody предлагает общий путь к атомным картам белков, которые ранее были слишком малы или ускользающими для изучения. Эта возможность может ускорить понимание белков, связанных с заболеваниями, и поддержать более быстую структурно-ориентированную разработку нанотел и диагностик.
Цитирование: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Ключевые слова: криоэлектронная микроскопия, каркасы нанотел, структура белка, белки, разработанные ИИ, малые мембранные белки