Clear Sky Science · pl
Trimbody z sztywnymi, zaprojektowanymi przez AI rusztowaniami umożliwia określenie struktury małych białek metodą kriotomografii elektronowej w rozdzielczości atomowej
Widzieć najmniejsze cegiełki
Białka to drobne maszyny podtrzymujące życie komórek, lecz wiele z nich jest zbyt małych, by dało się je wyraźnie zobaczyć za pomocą najpotężniejszych narzędzi obrazowania. W artykule przedstawiono „Trimbody” — sprytny, oparty na białkach pomocnik, który sprawia, że te maleńkie cele wyglądają większe i bardziej sztywne pod mikroskopem elektronowym w kriogenicznych warunkach, pozwalając naukowcom zobaczyć je z niemal atomową szczegółowością. Metoda obiecuje przyspieszyć badania podstawowe i rozwój leków opartych na nanoprzeciwciałach, zwłaszcza w odniesieniu do celów terapeutycznych, które wcześniej były zbyt małe lub zbyt elastyczne, by je dobrze zobrazować.
Dlaczego małe białka trudno dostrzec
Kriotomografia elektronowa (cryo-EM) zrewolucjonizowała biologię strukturalną, umożliwiając badaczom wizualizację dużych cząsteczek biologicznych w stanie bliskim naturalnemu, zamrożonym. Jednak gdy białka robią się mniejsze niż około 50–100 kilodaltonów (powszechna jednostka masy w białkach), stają się trudne do odróżnienia od szumu na obrazach. Ich kontury są słabe, brakuje im wyraźnych cech, których programy komputerowe potrzebują do złożenia ostrych modeli trójwymiarowych. Istniejące strategie próbują „powiększyć” te małe białka przez przyłączenie ich do większych partnerów, ale wiele z tych systemów jest skomplikowanych w budowie, do pewnego stopnia wiotkich lub działa tylko dla wąskiego zestawu celów. Naukowcy potrzebowali prostego, niezawodnego sposobu, aby małe białka wyglądały na duże, wyraźne i sztywne dla cryo-EM.
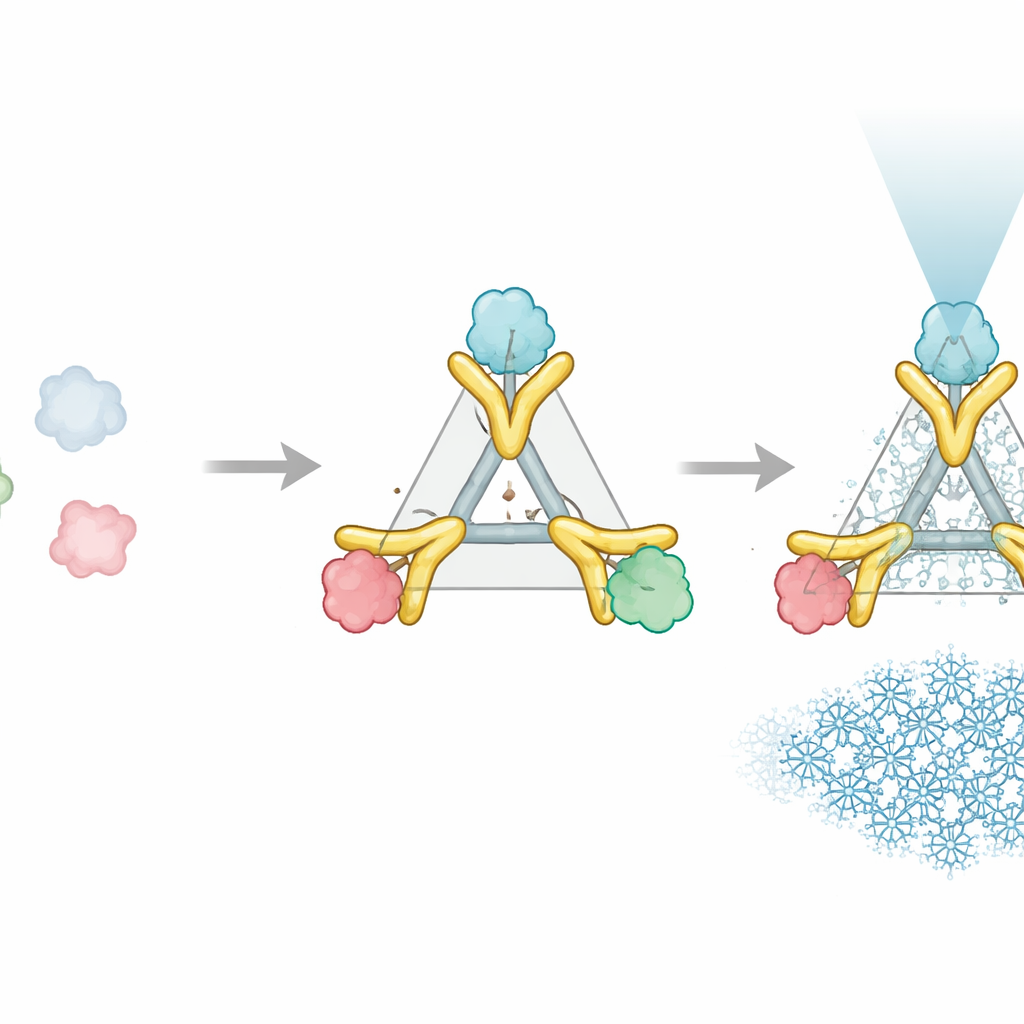
Dwu‑częściowy pomocnik działający jak sztywna rączka
System Trimbody rozwiązuje ten problem przy użyciu zaledwie dwóch zaprojektowanych elementów, które zatrzaskują się wokół białka docelowego. Pierwszy element to trimerowe rusztowanie — trójramienna struktura białkowa tworząca stabilne, sztywne jądro. Drugi element to spersonalizowana nanoprzeciwciało, mały fragment przeciwciała, który ściśle wiąże się z wybranym celem białkowym. To nanoprzeciwciało jest wydłużone za pomocą specjalnie zaprojektowanej domeny „TAIL”, która chwyta rusztowanie, podczas gdy zaprojektowany przez AI pakiet helikalny „H3” stabilizuje rusztowanie od wewnątrz. Razem te dodatki działają jak wzmocnienia i poprzeczki, blokując nanoprzeciwciało i rusztowanie w jedną sztywną jednostkę. Gdy trzy pary nanoprzeciwciało–cel przyłączą się do trzech ramion rusztowania, wcześniej maleńkie białko zaczyna zachowywać się jak część dużego, symetrycznego i łatwo rozpoznawalnego obiektu pod mikroskopem.
Testowanie Trimbody
Aby sprawdzić, czy Trimbody działa praktycznie, autorzy zastosowali go do kilku bardzo różnych małych białek. Obrazowali ludzkie białko związane z układem odpornościowym (Galectin-10), zielone białko fluorescencyjne często używane jako marker laboratoryjny, domenę zewnętrzną powiązanego z rakiem białka Nectin-4 oraz bakteryjny transporter błonowy przepuszczający laktozę. W każdym przypadku kompleks Trimbody tworzył czyste, dobrze zachowane cząsteczki na kratach do cryo-EM i dawał wysoko szczegółowe rekonstrukcje trójwymiarowe o rozdzielczości około 2,3–2,6 angstroma — wystarczająco precyzyjne, by rozróżnić większość pojedynczych łańcuchów bocznych aminokwasów. Skoncentrowane obliczeniowe dopracowanie jedynie obszaru nanoprzeciwciało–cel dało jeszcze wyraźniejsze obrazy, ukazując subtelne cechy takie jak elastyczne pętle, schowane grupy chemiczne i powierzchnie wiążące, które wcześniej trudno było uchwycić. Co ważne, w przypadku białek, dla których istniały struktury krystaliczne, modele cryo-EM oparte na Trimbody były z nimi w dobrym zgodności, pokazując, że pomocnicze rusztowanie nie zniekształca naturalnego kształtu celu.
Projektowana sztywność i szeroka zgodność
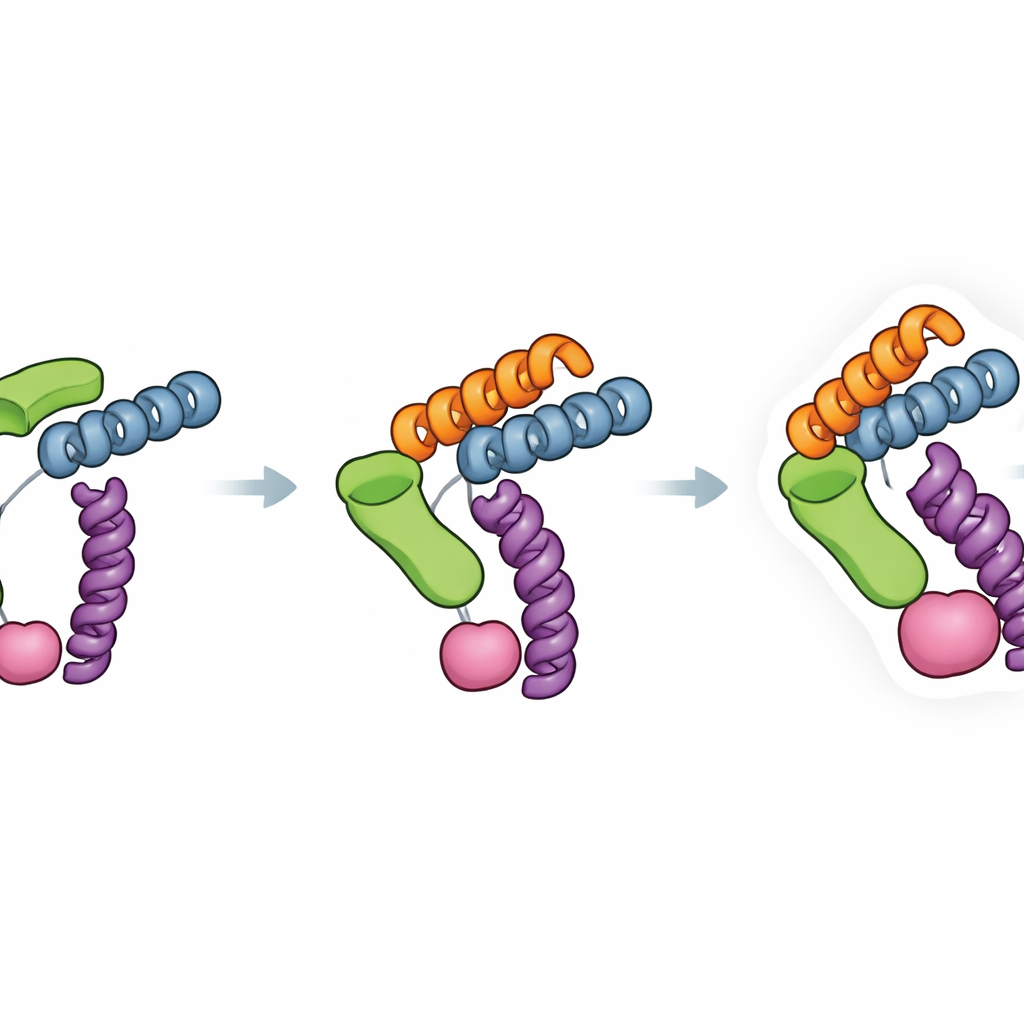
Kluczową siłą Trimbody jest celowo zaprojektowana sztywność. Domena H3 tworzy trójdrożne helikalne wzmocnienie, które blokuje wystającą część wiążącą z trimerową podstawą, podczas gdy domena TAIL i jej czterowo‑heliksowy łącznik tworzą drugie zakotwiczenie między nanoprzeciwciałem a rusztowaniem. Pomiary siły wiązania wykazały, że to podwójne zakotwiczenie poprawiło przyczepność nanoprzeciwciało–rusztowanie o około cztery rzędy wielkości, znacznie zmniejszając niepożądane ruchy, które mogą rozmazywać obrazy cryo-EM. Autorzy przeanalizowali także wiele istniejących struktur nanoprzeciwciało–białko, by sprawdzić, jak często Trimbody napotkałby konflikty steryczne — sytuacje, w których rusztowanie uderzałoby w samo białko. Ich przegląd sugeruje, że dla większości nanoprzeciwciał i celów system można dostosować przez modyfikację niewielkiego zestawu reszt szkieletowych i przetestowanie tworzenia kompleksu standardowymi testami biochemicznymi.
Otwierając jaśniejsze okno na malutkie cele
Mówiąc prosto, Trimbody działa jak precyzyjnie wykonana rączka, która pozwala mikroskopom „uchwycić” i wyrównać bardzo małe białka bez drżenia. Ponieważ opiera się tylko na dwóch białkach fuzyjnych, które są proste do wyprodukowania w bakteriach, podejście jest zarówno opłacalne, jak i dostępne dla wielu laboratoriów. Przekształcając szeroką gamę par nanoprzeciwciało–cel w sztywne kompleksy przyjazne dla cryo-EM, Trimbody oferuje ogólną drogę do widoków na poziomie atomowym białek, które wcześniej były zbyt małe lub zbyt ulotne, by je badać. Ta zdolność może przyspieszyć zrozumienie białek związanych z chorobami oraz wesprzeć szybszy, oparty na strukturze rozwój leków i diagnostyki opartych na nanoprzeciwciałach.
Cytowanie: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Słowa kluczowe: kriotomografia elektronowa, rusztowania nanoprzeciwciał, struktura białka, białka zaprojektowane przez AI, małe białka błonowe