Clear Sky Science · fr
Trimbody avec échafaudages rigides conçus par IA permet la détermination de structures cryo‑EM à résolution atomique de protéines de petite taille
Voir les plus petits éléments constitutifs
Les protéines sont les minuscules machines qui maintiennent nos cellules en vie, mais beaucoup d’entre elles sont trop petites pour être distinguées clairement avec les outils d’imagerie les plus puissants actuels. Cet article présente « Trimbody », un assistant ingénieux à base de protéines qui fait paraître ces cibles minuscules plus grandes et plus rigides au microscope cryo‑électronique, permettant aux chercheurs de les visualiser avec un niveau de détail proche de l’échelle atomique. La méthode promet d’accélérer la biologie fondamentale et le développement de médicaments à base de nanocorps, en particulier pour des cibles thérapeutiques auparavant trop petites ou trop flexibles pour être bien imagées.
Pourquoi les petites protéines sont difficiles à voir
La microscopie cryo‑électronique (cryo‑EM) a révolutionné la biologie structurale en permettant d’observer de grandes molécules biologiques dans un état congelé proche du natif. Cependant, lorsque les protéines deviennent plus petites qu’environ 50–100 kilodaltons (une unité de taille courante pour les protéines), elles deviennent difficiles à distinguer du bruit dans les images. Leurs contours sont faibles et elles manquent de motifs marquants dont les algorithmes ont besoin pour assembler des modèles tridimensionnels nets. Les stratégies existantes cherchent à « grossir » ces petites protéines en les attachant à des partenaires plus volumineux, mais beaucoup de ces systèmes sont compliqués à construire, relativement flexibles, ou ne fonctionnent que pour un nombre limité de cibles. Les scientifiques avaient besoin d’un moyen simple et robuste rendant les petites protéines grandes, lumineuses et rigides pour la cryo‑EM.
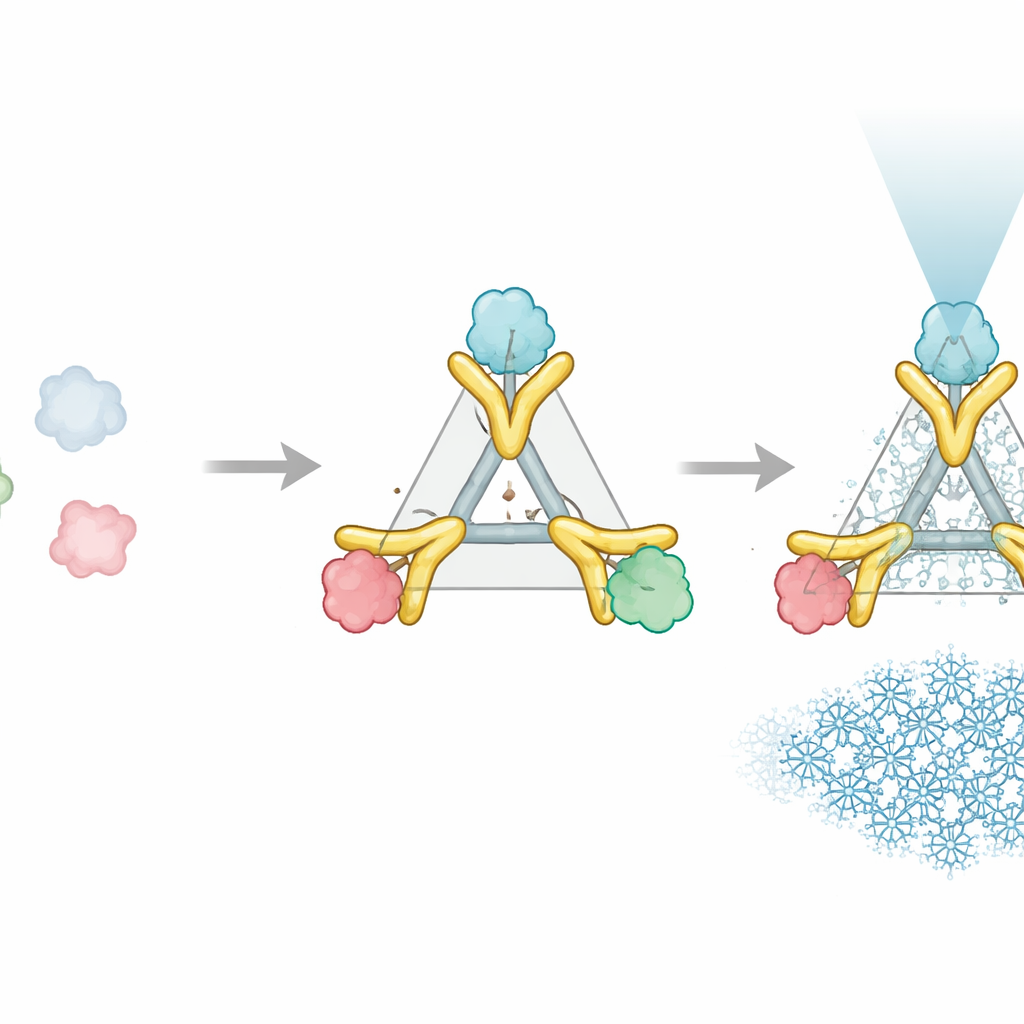
Un aide en deux parties qui agit comme une poignée rigide
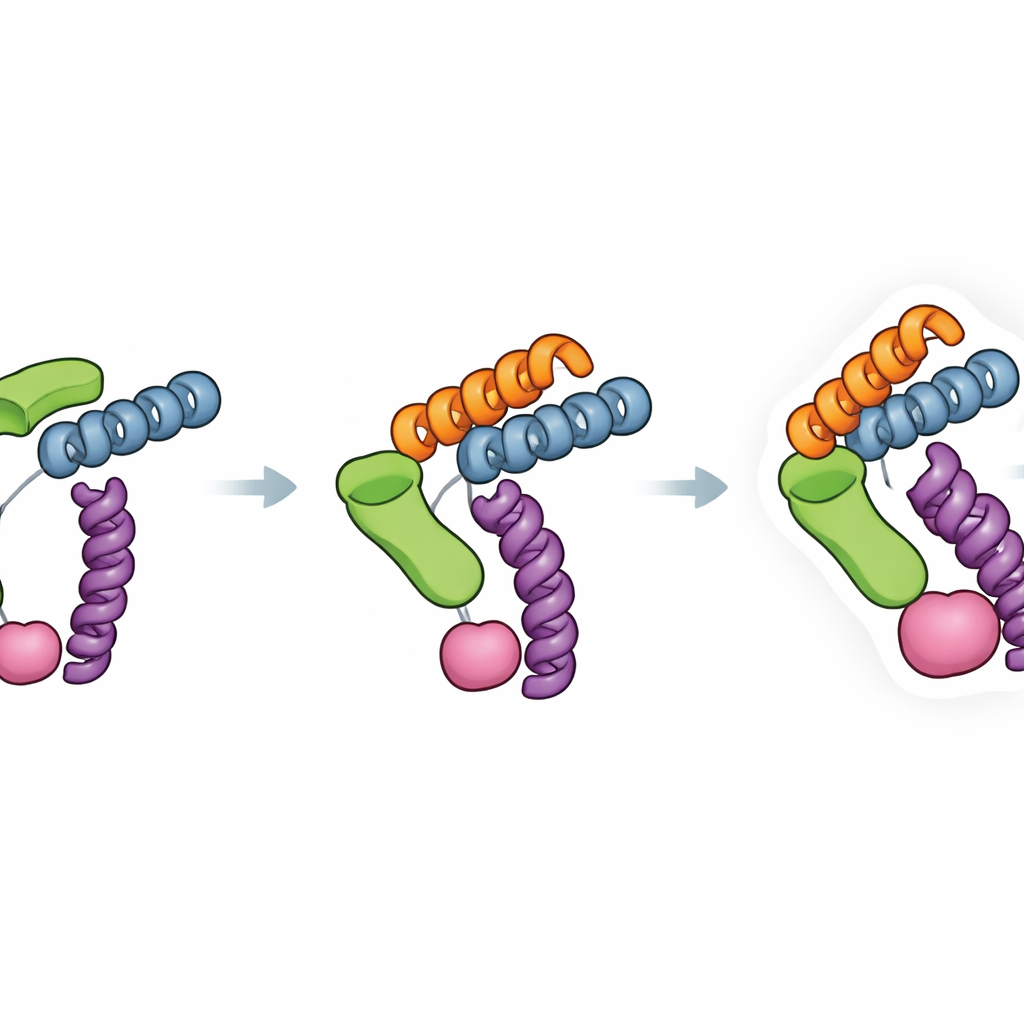
Le système Trimbody résout ce problème avec seulement deux éléments conçus qui s’emboîtent autour de la protéine d’intérêt. La première partie est un échafaudage trimérique — un assemblage protéique à trois bras qui forme un noyau stable et rigide. La seconde est un nanocorps personnalisé, un petit fragment d’anticorps qui se lie fortement à la protéine cible choisie. Ce nanocorps est prolongé par un domaine « TAIL » spécialement conçu qui accroche l’échafaudage, tandis qu’un empilement hélicoïdal « H3 » conçu par IA stabilise l’échafaudage de l’intérieur. Ensemble, ces ajouts fonctionnent comme des supports et des traverses, verrouillant le nanocorps et l’échafaudage en une seule unité rigide. Lorsque trois paires nanocorps–cible se fixent aux trois bras de l’échafaudage, la protéine auparavant minuscule se comporte désormais comme partie d’un objet grand, symétrique et facilement reconnaissable au microscope.
Mettre Trimbody à l’épreuve
Pour vérifier l’efficacité de Trimbody en pratique, les auteurs l’ont appliqué à plusieurs petites protéines très différentes. Ils ont imagé une protéine humaine liée au système immunitaire (Galectin‑10), une protéine fluorescente verte souvent utilisée comme marqueur en laboratoire, le domaine frontal de la molécule liée au cancer Nectin‑4, et un transporteur membranaire bactérien qui transporte le lactose à travers les membranes cellulaires. Dans chaque cas, le complexe Trimbody a formé des particules propres et bien comportées sur les grilles cryo‑EM et a produit des reconstructions tridimensionnelles très détaillées avec des résolutions autour de 2,3–2,6 angströms — suffisamment fines pour distinguer la plupart des chaînes latérales individuelles d’acides aminés. Un raffinement computationnel focalisé uniquement sur la région nanocorps–cible a fourni des vues encore plus nettes, révélant des caractéristiques subtiles comme des boucles flexibles, des groupes chimiques enfouis et des surfaces de liaison qui étaient auparavant difficiles à capturer. Fait important, pour les protéines disposant déjà de structures cristallines, les modèles cryo‑EM basés sur Trimbody les ont fidèlement reproduites, montrant que l’échafaudage d’assistance ne déforme pas la forme naturelle de la cible.
Rigidité conçue et compatibilité étendue
Une force clé de Trimbody réside dans la façon dont sa rigidité a été délibérément ingénierée. Le domaine H3 forme une bride hélicoïdale tripode qui verrouille le module de liaison saillant sur la base trimérique, tandis que le domaine TAIL et son connecteur à quatre hélices créent une seconde ancre entre le nanocorps et l’échafaudage. Les mesures de la force d’interaction ont montré que cette double ancrage améliore l’attachement nanocorps–échafaudage d’environ quatre ordres de grandeur, réduisant considérablement les mouvements indésirables qui peuvent brouiller les images cryo‑EM. Les auteurs ont également analysé de nombreuses structures existantes nanocorps–protéine pour vérifier la fréquence des clashes stériques — situations où l’échafaudage heurterait la protéine elle‑même. Leur enquête suggère que, pour la plupart des nanocorps et des cibles, le système peut être rendu compatible en ajustant un petit ensemble de résidus du cadre et en testant la formation du complexe avec des essais biochimiques standards.
Ouvrir une fenêtre plus nette sur les petites cibles
En termes quotidiens, Trimbody agit comme une poignée conçue avec précision qui permet aux microscopes de « saisir » et d’aligner de très petites protéines sans les agiter. Parce qu’il repose sur seulement deux protéines de fusion faciles à produire en bactéries, cette approche est à la fois économique et accessible à de nombreux laboratoires. En transformant une grande variété de paires nanocorps–cible en complexes rigides et compatibles avec la cryo‑EM, Trimbody offre une voie générale vers des vues à l’échelle atomique de protéines auparavant trop petites ou trop insaisissables pour être étudiées. Cette capacité peut accélérer la compréhension des protéines impliquées dans les maladies et soutenir le développement plus rapide, guidé par la structure, de médicaments et diagnostics à base de nanocorps.
Citation: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Mots-clés: microscopie cryo‑électronique, échafaudages de nanocorps, structure des protéines, protéines conçues par IA, petites protéines membranaires