Clear Sky Science · es
Trimbody con andamios rígidos diseñados por IA permite la determinación por crio-EM de la estructura de proteínas pequeñas a resolución atómica
Ver los bloques de construcción más pequeños
Las proteínas son las pequeñas máquinas que mantienen vivas nuestras células, pero muchas de ellas son demasiado pequeñas para verse con claridad con las herramientas de imagen más potentes actuales. Este artículo presenta “Trimbody”, un ingenioso ayudante basado en proteínas que hace que estos objetivos diminutos parezcan más grandes y rígidos bajo un microscopio crioelectrónico, permitiendo a los científicos verlos con detalle casi atómico. El método promete acelerar la biología básica y el desarrollo de fármacos basados en nanocuerpos, especialmente para dianas farmacológicas que antes eran demasiado pequeñas o flexibles para obtener buenas imágenes.
Por qué es difícil ver las proteínas pequeñas
La microscopía crioelectrónica (crio-EM) ha revolucionado la biología estructural al permitir a los investigadores visualizar grandes moléculas biológicas en un estado congelado cercano al nativo. Sin embargo, cuando las proteínas son más pequeñas de unos 50–100 kilodaltons (una unidad de tamaño común para proteínas), se vuelven difíciles de distinguir del ruido en las imágenes. Sus contornos son débiles y carecen de rasgos llamativos que los programas informáticos necesitan para ensamblar modelos tridimensionales nítidos. Las estrategias existentes intentan “engrosar” estas proteínas pequeñas uniéndolas a socios mayores, pero muchos de estos sistemas son complicados de construir, algo flexibles o funcionan solo para un conjunto limitado de dianas. Los científicos necesitaban una forma simple y robusta de hacer que las proteínas pequeñas parecieran grandes, brillantes y sólidas para la crio-EM.
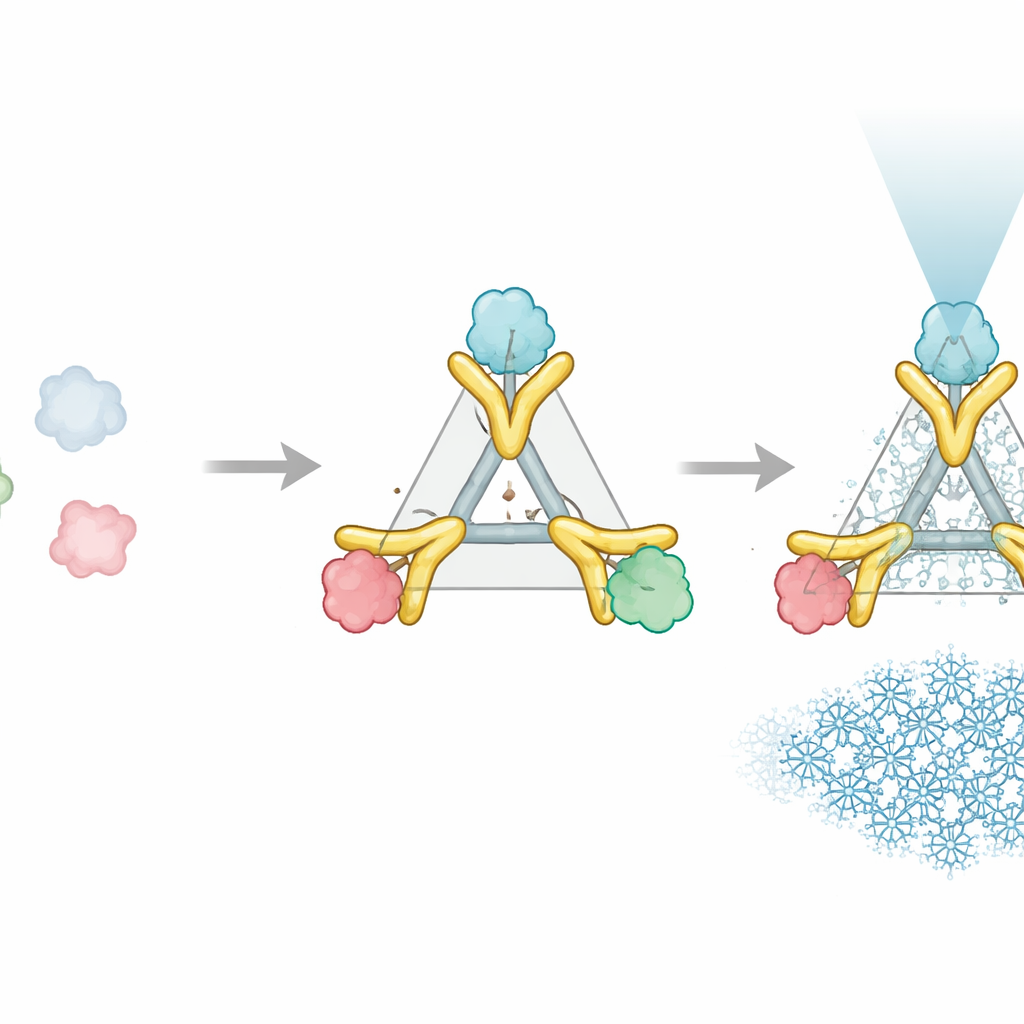
Un ayudante de dos partes que actúa como un mango rígido
El sistema Trimbody resuelve este problema con solo dos componentes diseñados que encajan alrededor de la proteína de interés. La primera parte es un andamio trimérico—una ensambladura proteica de tres brazos que forma un núcleo estable y rígido. La segunda parte es un nanocuerpo personalizado, un fragmento de anticuerpo diminuto que se une con fuerza a una diana proteica elegida. Este nanocuerpo se extiende con un dominio “TAIL” especialmente diseñado que se agarra al andamio, mientras que un haz helicoidal “H3” diseñado por IA estabiliza el andamio desde el interior. Juntos, estas adiciones actúan como refuerzos y travesaños, bloqueando el nanocuerpo y el andamio en una única unidad rígida. Cuando tres pares nanocuerpo–diana se unen a los tres brazos del andamio, la proteína anteriormente pequeña se comporta ahora como parte de un objeto grande, simétrico y fácilmente reconocible en el microscopio.
Poniendo a prueba Trimbody
Para comprobar si Trimbody funciona en la práctica, los autores lo aplicaron a varias proteínas muy distintas entre sí. Obtuvieron imágenes de una proteína humana relacionada con el sistema inmune (Galectina-10), una proteína fluorescente verde usada a menudo como marcador de laboratorio, el dominio delantero de la molécula ligada al cáncer Nectin-4 y un transportador de membrana bacteriano que mueve lactosa a través de membranas celulares. En cada caso, el complejo Trimbody formó partículas limpias y bien comportadas en las rejillas de crio-EM y produjo reconstrucciones tridimensionales altamente detalladas con resoluciones en torno a 2,3–2,6 angstroms—lo bastante finas para distinguir la mayoría de las cadenas laterales individuales de aminoácidos. El refinamiento computacional centrado solo en la región nanocuerpo–diana ofreció vistas aún más nítidas, revelando rasgos sutiles como bucles flexibles, grupos químicos enterrados y superficies de unión que antes eran difíciles de capturar. Es importante destacar que, para proteínas con estructuras cristalinas existentes, los modelos por crio-EM basados en Trimbody coincidieron de cerca con ellas, demostrando que el andamio ayudante no distorsiona la forma natural de la diana.
Rigidez diseñada y amplia compatibilidad
Una fortaleza clave de Trimbody reside en lo deliberadamente que se diseñó su rigidez. El dominio H3 forma un refuerzo helicoidal trifurcado que bloquea el módulo de unión proyectado a la base trimérica, mientras que el dominio TAIL y su conector de cuatro hélices crean un segundo anclaje entre el nanocuerpo y el andamio. Las mediciones de la fuerza de unión mostraron que este anclaje doble mejoró la adhesión nanocuerpo–andamio en aproximadamente cuatro órdenes de magnitud, reduciendo considerablemente el movimiento no deseado que puede emborronar las imágenes de crio-EM. Los autores también analizaron muchas estructuras existentes de nanocuerpo–proteína para comprobar con qué frecuencia Trimbody se encontraría con choques estéricos—situaciones en las que el andamio chocaría con la propia proteína. Su sondeo sugiere que, para la mayoría de nanocuerpos y dianas, el sistema puede hacerse compatible ajustando un pequeño conjunto de residuos del armazón y probando la formación de complejos con ensayos bioquímicos estándar.
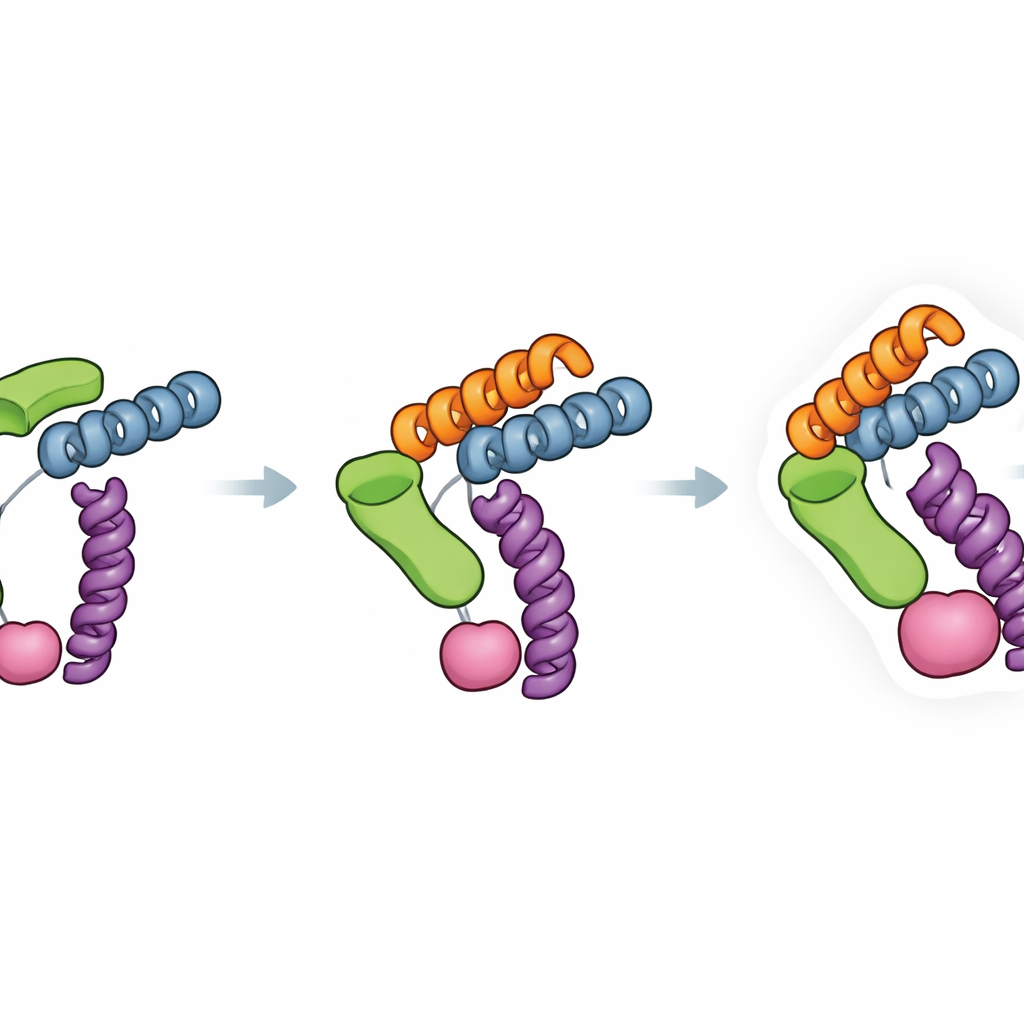
Abrir una ventana más clara sobre objetivos diminutos
En términos cotidianos, Trimbody actúa como un asa de precisión que permite a los microscopios “agarrar” y alinear proteínas muy pequeñas sin que vibren. Debido a que se basa en solo dos proteínas de fusión que son sencillas de producir en bacterias, el enfoque es tanto rentable como accesible para muchos laboratorios. Al convertir una amplia variedad de pares nanocuerpo–diana en complejos rígidos y compatibles con la crio-EM, Trimbody ofrece una vía general hacia vistas a nivel atómico de proteínas que antes eran demasiado pequeñas o elusivas para estudiar. Esta capacidad puede acelerar la comprensión de proteínas relacionadas con enfermedades y facilitar un desarrollo más rápido, guiado por la estructura, de fármacos y diagnósticos basados en nanocuerpos.
Cita: Song, J., Qi, L., Li, Y. et al. Trimbody with rigid AI-designed scaffolds enables atomic-resolution cryo-EM structure determination of small proteins. Nat Commun 17, 3135 (2026). https://doi.org/10.1038/s41467-026-69941-9
Palabras clave: microscopía crioelectrónica, andamios de nanocuerpos, estructura proteica, proteínas diseñadas por IA, pequeñas proteínas de membrana