Clear Sky Science · zh
衣壳抑制剂的理性设计及其体内验证:针对肠道病毒 D68
这对父母和医生意味着什么
每隔几年,一种鲜为人知的病原体——肠道病毒 D68 就会在社区中传播,主要感染儿童。对多数人来说,它的症状像是严重的感冒。但在极少数情况下,它会侵袭脊髓,使儿童出现突发的、类似小儿麻痹的无力甚至永久性瘫痪。目前尚无经批准的疫苗或抗病毒药物可用。该研究描述了科学家如何设计并测试两种实验性药物,它们阻断病毒的外壳、在小鼠中保护脊髓,并可能为将来应对这些可怕病例的治疗提供方向。
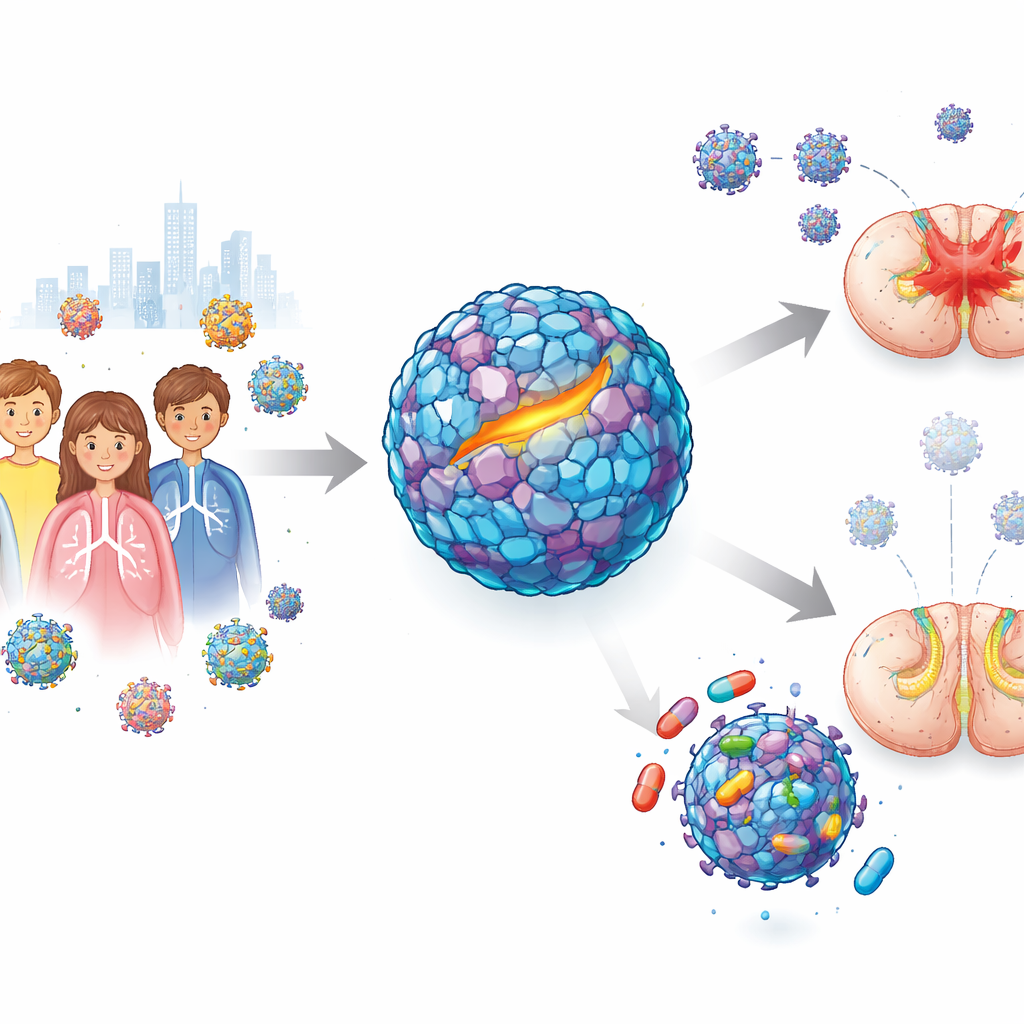
从轻微感冒到突发无力
肠道病毒 D68 通常通过咳嗽和打喷嚏传播,引起轻度呼吸道症状。然而在 2014 年的一次大规模暴发中,医生注意到一个令人不安的模式:一些感染的儿童出现急性弛缓性脊髓炎,表现为手臂或腿部迅速变得无力或松弛。研究显示,更新的病毒株比旧株更容易感染神经细胞,这引发了该病原体可能导致更广泛、更严重暴发的担忧。尽管多年来有许多努力,早期在试管中看起来有希望的药物在动物模型中未能发挥保护作用,尤其是在模拟神经系统疾病的模型中。这留下了一个紧迫的问题:当病毒已经开始攻击神经系统时,是否有药物能真正阻止它?
为病毒衣壳设计更好的“锁”
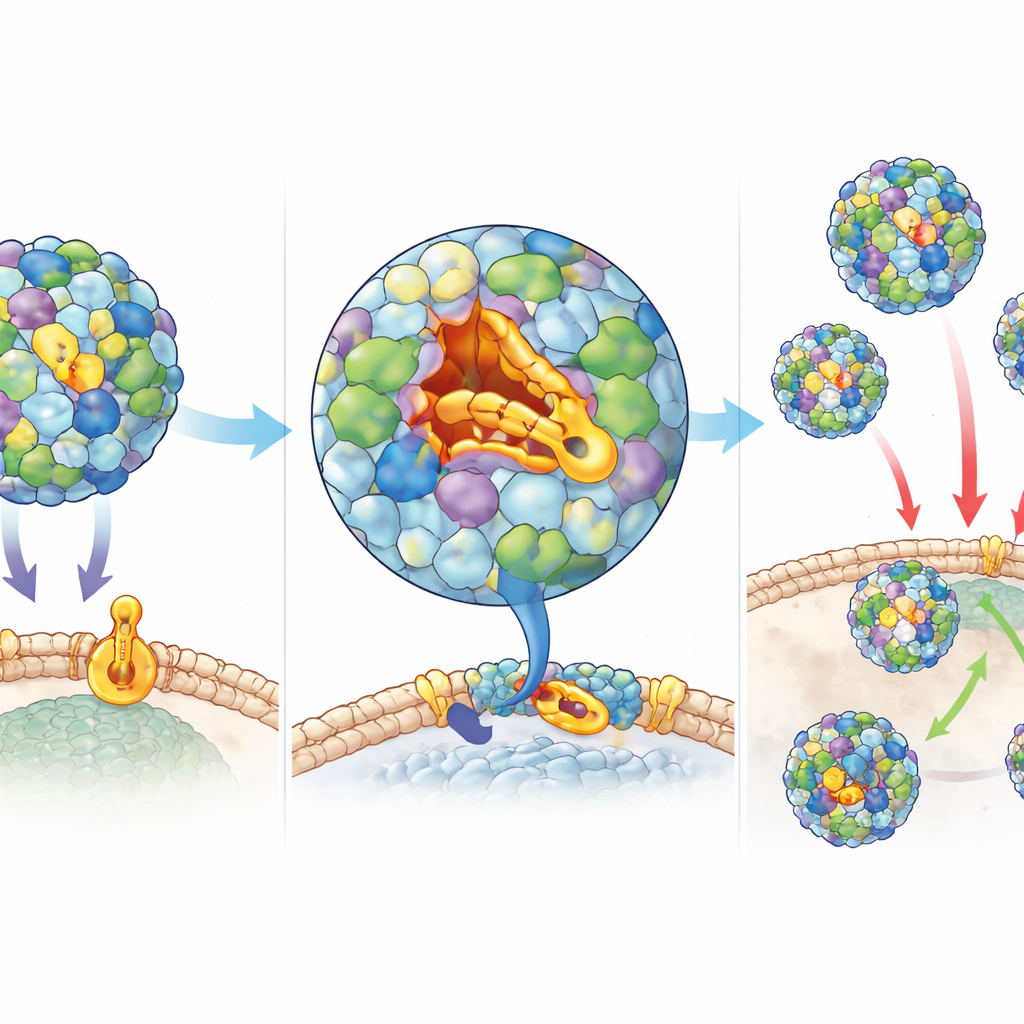
病毒被一层坚固的蛋白质外壳(即衣壳)包裹,保护其遗传物质并帮助附着到人体细胞。衣壳中的一种蛋白 VP1 包含一条狭窄的沟槽,被称为峡谷,该处通常容纳一个疏水分子,帮助保持衣壳稳定并为感染做好准备。此前的药物试图楔入该沟槽,但在动物体内效果不佳。在本研究中,研究人员使用计算机筛选数百万个候选分子,寻找可能紧密嵌入峡谷的化合物。随后通过药物化学对最佳命中项进行优化,调整分子形状和化学基团以更牢固地抓住所述口袋并在体内存留更久。该过程产生了两种突出化合物,命名为 Jun11695 和 Jun11787,它们在极低浓度下就能强力阻止病毒对细胞的破坏。
观察药物作用并绘制耐药图谱
研究团队利用高分辨率冷冻电子显微镜可视化了新化合物如何深嵌在病毒衣壳的峡谷口袋中,与周围的衣壳蛋白形成多处紧密接触。此类结合似乎将衣壳锁定在一种稳定构象,阻止病毒执行感染的早期步骤。时间添加实验证实,这些药物在病毒进入细胞之前或进入过程中最为有效,而在随后阶段无效,这与靶向衣壳的作用机制一致。当病毒在一种化合物 Jun11695 存在下反复培养时,出现了少量对药物敏感性降低的突变株。这些突变定位于与化合物接触的衣壳蛋白特定位置,既帮助确认了作用机制,也显示出耐药通常伴随病毒适应性方面的一定代价。
在小鼠模型中保护脊髓
关键问题是这些设计型化合物能否在活体动物中预防瘫痪。研究人员使用了一个成熟的小鼠模型:新生鼠在一条后肢肌肉中接种病毒,随后随着病毒向脊髓扩散并杀死运动神经元,出现进行性后肢无力。两种化合物在注射后都具有良好的吸收性,并在血液中维持数小时。当在感染后立即开始治疗时,每日给予 Jun11695 或 Jun11787 的小鼠均未出现瘫痪迹象,且体重增长超过未治疗的同窝小鼠。即便延迟 24 小时才开始给药或仅在出现首批明显的肢体无力迹象后才开始用药,这些药物仍显著降低了瘫痪评分,与对照组相比有明显改善。尤其是 Jun11787,能将肌肉和脊髓中的病毒水平降到检测下限以下,并保护脊髓内的运动神经元,使处理过的动物基本不出现无力。
对未来暴发的意义
对家庭和临床医生而言,主要信息既令人鼓舞又需谨慎解读。这些实验表明,有可能设计出小分子直接靶向病毒衣壳、到达神经系统并显著削弱甚至预防瘫痪——至少在小鼠身上是如此。Jun11695 和 Jun11787 是处于早期的候选先导,尚不可用于人类,且仍有重要难题需要克服,包括开发口服剂型和防范耐药性。然而,这项工作坚定地验证了病毒衣壳作为肠道病毒 D68 药物靶点的可行性,并为未来可能保护儿童免受这种罕见但毁灭性瘫痪的药物提供了具体蓝图。
引用: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
关键词: 肠道病毒 D68, 急性弛缓性脊髓炎, 抗病毒药物设计, 病毒衣壳抑制剂, 神经系统感染