Clear Sky Science · nl
Rationeel ontwerp en in vivo-validatie van capside-remmers voor enterovirus D68
Waarom dit belangrijk is voor ouders en artsen
Om de paar jaar verspreidt een weinig bekend micro-organisme, enterovirus D68, zich door gemeenschappen en besmet het vooral kinderen. Bij de meesten lijkt het op een zware verkoudheid. In zeldzame gevallen valt het echter het ruggenmerg aan, waardoor kinderen plotseling verzwakking krijgen die op polio lijkt of zelfs blijvende verlamming. Er is geen goedgekeurd vaccin of antiviraal middel tegen dit virus. Deze studie beschrijft hoe wetenschappers twee experimentele medicijnen hebben ontworpen en getest die de buitenste schaal van het virus blokkeren, het ruggenmerg beschermen bij muizen en mogelijk de weg wijzen naar toekomstige behandelingen voor deze angstaanjagende aandoeningen.
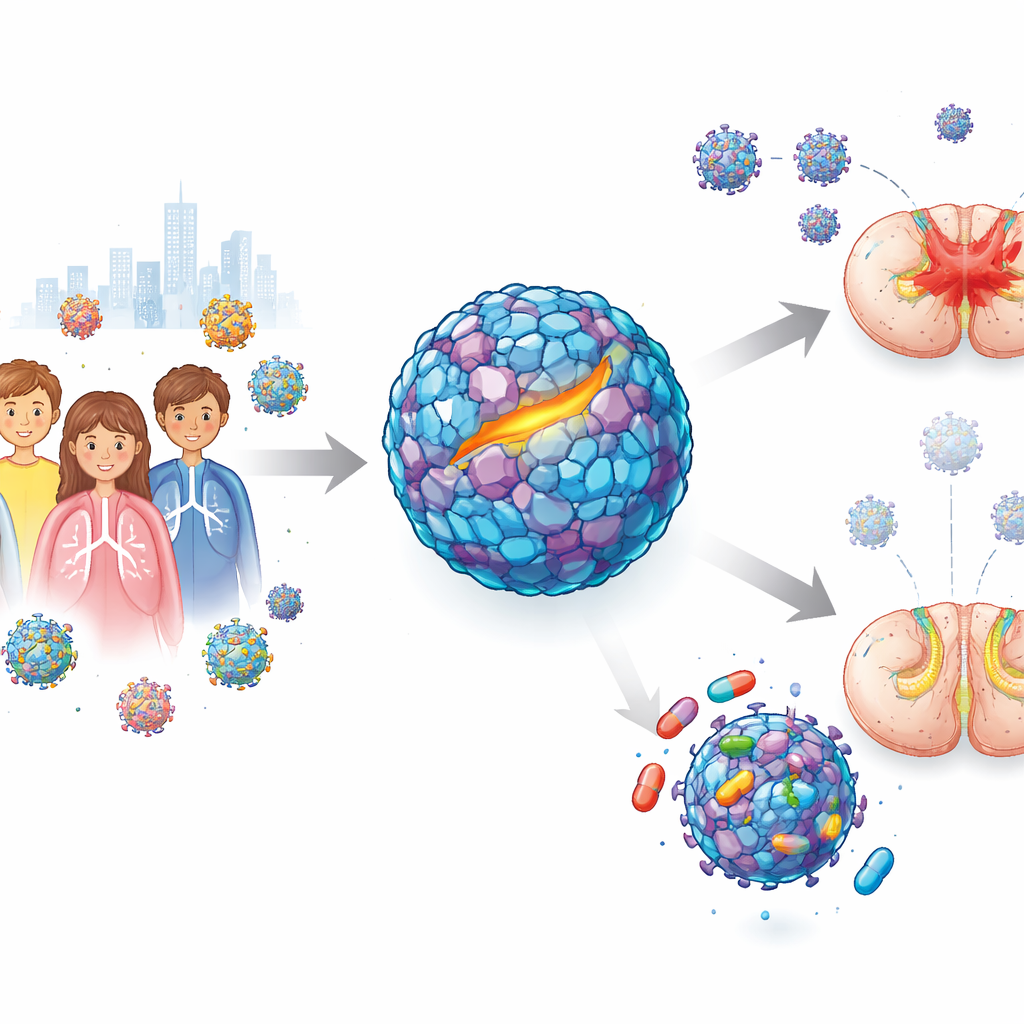
Van milde verkoudheden tot plotselinge verzwakking
Enterovirus D68 verspreidt zich meestal via hoesten en niezen en veroorzaakt milde luchtwegklachten. Tijdens een grote uitbraak in 2014 merkten artsen echter een verontrustend patroon: sommige geïnfecteerde kinderen ontwikkelden acute slappe myelitis, een aandoening waarbij armen of benen snel zwak of slap worden. Studies hebben aangetoond dat nieuwere stammen van het virus beter in staat zijn zenuwcellen te infecteren dan oudere stammen, wat de bezorgdheid vergroot dat dit pathogeen het potentieel heeft om grotere en ernstiger uitbraken te veroorzaken. Ondanks jarenlange inspanningen faalden eerdere kandidaat-geneesmiddelen die veelbelovend waren in reageerbuizen om dieren te beschermen, vooral in modellen die de neurologische ziekte nabootsen. Dat liet een dringende vraag over: kan een geneesmiddel het virus daadwerkelijk stoppen zodra het het zenuwstelsel begonnen is aan te vallen?
Een betere sluiting voor de virusmantel ontwerpen
Het virus is omhuld door een stevige eiwitmantel, of capsid, die zijn genetisch materiaal beschermt en helpt vasthechten aan menselijke cellen. Een van deze mantelproteïnen, VP1 genoemd, bevat een smalle groeve die bekendstaat als een canyon, waarin normaal gesproken een vettig molecuul zit dat de schaal stabiel houdt en klaar om cellen te infecteren. Eerdere geneesmiddelen probeerden zich in die groeve te klemmen, maar werkten niet goed genoeg in dieren. In deze studie gebruikten de onderzoekers computergebaseerde screening om miljoenen kandidaat-moleculen te doorzoeken op zoek naar stoffen die strak in de canyon zouden passen. Ze verfijnden de beste hits vervolgens met medicinale chemie, waarbij ze vormen en chemische groepen finetuneden om de pocket steviger vast te grijpen en langer in het lichaam te blijven. Dit proces leverde twee opvallende verbindingen op, Jun11695 en Jun11787, die het virus krachtig stopten met het beschadigen van cellen in kweek bij extreem lage concentraties.
Het middel in actie zien en resistentie in kaart brengen
Met behulp van hogeresolutie cryo-elektronenmicroscopie visualiseerde het team hoe de nieuwe verbindingen diep in de canyon-pocket op de virale mantel nestelen en veel nauwe contacten maken met de omringende capsid-eiwitten. Deze binding lijkt de mantel in een stabiele vorm te vergrendelen die verhindert dat het virus de vroege stappen van infectie uitvoert. Time-of-addition-experimenten bevestigden dat de middelen het meest effectief zijn wanneer ze aanwezig zijn vóór of tijdens de virale binnenkomst in cellen, maar niet later, wat consistent is met een capsid-gerichte werking. Toen het virus herhaaldelijk werd gekweekt in aanwezigheid van één verbinding, Jun11695, ontstonden zeldzame mutanten die minder gevoelig waren voor het middel. Deze mutaties waren gelokaliseerd op specifieke posities van de mantelproteïnen die het molecuul aanraken, wat de werking bevestigt maar ook laat zien dat resistentie gepaard gaat met enig verlies aan viraal fitness.
Het ruggenmerg beschermen in een muismodel
De cruciale vraag was of deze ontworpen verbindingen verlamming in levende dieren konden voorkomen. De onderzoekers gebruikten een goed vastgesteld muismodel waarbij pasgeboren jongen het virus in een beenspier krijgen en vervolgens progressieve zwakte van de achterpoten ontwikkelen naarmate het virus naar het ruggenmerg verspreidt en motorische neuronen doodt. Beide verbindingen werden na injectie goed opgenomen en bleven vele uren in de bloedbaan aanwezig. Wanneer de behandeling onmiddellijk na infectie begon, vertoonden muizen die dagelijks doses van Jun11695 of Jun11787 kregen geen tekenen van verlamming en kwamen ze meer aan in gewicht dan onbehandelde nestgenoten. Zelfs wanneer de toediening met 24 uur werd uitgesteld of pas begon nadat de eerste duidelijke tekenen van ledemaatzwakte waren verschenen, verminderden de middelen de verlammingsscores significant vergeleken met controles. Jun11787 verlaagde in het bijzonder de virusniveaus in zowel spier als ruggenmerg onder de detectielimiet en behield motorische neuronen in het ruggenmerg, waardoor behandelde dieren nagenoeg vrij van zwakte bleven.
Wat dit betekent voor toekomstige uitbraken
Voor gezinnen en clinici is de kernboodschap hoopvol maar terughoudend. Deze experimenten tonen aan dat het mogelijk is om kleine moleculen te ontwerpen die rechtstreeks de virusmantel targeten, het zenuwstelsel bereiken en verlamming betekenisvol afremmen of zelfs voorkomen — althans bij muizen. Jun11695 en Jun11787 zijn vroegtijdige kandidaatstoffen, niet klaar voor gebruik bij mensen, en belangrijke obstakels blijven bestaan, waaronder het testen van orale vormen en het voorkomen van resistentie. Toch valideert dit werk overtuigend de virale mantel als geneesmiddelendoelwit voor enterovirus D68 en biedt het een concreet stappenplan voor middelen die op een dag kinderen zouden kunnen beschermen tegen deze zeldzame maar verwoestende vorm van verlamming.
Bronvermelding: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Trefwoorden: enterovirus D68, acute slappe myelitis, ontwerp van antivirale middelen, virale capsideremmers, neurologische infectie