Clear Sky Science · de
Rationales Design und In-vivo-Validierung von Kapsidinhibitoren für Enterovirus D68
Warum das für Eltern und Ärztinnen wichtig ist
Alle paar Jahre breitet sich ein wenig bekanntes Keim namens Enterovirus D68 in Gemeinden aus und infiziert vor allem Kinder. Für die meisten ähnelt die Erkrankung einer starken Erkältung. In seltenen Fällen greift das Virus jedoch das Rückenmark an und hinterlässt bei Kindern plötzlich eine polioähnliche Schwäche oder sogar bleibende Lähmungen. Es gibt keinen zugelassenen Impfstoff oder antiviralen Wirkstoff gegen dieses Virus. In dieser Studie beschreiben Forschende, wie sie zwei experimentelle Wirkstoffe entwarfen und prüften, die die Außenhülle des Virus blockieren, das Rückenmark von Mäusen schützen und mögliche Wege zu künftigen Behandlungen für diese beängstigenden Krankheitsverläufe aufzeigen.
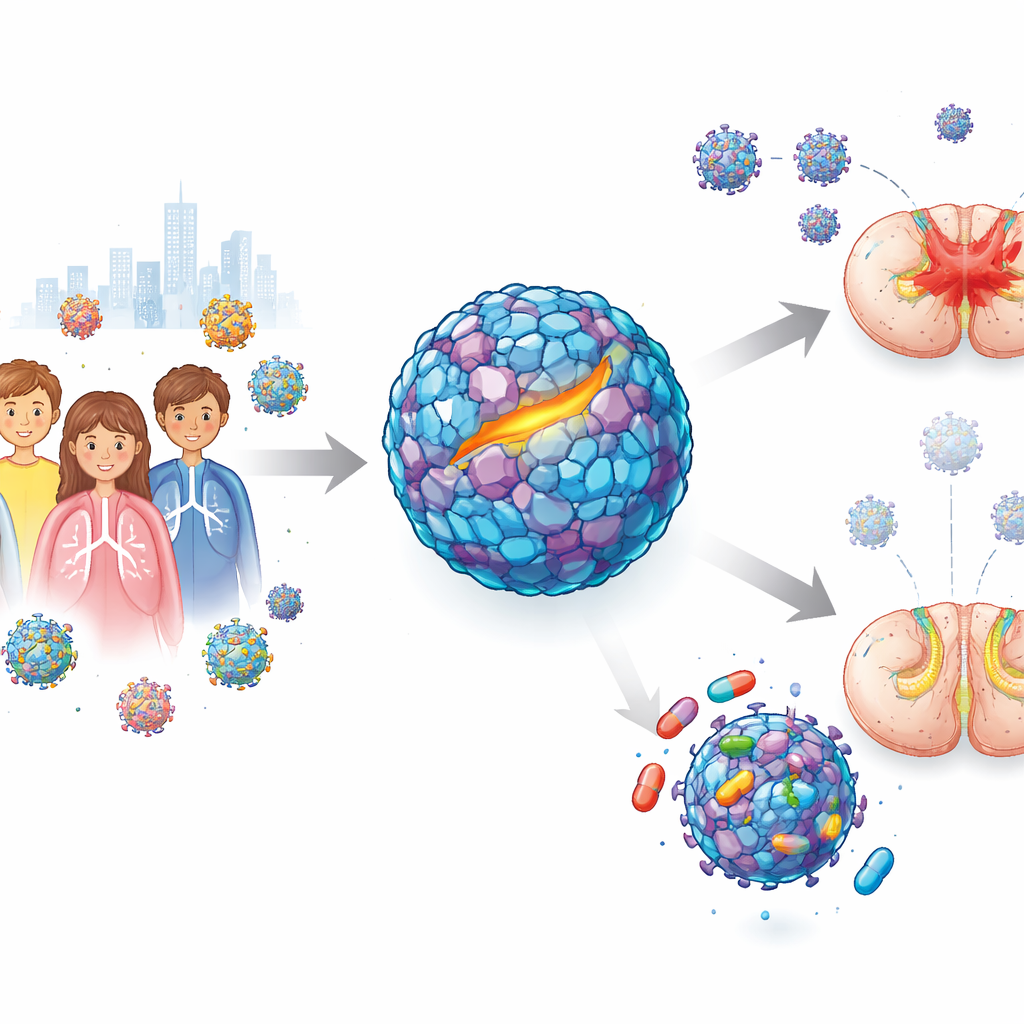
Von harmlosen Erkältungen zu plötzlicher Schwäche
Enterovirus D68 verbreitet sich meist durch Husten und Niesen und verursacht milde Atemwegsbeschwerden. Während eines großen Ausbruchs 2014 fiel Ärzten jedoch ein beunruhigendes Muster auf: Einige infizierte Kinder entwickelten eine akute schlaffe Myelitis, bei der Arme oder Beine schnell schwach oder schlaff werden. Studien zeigen, dass neuere Virusstämme Nervenzellen besser infizieren können als ältere, was die Sorge nährt, dass dieser Erreger das Potenzial für breitere und schwerere Ausbrüche hat. Trotz jahrelanger Bemühungen scheiterten frühere Wirkstoffkandidaten, die in Zellkulturen vielversprechend wirkten, daran, Tiere zu schützen — besonders in Modellen, die die neurologische Erkrankung nachahmen. Bleibt die drängende Frage: Kann ein Medikament das Virus tatsächlich stoppen, wenn es bereits das Nervensystem zu befällen beginnt?
Ein besseres Schloss für die Virushülle entwerfen
Das Virus ist von einer stabilen Proteinhülle, dem Kapsid, umgeben, die sein Erbgut schützt und ihm hilft, an menschliche Zellen anzudocken. Eines dieser Hüllproteine, VP1 genannt, enthält eine schmale Rinne — den sogenannten Canyon — die üblicherweise ein fettähnliches Molekül aufnimmt, welches die Hülle stabil hält und das Infektionsvermögen unterstützt. Frühere Wirkstoffe versuchten, sich in diese Rinne zu klemmen, waren in Tiermodellen jedoch nicht ausreichend wirksam. In dieser Studie nutzten die Forschenden computerbasierte Durchsuchungen, um Millionen Kandidatenmoleküle zu finden, die eng in den Canyon passen könnten. Anschließend verfeinerten sie die besten Treffer mittels medizinisch-chemischer Optimierung, passten Form und chemische Gruppen an, damit die Moleküle die Tasche fester greifen und im Körper länger bestehen. Dieser Prozess brachte zwei herausragende Verbindungen hervor, Jun11695 und Jun11787, die das Virus in Zellkulturen bereits in sehr niedrigen Konzentrationen kraftvoll am Schaden verhinderten.
Den Wirkstoff in Aktion sehen und Resistenzkartierung
Mithilfe hochauflösender Kryo-Elektronenmikroskopie visualisierte das Team, wie sich die neuen Verbindungen tief in die Canyon-Tasche der Virushülle einlagern und zahlreiche enge Kontakte zu den umgebenden Kapsidproteinen ausbilden. Diese Bindung scheint die Hülle in einer stabilen Form zu fixieren und verhindert so, dass das Virus die frühen Schritte der Infektion durchführt. Zeitpunkt-der-Zugabe-Experimente bestätigten, dass die Wirkstoffe am effektivsten sind, wenn sie vor oder während des Eindringens des Virus in Zellen vorhanden sind, nicht aber später — ein Befund, der zur kapsidgerichteten Wirkungsweise passt. Wurde das Virus wiederholt in Gegenwart eines Wirkstoffs, Jun11695, vermehrt, traten seltene Mutanten auf, die weniger empfindlich auf das Medikament reagierten. Diese Mutationen lagen an bestimmten Stellen der Hüllproteine, die Kontakt mit der Verbindung haben, was den Wirkmechanismus bestätigt und zugleich zeigt, dass Resistenz mit einem gewissen Fitnesskostengepäck für das Virus einhergeht.
Schutz des Rückenmarks in einem Mausmodell
Die entscheidende Frage war, ob diese maßgeschneiderten Verbindungen Lähmungen in lebenden Tieren verhindern können. Die Forschenden verwendeten ein etabliertes Mausmodell, in dem neugeborene Mäuse das Virus in einen Beinmuskel injiziert bekommen und dann fortschreitende Schwäche der Hinterbeine entwickeln, während das Virus ins Rückenmark wandert und Motoneuronen abtötet. Beide Verbindungen wurden nach Injektion gut aufgenommen und blieben viele Stunden im Blut. Wenn die Behandlung sofort nach der Infektion begonnen wurde, zeigten Mäuse, die täglich Dosen von Jun11695 oder Jun11787 erhielten, keinerlei Anzeichen von Lähmung und nahmen mehr Gewicht zu als unbehandelte Wurfgeschwister. Selbst wenn die Gabe um 24 Stunden verzögert wurde oder erst nach den ersten deutlichen Anzeichen von Gliedmaßenschwäche startete, verringerten die Wirkstoffe die Lähmungsscores gegenüber Kontrollen deutlich. Jun11787 senkte insbesondere die Viruslast in Muskel und Rückenmark unter die Nachweisgrenze und bewahrte Motoneuronen im Rückenmark, sodass behandelte Tiere im Wesentlichen frei von Schwäche blieben.
Was das für künftige Ausbrüche bedeutet
Für Familien und Kliniker lautet die Kernbotschaft hoffnungsvoll, aber vorsichtig. Diese Experimente zeigen, dass es möglich ist, kleine Moleküle zu entwerfen, die gezielt die Virushülle angreifen, das Nervensystem erreichen und Lähmungen deutlich abschwächen oder sogar verhindern — zumindest bei Mäusen. Jun11695 und Jun11787 sind frühe Leitverbindungen, noch nicht für den Gebrauch beim Menschen geeignet, und es bleiben wichtige Hürden, etwa die Prüfung oraler Formulierungen und der Schutz vor Resistenzentwicklung. Dennoch validiert die Arbeit eindrücklich das Kapsid als Arzneimittelziel für Enterovirus D68 und liefert einen konkreten Bauplan für Wirkstoffe, die eines Tages Kinder vor dieser seltenen, aber verheerenden Form der Lähmung schützen könnten.
Zitation: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Schlüsselwörter: enterovirus D68, akute schlaffe Myelitis, Design antiviraler Wirkstoffe, virale Kapsid-Inhibitoren, neurologische Infektion