Clear Sky Science · pt
Projeto racional e validação in vivo de inibidores de capsídeo para enterovírus D68
Por que isso importa para pais e médicos
De alguns em alguns anos, um microrganismo pouco conhecido chamado enterovírus D68 varre comunidades, infectando principalmente crianças. Para a maioria, parece um resfriado forte. Mas, em casos raros, ele ataca a medula espinhal, deixando crianças com fraqueza súbita semelhante à pólio ou até paralisia permanente. Não existe vacina aprovada nem medicamento antiviral para esse vírus. Este estudo descreve como cientistas projetaram e testaram duas drogas experimentais que bloqueiam a camada externa do vírus, protegem a medula espinhal em camundongos e podem indicar um caminho para tratamentos futuros desses episódios assustadores.
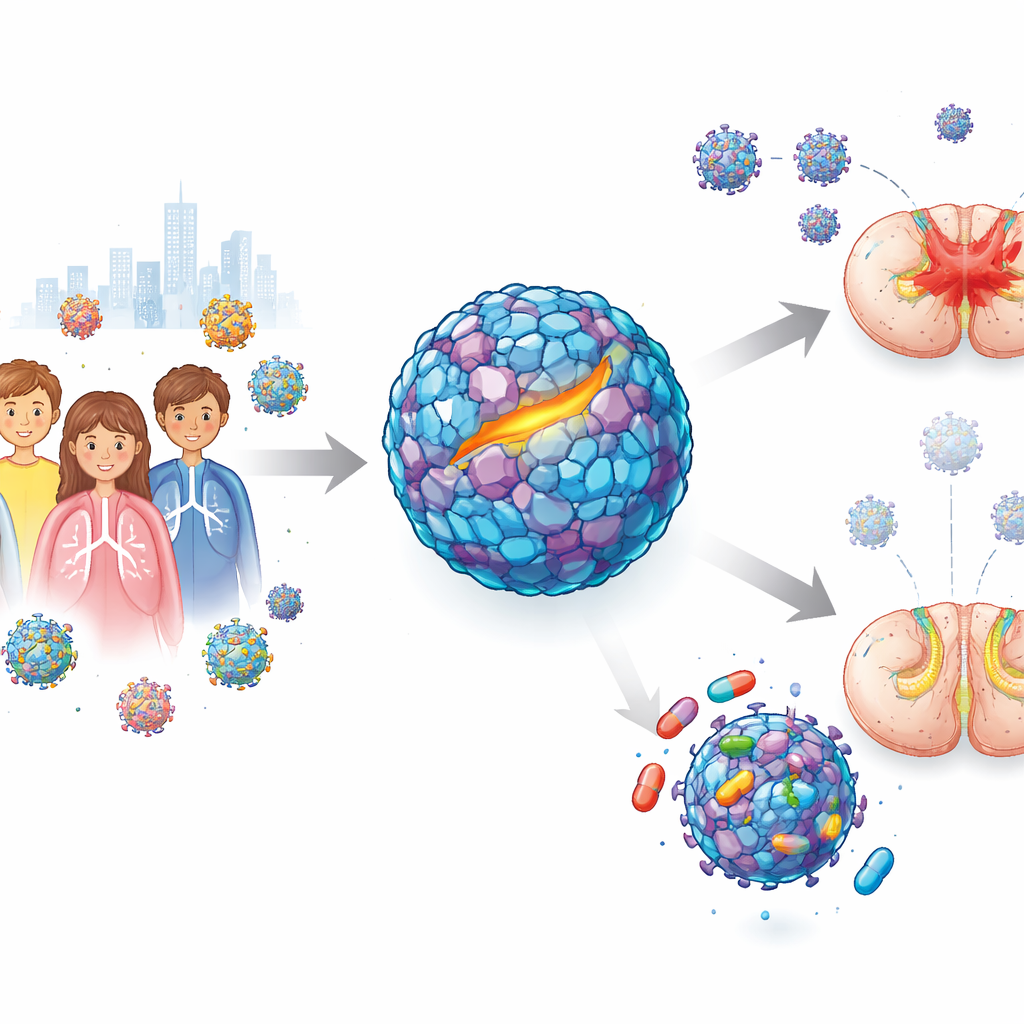
De resfriados leves à fraqueza súbita
O enterovírus D68 costuma se espalhar por tosse e espirro e causa sintomas respiratórios leves. Durante um grande surto em 2014, porém, os médicos notaram um padrão preocupante: algumas crianças infectadas desenvolveram mielite flácida aguda, uma condição em que braços ou pernas ficam rapidamente fracos ou flácidos. Estudos mostraram que cepas mais recentes do vírus conseguem infectar células nervosas melhor do que as mais antigas, aumentando a preocupação de que esse patógeno possa causar surtos mais amplos e graves. Apesar de anos de esforço, candidatos a medicamentos anteriores que pareciam promissores em placas de laboratório não protegeram animais, especialmente em modelos que imitam a doença neurológica. Isso deixou uma lacuna urgente: um medicamento pode realmente deter esse vírus depois que ele já começou a atacar o sistema nervoso?
Projetando uma trava melhor para a casca do vírus
O vírus é envolvido por uma casca proteica resistente, ou capsídeo, que protege seu material genético e ajuda a se ligar às células humanas. Uma dessas proteínas do capsídeo, chamada VP1, contém um sulco estreito conhecido como cânion, que normalmente abriga uma molécula oleosa que ajuda a manter a casca estável e pronta para infectar células. Drogas anteriores tentaram se enfiar nesse sulco, mas não funcionaram bem o suficiente em animais. Neste estudo, os pesquisadores usaram triagem por computador para vasculhar milhões de moléculas candidatas em busca daquelas que pudessem se encaixar firmemente no cânion. Em seguida, refinaram os melhores achados por meio da química medicinal, ajustando formas e grupos químicos para agarrar o bolso com mais força e sobreviver mais tempo no corpo. Esse processo gerou dois compostos de destaque, chamados Jun11695 e Jun11787, que bloquearam poderosamente o dano viral às células em cultura em concentrações extremamente baixas.
Vendo a droga em ação e mapeando resistência
Usando criomicroscopia eletrônica de alta resolução, a equipe visualizou como os novos compostos se acomodam profundamente dentro do bolso do cânion no capsídeo viral, fazendo muitos contatos justos com proteínas do capsídeo ao redor. Essa ligação parece bloquear a casca em uma forma estável que impede o vírus de realizar os passos iniciais da infecção. Experimentos de tempo de adição confirmaram que as drogas são mais eficazes quando presentes antes ou durante a entrada do vírus nas células, mas não depois, consistente com uma ação direcionada ao capsídeo. Quando o vírus foi repetidamente cultivado na presença de um dos compostos, Jun11695, surgiram mutantes raros menos sensíveis à droga. Essas mutações se mapearam em posições específicas das proteínas do capsídeo que tocam o composto, ajudando a confirmar o mecanismo e mostrando também que a resistência vem com algum custo para a aptidão viral.
Protegendo a medula espinhal em um modelo de camundongo
A pergunta crucial era se esses compostos projetados poderiam prevenir a paralisia em animais vivos. Os pesquisadores usaram um modelo de camundongo bem estabelecido no qual filhotes recém-nascidos recebem o vírus em um músculo da perna e então desenvolvem fraqueza progressiva nos membros posteriores à medida que o vírus se espalha para a medula espinhal e mata motoneurônios. Ambos os compostos foram bem absorvidos após injeção e permaneceram na corrente sanguínea por muitas horas. Quando o tratamento começou imediatamente após a infecção, camundongos que receberam doses diárias de Jun11695 ou Jun11787 não mostraram sinais de paralisia e ganharam mais peso do que irmãos não tratados. Mesmo quando a dosagem foi atrasada em 24 horas ou iniciada apenas após os primeiros sinais claros de fraqueza nos membros, os medicamentos reduziram significativamente as pontuações de paralisia em comparação com controles. Jun11787, em particular, abaixou os níveis do vírus tanto no músculo quanto na medula espinhal abaixo do limite de detecção e preservou motoneurônios na medula espinhal, deixando os animais tratados essencialmente sem fraqueza.
O que isso significa para futuros surtos
Para famílias e clínicos, a mensagem principal é esperançosa, mas cautelosa. Esses experimentos mostram que é possível projetar pequenas moléculas que miram diretamente o capsídeo viral, alcançam o sistema nervoso e atenuam ou até previnem de forma significativa a paralisia — pelo menos em camundongos. Jun11695 e Jun11787 são candidatos em estágio inicial, não prontos para uso humano, e permanecem obstáculos importantes, incluindo testar formulações orais e se proteger contra resistência. Ainda assim, o trabalho valida firmemente o capsídeo viral como um alvo farmacológico para o enterovírus D68 e oferece um roteiro concreto para medicamentos que, um dia, podem proteger crianças diante dessa forma rara, porém devastadora, de paralisia.
Citação: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Palavras-chave: enterovírus D68, mielite flácida aguda, projeto de antivirais, inibidores do capsídeo viral, infecção neurológica