Clear Sky Science · pl
Racjonalne projektowanie i walidacja in vivo inhibitorów kapsydu dla enterowirusa D68
Dlaczego to ma znaczenie dla rodziców i lekarzy
Co kilka lat mało znany drobnoustrój zwany enterowirusem D68 rozprzestrzenia się w społecznościach, głównie zakażając dzieci. U większości przebiega jak cięższe przeziębienie. Jednak w rzadkich przypadkach atakuje rdzeń kręgowy, pozostawiając dzieci z nagłą, polio-podobną słabością, a nawet trwałym paraliżem. Nie ma zatwierdzonej szczepionki ani leku przeciwwirusowego przeciwko temu wirusowi. W tym badaniu naukowcy opisują, jak zaprojektowali i przetestowali dwa eksperymentalne leki, które blokują zewnętrzną powłokę wirusa, chronią rdzeń kręgowy u myszy i mogą wskazywać drogę do przyszłych terapii tych przerażających epizodów.
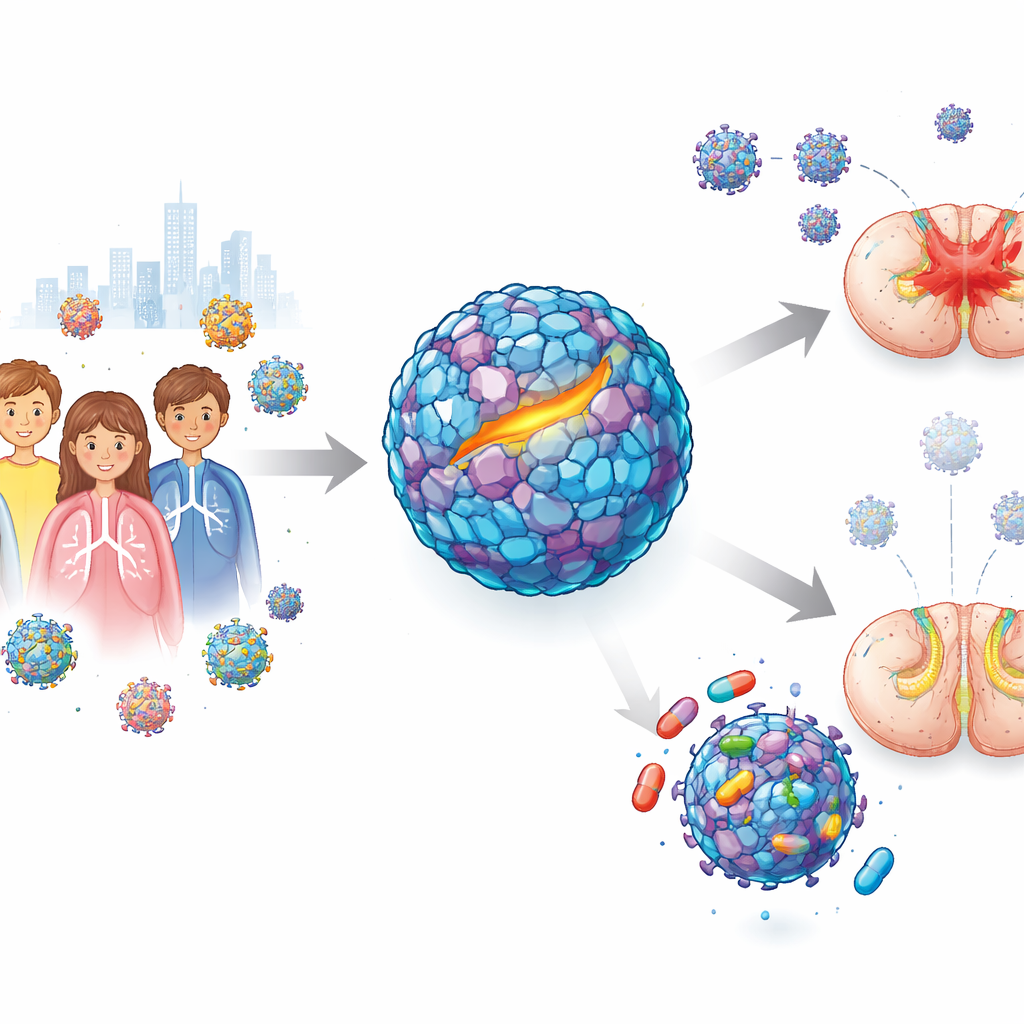
Od łagodnych przeziębień do nagłej słabości
Enterowirus D68 zwykle rozprzestrzenia się przez kaszel i kichanie i powoduje łagodne problemy z oddychaniem. Podczas dużego ogniska w 2014 r. lekarze jednak zauważyli niepokojący wzorzec: niektóre zakażone dzieci rozwijały ostre wiotkie zapalenie rdzenia, stan, w którym ramiona lub nogi szybko stawały się słabe lub wiotkie. Badania wykazały, że nowsze szczepy wirusa lepiej zakażają komórki nerwowe niż starsze, co budzi obawy, że patogen ten ma potencjał wywoływania szerszych i cięższych ognisk. Pomimo wieloletnich wysiłków wcześniejsze kandydaty na leki, które wyglądały obiecująco w hodowlach komórkowych, nie chroniły zwierząt, zwłaszcza w modelach odzwierciedlających chorobę neurologiczną. Pozostawiło to pilną lukę: czy lek faktycznie może zatrzymać wirusa, gdy ten już zaczął atakować układ nerwowy?
Projektowanie lepszego zamka dla powłoki wirusa
Wirus jest otoczony wytrzymałą białkową powłoką, czyli kapsydem, która chroni materiał genetyczny i pomaga przyczepiać się do komórek człowieka. Jeden z białkowych elementów tej powłoki, zwany VP1, zawiera wąską szczelinę zwaną kanionem, która normalnie mieści tłustą cząsteczkę pomagającą utrzymać powłokę w stabilnej, gotowej do zakażenia formie. Wcześniejsze leki próbowały klinować się w tym kanionie, ale nie działały wystarczająco dobrze u zwierząt. W tym badaniu badacze wykorzystali komputerowe przesiewy, aby przeszukać miliony kandydatów i znaleźć te, które mogą ciasno pasować do kanionu. Następnie udoskonalili najlepsze trafienia za pomocą chemii medycznej, dopasowując kształty i grupy chemiczne, by mocniej chwycić kieszeń i przetrwać dłużej w organizmie. Ten proces dał dwa wyróżniające się związki, nazwane Jun11695 i Jun11787, które gwałtownie zatrzymywały wirusa przed uszkadzaniem komórek w hodowlach przy niezwykle niskich stężeniach.
Obserwowanie leku w działaniu i mapowanie oporności
Przy użyciu wysokorozdzielczej krioelektronowej mikroskopii zespół zobrazował, jak nowe związki umieszczają się głęboko wewnątrz kieszeni kanionu na powłoce wirusa, nawiązując liczne ciasne kontakty z otaczającymi białkami kapsydu. To wiązanie wydaje się blokować powłokę w stabilnej formie, uniemożliwiając wirusowi wykonanie wczesnych etapów zakażenia. Eksperymenty z czasem dodania potwierdziły, że leki są najskuteczniejsze, gdy obecne są przed lub w trakcie wejścia wirusa do komórek, ale nie później, co jest zgodne z mechanizmem ukierunkowanym na kapsyd. Gdy wirusa wielokrotnie hodowano w obecności jednego ze związków, Jun11695, pojawiły się rzadkie mutacje mniej wrażliwe na lek. Mutacje te zlokalizowano w konkretnych pozycjach białek powłoki stykających się ze związkiem, co pomogło potwierdzić mechanizm, a jednocześnie pokazało, że oporność wiąże się z pewnym kosztem dla sprawności wirusa.
Ochrona rdzenia kręgowego w modelu myszy
Kluczowe pytanie brzmiało, czy te zaprojektowane związki mogą zapobiec paraliżowi u żywych zwierząt. Badacze użyli dobrze ugruntowanego modelu myszy, w którym nowo narodzone myszę otrzymują wirusa w mięsień nogi, a następnie rozwija się postępujące osłabienie tylnych kończyn, gdy wirus rozprzestrzenia się do rdzenia kręgowego i zabija neurony ruchowe. Oba związki były dobrze wchłaniane po wstrzyknięciu i utrzymywały się we krwi przez wiele godzin. Gdy leczenie rozpoczęto natychmiast po zakażeniu, myszy otrzymujące codzienne dawki Jun11695 lub Jun11787 nie wykazywały oznak paraliżu i przybierały na wadze bardziej niż nieleczone rodzeństwo. Nawet gdy dawkowanie opóźniono o 24 godziny lub rozpoczęto dopiero po pojawieniu się pierwszych wyraźnych oznak osłabienia kończyn, leki znacząco obniżały wyniki paraliżu w porównaniu z kontrolami. Jun11787, w szczególności, obniżył poziomy wirusa w mięśniach i rdzeniu kręgowym poniżej granicy wykrywalności i zachował neurony ruchowe w rdzeniu, pozostawiając leczone zwierzęta praktycznie bez słabości.
Co to oznacza na przyszłość w razie ognisk
Dla rodzin i klinicystów kluczowy przekaz jest pełen nadziei, ale ostrożny. Te eksperymenty pokazują, że możliwe jest zaprojektowanie małych cząsteczek, które bezpośrednio celują w powłokę wirusa, docierają do układu nerwowego i istotnie łagodzą lub nawet zapobiegają paraliżowi — przynajmniej u myszy. Jun11695 i Jun11787 to wczesne kandydaty, niegotowe do użycia u ludzi, i pozostaje wiele przeszkód, w tym testy form doustnych i zabezpieczenie przed narastającą opornością. Mimo to praca solidnie potwierdza kapsyd wirusa jako cel lekowy dla enterowirusa D68 i oferuje konkretne wskazówki do opracowania leków, które pewnego dnia mogą chronić dzieci przed tą rzadką, lecz druzgocącą formą paraliżu.
Cytowanie: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Słowa kluczowe: enterowirus D68, ostre wiotkie zapalenie rdzenia, projektowanie leków przeciwwirusowych, viral capsid inhibitors</keyword-inhibitory kapsydu wirusa> <keyword>zakażenie neurologiczne