Clear Sky Science · fr
Conception rationnelle et validation in vivo d’inhibiteurs de la capside pour l’entérovirus D68
Pourquoi c’est important pour les parents et les médecins
Tous les quelques années, un microbe peu connu appelé entérovirus D68 se propage dans les communautés, infectant principalement les enfants. Pour la plupart, cela ressemble à un gros rhume. Mais, dans de rares cas, il attaque la moelle épinière, laissant des enfants avec une faiblesse soudaine de type polio ou même une paralysie permanente. Il n’existe aucun vaccin ni antiviral approuvé contre ce virus. Cette étude décrit comment des scientifiques ont conçu et testé deux médicaments expérimentaux qui bloquent l’enveloppe virale, protègent la moelle épinière chez la souris et peuvent indiquer une voie vers de futurs traitements pour ces épisodes inquiétants.
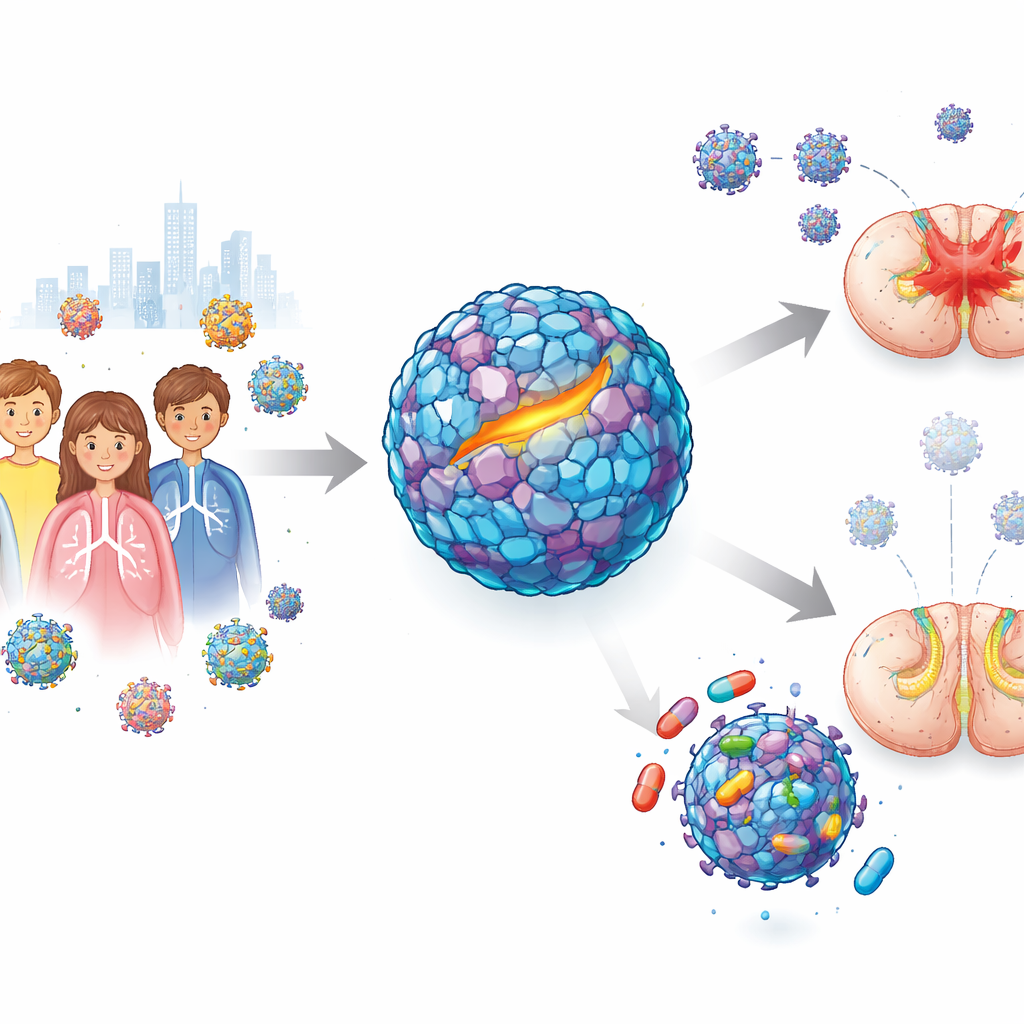
Des rhumes bénins à la faiblesse soudaine
L’entérovirus D68 se transmet habituellement par la toux et les éternuements et provoque des troubles respiratoires légers. Lors d’une large épidémie en 2014, cependant, les médecins ont remarqué un schéma inquiétant : certains enfants infectés ont développé une myélite flasque aiguë, une affection où les bras ou les jambes deviennent rapidement faibles ou flasques. Des études ont montré que des souches plus récentes du virus infectent mieux les cellules nerveuses que les anciennes, ce qui fait craindre que cet agent pathogène puisse provoquer des flambées plus vastes et plus sévères. Malgré des années d’efforts, des candidats médicaments antérieurs prometteurs en laboratoire n’ont pas protégé les animaux, en particulier dans des modèles reproduisant la maladie neurologique. Il restait donc une question urgente : un médicament peut‑il réellement arrêter ce virus une fois qu’il a commencé à attaquer le système nerveux ?
Concevoir une meilleure serrure pour la coque virale
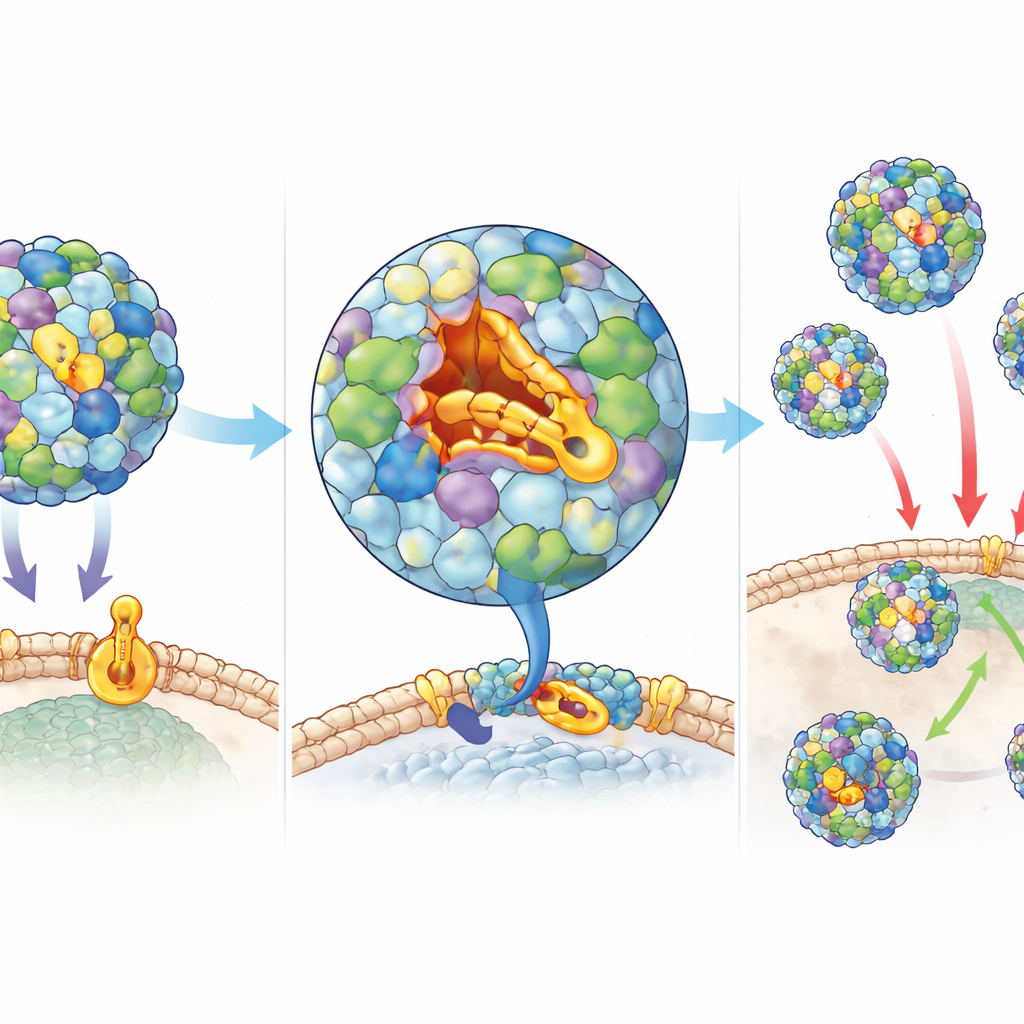
Le virus est enveloppé d’une coque protéique robuste, ou capside, qui protège son matériel génétique et l’aide à s’attacher aux cellules humaines. L’une de ces protéines de la coque, appelée VP1, contient une étroite gouttière connue sous le nom de canyon, qui contient normalement une molécule grasse aidant à stabiliser la capside et à la maintenir prête à infecter les cellules. Les médicaments précédents ont tenté de s’insérer dans cette gouttière mais n’ont pas suffisamment fonctionné chez l’animal. Dans cette étude, les chercheurs ont utilisé un criblage par ordinateur pour rechercher des millions de molécules candidates susceptibles de s’emboîter étroitement dans le canyon. Ils ont ensuite affiné les meilleurs candidats par chimie médicamenteuse, ajustant leurs formes et groupes chimiques pour mieux s’accrocher à la poche et persister plus longtemps dans l’organisme. Ce processus a donné deux composés remarquables, baptisés Jun11695 et Jun11787, qui ont puissamment empêché le virus d’endommager les cellules en culture à des concentrations extrêmement faibles.
Voir le médicament à l’œuvre et cartographier la résistance
À l’aide de la cryo‑microscopie électronique à haute résolution, l’équipe a visualisé comment les nouveaux composés s’insèrent profondément dans la poche du canyon de la capside, établissant de nombreux contacts étroits avec les protéines environnantes. Ce liaison semble verrouiller la capside dans une forme stable qui empêche le virus d’accomplir les premières étapes de l’infection. Des expériences de temps d’ajout ont confirmé que les médicaments sont plus efficaces lorsqu’ils sont présents avant ou pendant l’entrée du virus dans les cellules, mais pas après, ce qui est cohérent avec une action ciblant la capside. Lorsque le virus a été cultivé à plusieurs reprises en présence de l’un des composés, Jun11695, des mutants rares moins sensibles au médicament sont apparus. Ces mutations se sont situées à des positions spécifiques des protéines de la capside en contact avec le composé, contribuant à confirmer le mécanisme tout en montrant que la résistance s’accompagne d’un certain coût pour la fitness virale.
Protection de la moelle épinière dans un modèle murin
La question cruciale était de savoir si ces composés conçus pouvaient prévenir la paralysie chez des animaux vivants. Les chercheurs ont utilisé un modèle murin bien établi dans lequel des souriceaux nouveau‑nés reçoivent le virus dans un muscle de la patte puis développent une faiblesse progressive des membres postérieurs à mesure que le virus se propage vers la moelle épinière et tue les neurones moteurs. Les deux composés ont été bien absorbés après injection et sont restés dans le sang pendant de nombreuses heures. Lorsque le traitement a commencé immédiatement après l’infection, les souris recevant des doses quotidiennes de Jun11695 ou Jun11787 n’ont présenté aucun signe de paralysie et ont pris plus de poids que leurs congénères non traités. Même lorsque l’administration a été retardée de 24 heures ou commencée seulement après les premiers signes nets de faiblesse des membres, les médicaments ont significativement réduit les scores de paralysie par rapport aux témoins. Jun11787, en particulier, a abaissé les niveaux viraux dans le muscle et la moelle épinière en dessous du seuil de détection et a préservé les neurones moteurs dans la moelle, laissant les animaux traités essentiellement exempts de faiblesse.
Que cela signifie pour de futures épidémies
Pour les familles et les cliniciens, le message principal est porteur d’espoir mais prudent. Ces expériences montrent qu’il est possible de concevoir de petites molécules ciblant directement la capside virale, atteignant le système nerveux et atténuant de manière significative, voire empêchant, la paralysie — du moins chez la souris. Jun11695 et Jun11787 sont des pistes en phase précoce, pas prêtes pour l’usage humain, et d’importants obstacles subsistent, notamment la mise au point de formes orales et la prévention de l’émergence de résistances. Néanmoins, ce travail valide fermement la capside virale comme cible thérapeutique pour l’entérovirus D68 et fournit une feuille de route concrète pour des médicaments qui pourraient un jour protéger les enfants confrontés à cette forme rare mais dévastatrice de paralysie.
Citation: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Mots-clés: entérovirus D68, myélite flasque aiguë, conception d’antiviraux, inhibiteurs de la capside virale, infection neurologique