Clear Sky Science · sv
Rationell design och in vivo-validering av kapsidhämmare för enterovirus D68
Varför detta är viktigt för föräldrar och läkare
Varje par år sveper en relativt okänd mikroorganism, enterovirus D68, genom samhällen och smittar främst barn. För de flesta liknar det en kraftig förkylning. Men i sällsynta fall angriper det ryggmärgen och lämnar barn med plötslig, polio-liknande svaghet eller till och med bestående förlamning. Det finns varken ett godkänt vaccin eller antiviralt läkemedel mot detta virus. Denna studie beskriver hur forskare tog fram och testade två experimentella läkemedel som blockerar virusets yttre skal, skyddar ryggmärgen hos möss och kan peka ut en väg framåt för framtida behandlingar av dessa skrämmande episoder.
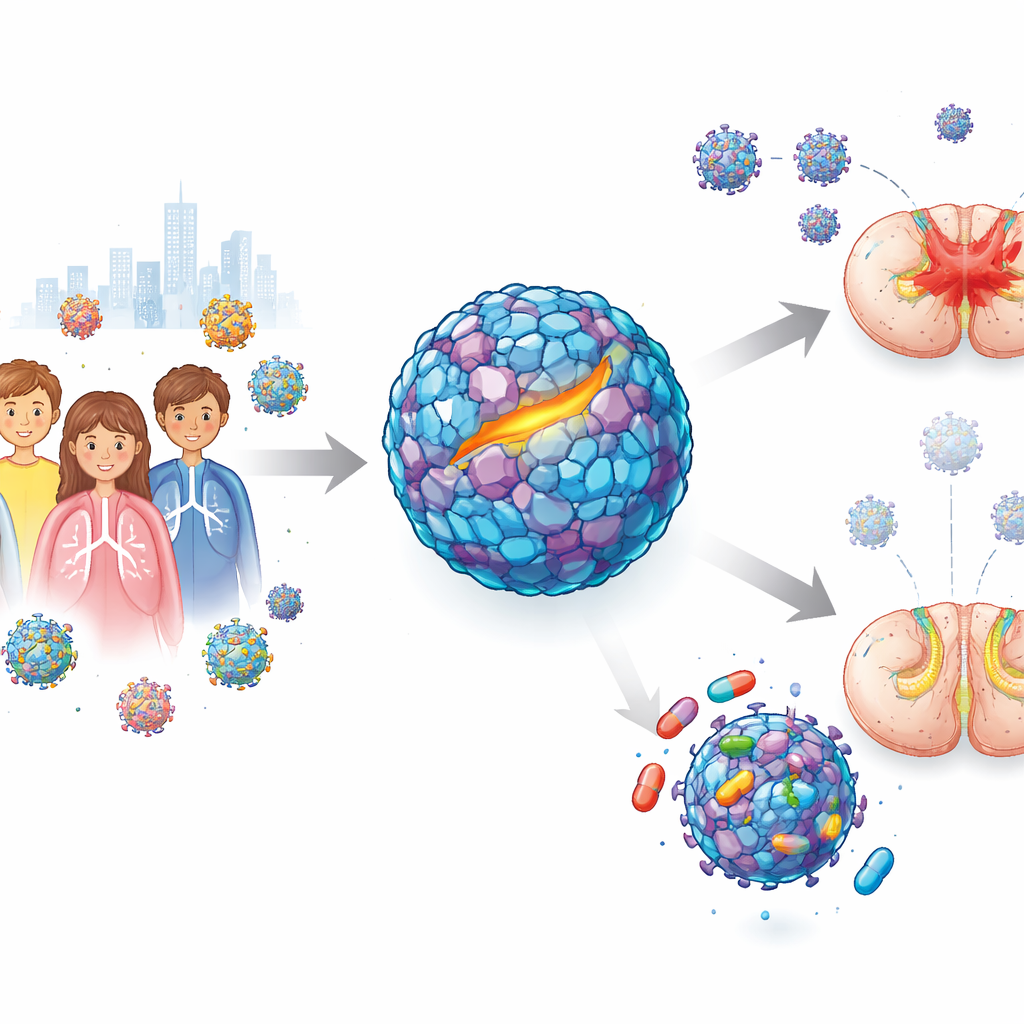
Från milda förkylningar till plötslig svaghet
Enterovirus D68 sprids vanligen via hosta och nysningar och orsakar milda andningsbesvär. Vid ett stort utbrott 2014 lade dock läkare märke till ett oroväckande mönster: vissa infekterade barn utvecklade akut slapp myelit, ett tillstånd där armar eller ben snabbt blir svaga eller slappa. Studier har visat att nyare stammar av viruset har större förmåga att infektera nervceller än äldre varianter, vilket väcker oro för att denna patogen kan orsaka bredare och allvarligare utbrott. Trots år av arbete misslyckades tidigare läkemedelskandidater som såg lovande ut i provrör med att skydda djur, särskilt i modeller som efterliknar den neurologiska sjukdomen. Det lämnade ett akut gap: kan ett läkemedel verkligen stoppa detta virus när det väl börjat angripa nervsystemet?
Att designa ett bättre lås för virusskalet
Viruset är omslutet av ett robust proteinskal, eller kapsid, som skyddar dess genetiska material och hjälper det att fästa vid mänskliga celler. Ett av dessa skalproteiner, kallat VP1, innehåller en smal fåra känd som en canyon, som normalt rymmer en fettlik molekyl som hjälper till att hålla skalet stabilt och redo att infektera celler. Tidigare läkemedel försökte kilas in i denna fåra men fungerade inte tillräckligt bra i djur. I denna studie använde forskarna datorbaserad screening för att söka bland miljontals kandidatmolekyler efter sådana som skulle kunna passa tätt i canyongrottan. De förfinade sedan de bästa träffarna med läkemedelskemi, genom att justera former och kemiska grupper för att greppa fickan mer bestämt och överleva längre i kroppen. Denna process gav två framstående föreningar, benämnda Jun11695 och Jun11787, som kraftfullt förhindrade att viruset skadade celler i odling vid extremt låga koncentrationer.
Att se läkemedlet i arbete och kartlägga resistens
Med hjälp av högupplöst kryoelektronmikroskopi visualiserade teamet hur de nya föreningarna lägger sig djupt inne i canyonfickan på virusskalet och gör många täta kontakter med omgivande kapsidproteiner. Denna bindning verkar låsa skalet i en stabil form som hindrar viruset från att genomföra de tidiga stegen i infektionen. Tidsförloppsexperiment bekräftade att läkemedlen är mest effektiva när de finns närvarande före eller under virusets inträde i celler, men inte senare, vilket är förenligt med en kapsidriktad verkan. När viruset upprepade gånger odlades i närvaro av en av föreningarna, Jun11695, uppstod sällsynta mutanter som var mindre känsliga för läkemedlet. Dessa mutationer kartlades till specifika positioner på skalproteinerna som rör vid föreningen, vilket hjälper till att bekräfta verkningsmekanismen samtidigt som det visar att resistens medför en viss kostnad för virusets fitness.
Att skydda ryggmärgen i en musmodell
Den avgörande frågan var om dessa designade föreningar kunde förhindra förlamning i levande djur. Forskarna använde en väletablerad musmodell där nyfödda ungar får viruset i en benmuskel och sedan utvecklar progressiv svaghet i bakbenen när viruset sprider sig till ryggmärgen och dödar motorneuroner. Båda föreningarna absorberades väl efter injektion och stannade kvar i blodomloppet i många timmar. När behandling påbörjades omedelbart efter infektion visade möss som fick dagliga doser av antingen Jun11695 eller Jun11787 inga tecken på förlamning och gick upp mer i vikt än obehandlade kullsyskon. Även när doseringen fördröjdes med 24 timmar eller startade först efter de första tydliga tecknen på lemsvaghet, minskade läkemedlen förlamningspoängen avsevärt jämfört med kontroller. Jun11787 sänkte särskilt virusnivåerna i både muskel och ryggmärg under detektionsgränsen och bevarade motorneuroner i ryggmärgen, vilket lämnade behandlade djur i praktiken utan svaghet.
Vad detta betyder för framtida utbrott
För familjer och kliniker är budskapet hoppfullt men försiktigt. Dessa experiment visar att det är möjligt att designa små molekyler som riktar sig direkt mot virusskalet, når nervsystemet och meningsfullt dämpar eller till och med förhindrar förlamning — åtminstone hos möss. Jun11695 och Jun11787 är tidiga ledande kandidater, inte redo för mänsklig användning, och viktiga hinder kvarstår, inklusive utveckling av orala formuleringar och skydd mot resistens. Ändå validerar arbetet tydligt virusskalet som ett läkemedelsmål för enterovirus D68 och erbjuder en konkret ritning för läkemedel som en dag kan skydda barn mot denna sällsynta men förödande form av förlamning.
Citering: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
Nyckelord: enterovirus D68, akut slapp myelit, design av antivirala läkemedel, virala kapsidhämmare, neurologisk infektion