Clear Sky Science · ar
تصميم منطقي والتحقق في الجسم الحي لمثبطات الكبسيد لفيروس إنتيرو-دي68
لماذا هذا مهم للآباء والأطباء
كل بضع سنوات، يجتاح جرثوم غير معروف إلى حد ما يُدعى فيروس إنتيرو D68 المجتمعات، ويصيب في الغالب الأطفال. بالنسبة لمعظمهم، يبدو الأمر كمجرد نزلة برد شديدة. لكن في حالات نادرة يهاجم الفيروس الحبل الشوكي، مما يترك الأطفال بضعف مفاجئ يشبه شلل الأطفال أو حتى شلل دائم. لا يوجد لقاح أو دواء مضاد للفيروسات معتمد لهذا الفيروس. تصف هذه الدراسة كيف صمم العلماء واختبروا دواءين تجريبيين يعوقان الغلاف الخارجي للفيروس، يحميان الحبل الشوكي في الفئران، وقد يشكلان طريقًا محتملًا لعلاجات مستقبلية لهذه النوبات المقلقة.
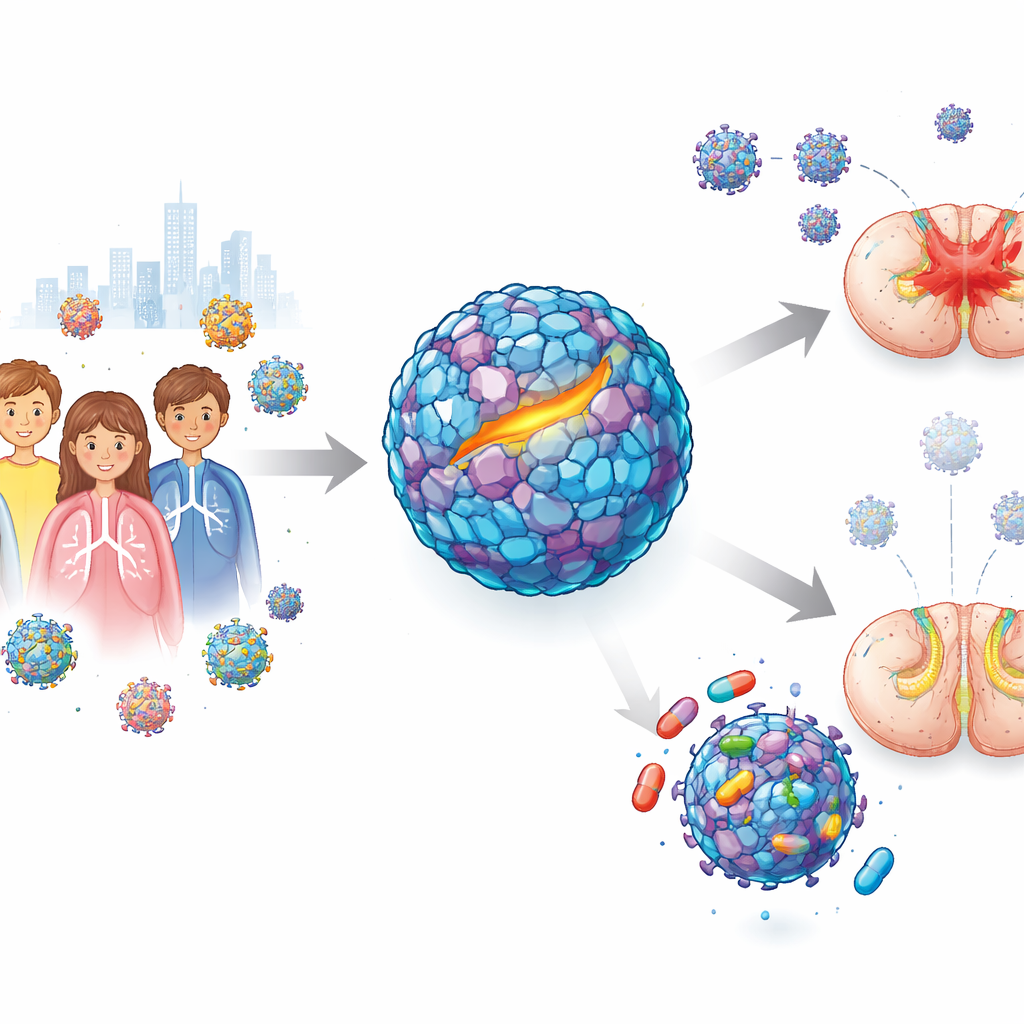
من نزلات برد خفيفة إلى ضعف مفاجئ
ينتشر فيروس إنتيرو D68 عادة عبر السعال والعطس ويسبب مشاكل تنفسية خفيفة. ومع ذلك، خلال تفشٍّ كبير عام 2014، لاحظ الأطباء نمطًا مقلقًا: بعض الأطفال المصابين طوّروا التهاب النخاع الرخو الحاد، وهي حالة تصبح فيها الذراعان أو الساقان ضعيفتين أو مرتخيتين بسرعة. أظهرت الدراسات أن السلالات الأحدث من الفيروس قادرة بشكل أفضل على إصابة الخلايا العصبية مقارنة بالسابقة، مما يثير القلق من أن هذا العامل الممرض قد يسبب تفشيات أوسع وأكثر شدة. بالرغم من سنوات من الجهود، فشلت مرشحات الأدوية السابقة التي بدت واعدة في أطباق المختبر في حماية الحيوانات، خصوصًا في النماذج التي تحاكي المرض العصبي. هذا ترك فجوة ملحة: هل يمكن لدواء أن يوقف هذا الفيروس بعد أن يبدأ في مهاجمة الجهاز العصبي بالفعل؟
تصميم قفل أفضل لغلاف الفيروس
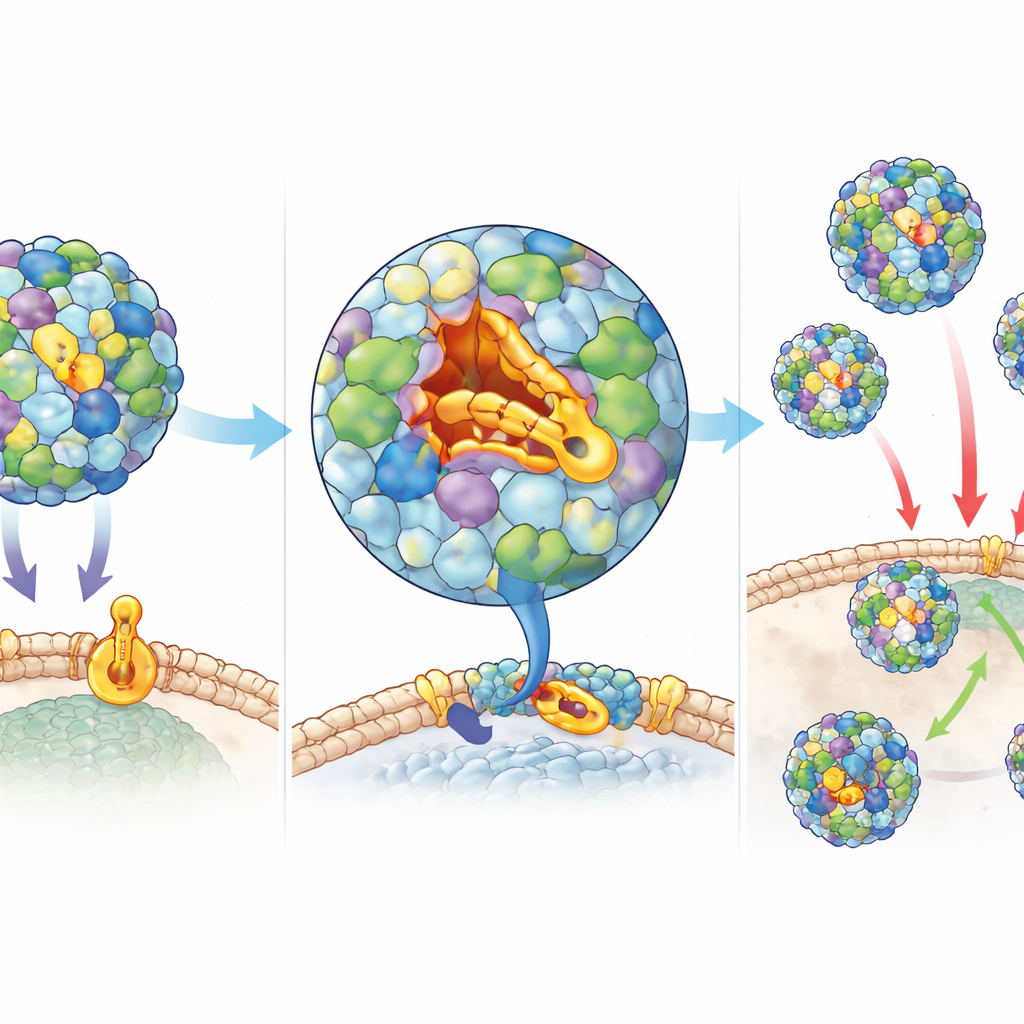
الفيروس ملفوف بغلاف بروتيني قوي، أو كبسيد، يحمي مادته الوراثية ويساعده على الالتصاق بالخلايا البشرية. أحد بروتينات هذا الغلاف، المسمى VP1، يحتوي على أخدود ضيق معروف باسم الواد (canyon)، والذي عادةً ما يحتضن جزيئًا دهنيًا يساعد في إبقاء الغلاف مستقرًا وجاهزًا للعدوى. حاولت الأدوية السابقة الانغلاق في هذا الأخدود لكنها لم تكن فعّالة بما فيه الكفاية في الحيوانات. في هذه الدراسة، استخدم الباحثون فحصًا حاسوبيًا عبر ملايين الجزيئات المرشحة للعثور على تلك التي قد تلائم الواد بإحكام. ثم قاموا بتحسين أفضل النتائج من خلال الكيمياء الدوائية، مهيئين أشكالها ومجموعاتها الكيميائية لتتماسك مع الجيب بقوة أكبر وتدوم أطول في الجسم. أسفر هذا المسار عن مركبين بارزين، أُطلق عليهما Jun11695 وJun11787، اللذان أوقفا الفيروس بقوة عن إتلاف الخلايا في الزرع بتركيزات منخفضة جدًا.
رؤية الدواء أثناء العمل ورسم مقاومة الفيروس
باستخدام المجهر الإلكتروني بالتبريد عالي الدقة (cryo-EM)، بصّر الفريق كيف تستقر المركبات الجديدة عميقًا داخل جيب الواد على غلاف الفيروس، مكونة العديد من التلامسات المحكمة مع بروتينات الكبسيد المحيطة. يبدو أن هذا الارتباط يقفل الغلاف في شكل مستقر يمنع الفيروس من تنفيذ خطوات العدوى المبكرة. أكدت تجارب توقيت الإضافة أن الأدوية تكون أكثر فعالية عندما تكون حاضرة قبل أو أثناء دخول الفيروس إلى الخلايا، ولكن ليس لاحقًا، وهو ما يتوافق مع آلية تستهدف الغلاف. عندما نما الفيروس مرارًا في وجود أحد المركبين، Jun11695، ظهرت طفرات نادرة أصبحت أقل حساسية للدواء. خرائط هذه الطفرات أوضحت مواقع محددة على بروتينات الغلاف التي تلامس المركب، مما ساعد على تأكيد الآلية بينما أظهر أيضًا أن المقاومة تأتي مع تكلفة على لياقة الفيروس.
حماية الحبل الشوكي في نموذج الفأر
السؤال الحاسم كان ما إذا كانت هذه المركبات المصممة قادرة على منع الشلل في حيوانات حية. استخدم الباحثون نموذج فأر مثبت جيدًا حيث يُحقن الصغار حديثو الولادة بالفيروس في عضلة الساق ثم يطوّرون ضعفًا تدريجيًا في الأطراف الخلفية مع انتشار الفيروس إلى الحبل الشوكي وموت الخلايا الحركية. تم امتصاص كلا المركبين جيدًا بعد الحقن وبقيا في مجرى الدم لساعات عديدة. عندما بدأ العلاج فورًا بعد العدوى، لم تُظهر الفئران التي تلقت جرعات يومية من Jun11695 أو Jun11787 أي علامة على الشلل واكتسبت وزنًا أكثر من إخوتها غير المعالجين. حتى عندما تأخر بدء الجرعات لمدة 24 ساعة أو بدأ العلاج فقط بعد أول علامات واضحة لضعف الأطراف، قلّلت الأدوية بشكل كبير من درجات الشلل مقارنة بالمراقِبين. خفض Jun11787، على وجه الخصوص، مستويات الفيروس في كل من العضلات والحبل الشوكي إلى ما دون حد الاكتشاف وحافظ على الخلايا الحركية في الحبل الشوكي، تاركًا الحيوانات المعالجة خالية في الأساس من الضعف.
ماذا يعني هذا لتفشيات مستقبلية
بالنسبة للعائلات والعيادات، الرسالة الأساسية متفائلة لكنها حذرة. تُظهر هذه التجارب أنه من الممكن تصميم جزيئات صغيرة تستهدف غلاف الفيروس مباشرةً، وتصل إلى الجهاز العصبي، وتقلّل بشكل ملموس أو حتى تمنع الشلل — على الأقل في الفئران. يُعد Jun11695 وJun11787 مرشحين في مرحلة مبكرة، وليسا جاهزين للاستخدام البشري، ولا تزال هناك عقبات مهمة، بما في ذلك اختبار أشكال فموية والحماية من المقاومة. ومع ذلك، تؤكد هذه الدراسة الغلاف الفيروسي كهدف دوائي لفيروس إنتيرو D68 وتقدّم مخططًا عمليًا لأدوية قد تحمي الأطفال يومًا ما من هذا الشكل النادر لكنه المدمّر من الشلل.
الاستشهاد: Li, K., Rudy, M.J., Klose, T. et al. Rational design and in vivo validation of capsid inhibitors for enterovirus D68. Nat Commun 17, 3052 (2026). https://doi.org/10.1038/s41467-026-69351-x
الكلمات المفتاحية: فيروس إنتيرو D68, التهاب النخاع الرخو الحاد, تصميم أدوية مضادة للفيروسات, مثبطات غلاف الفيروس, عدوى عصبية