Clear Sky Science · zh
抑制癌症干细胞免疫检查点 SOAT1 通过小鼠跨细胞 20(S)-羟基胆固醇–GPR132 通路抑制调节性 T 细胞功能
将癌症的胆固醇伎俩反过来对付它
免疫治疗已经改变了癌症治疗格局,但许多患者仍然收效甚微,因为肿瘤会想办法躲避免疫系统。本研究揭示了这一“捉迷藏”游戏中一个意想不到的同谋:存在于癌症干细胞内的一个胆固醇处理酶。研究人员用一种新的试验性药物阻断该酶,发现可以唤醒机体防御,使小鼠中顽固肿瘤对治疗变得更为脆弱。
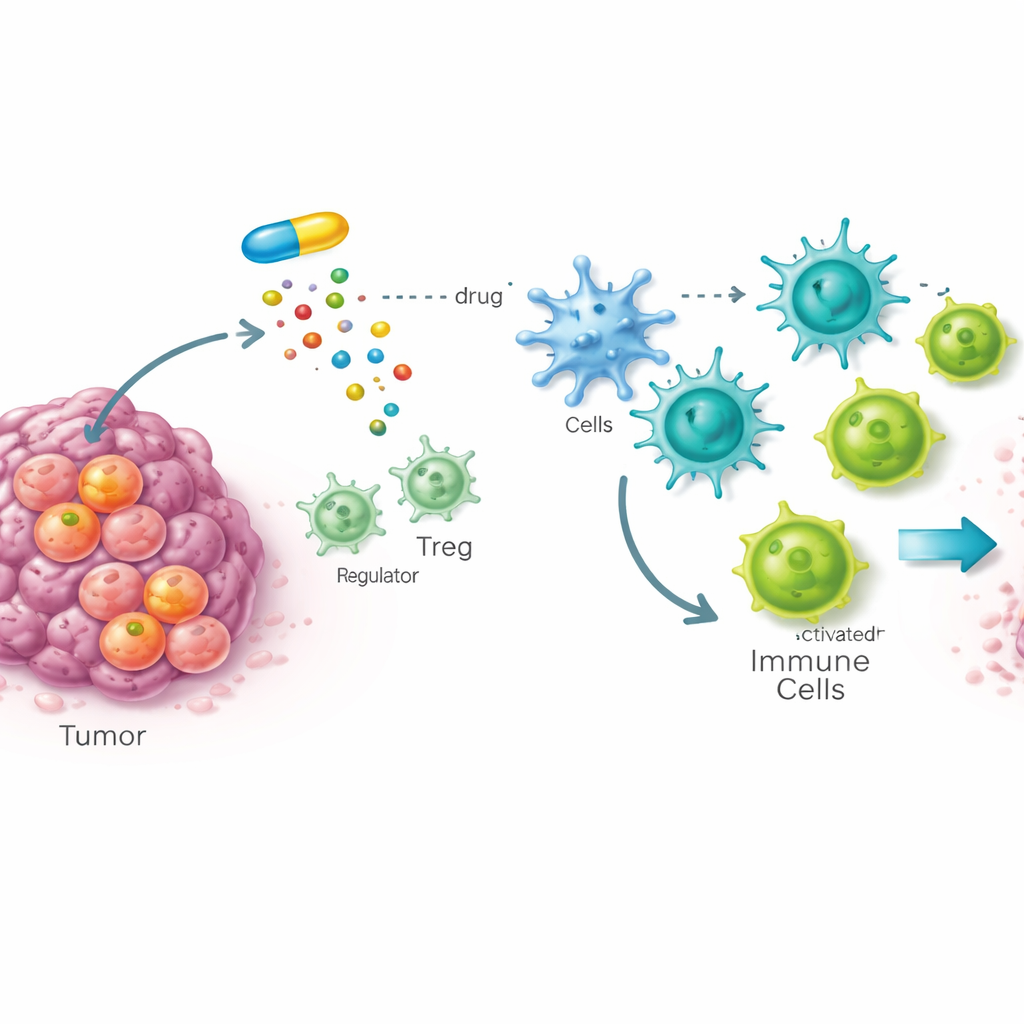
癌症干细胞的一个隐蔽弱点
许多肿瘤由癌症干细胞驱动,这是一小群能够再生肿瘤且常常耐受疗法的细胞。研究团队在携带干细胞样肿瘤的果蝇中建立了全身药物筛选,寻找能够选择性损伤这些危险细胞而不伤害正常组织的化合物。在近一万种候选物中,一种名为 STK 的化合物脱颖而出。后续在小鼠和人类癌细胞中的研究显示,STK 与一种名为 SOAT1 的酶紧密且特异地结合,SOAT1 帮助将过量胆固醇封存为储存滴。重要的是,SOAT1 在癌症干细胞中的含量远高于普通细胞,其存在与若干人类癌症的晚期病程和较差生存率有关。
在多种癌症类型中减缓肿瘤生长
当研究者用 STK 治疗小鼠时,在包括结肠、肝、肺、乳腺和皮肤癌在内的多种模型中,肿瘤缩小或生长显著变慢。在发生于原位器官的基因工程小鼠中,STK 降低了癌症干细胞数量,减轻了肿瘤负担并延长了存活期。在移植肿瘤模型中——包括在“人源化”小鼠中生长的患者来源肿瘤——STK 同样抑制了肿瘤生长且毒性迹象有限。基因学实验证明这些益处依赖于 SOAT1:当肿瘤细胞中已沉默 SOAT1 时,加入 STK 并未带来额外好处。总体数据指向 SOAT1 作为肿瘤用于繁荣和逃避免疫控制的共同代谢“检查点”。
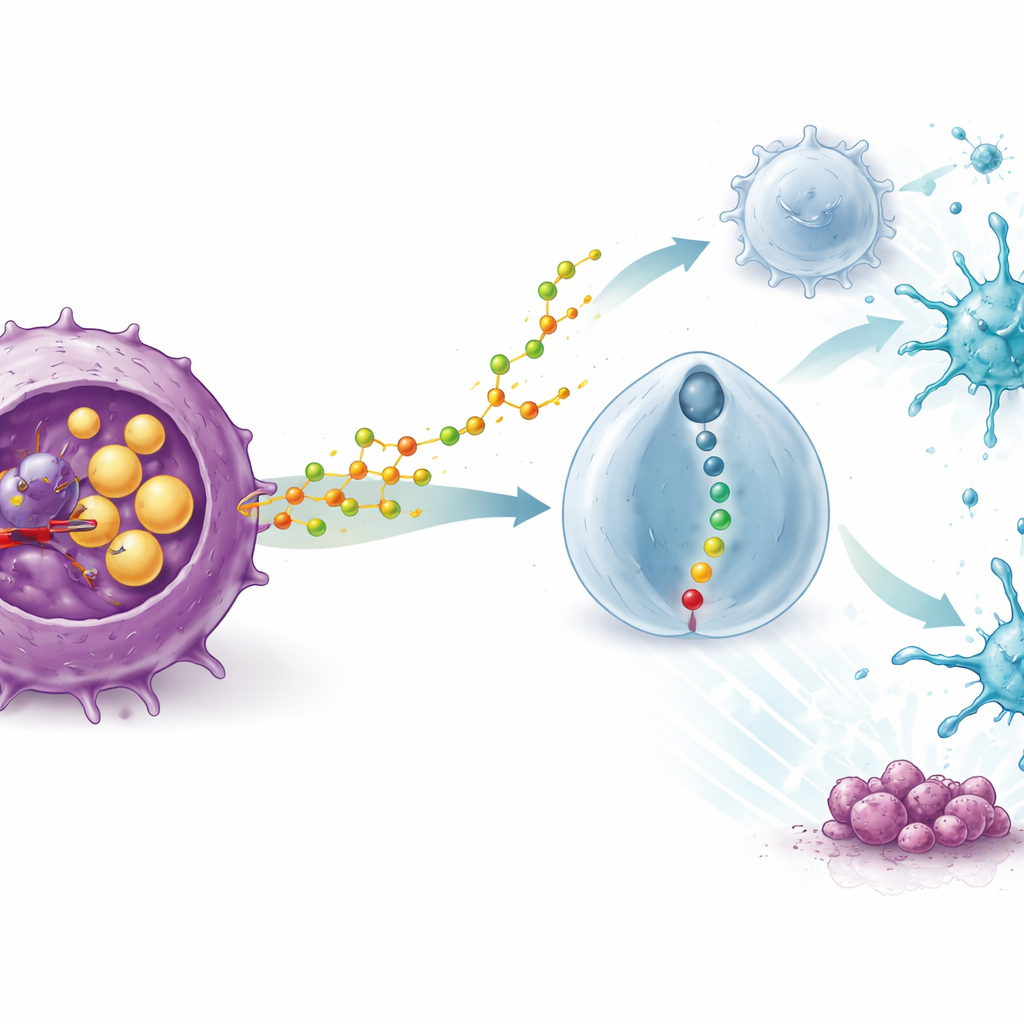
胆固醇代谢副产物如何重编程免疫细胞
最显著的发现是 STK 的效力依赖于完整的免疫系统。在免疫缺陷小鼠中,该药失去了抗肿瘤作用,阻断 T 细胞则抹去了其益处。肿瘤样本的单细胞 RNA 测序显示,STK 治疗使肿瘤浸润了有益的免疫细胞——尤其是呈递肿瘤物质的树突状细胞和杀伤性的 CD8 T 细胞——同时显著减少了调节性 T 细胞(Tregs)的数量和功能强度。机制研究揭示了原因:在肿瘤细胞中阻断 SOAT1 使它们释放出更多一种特定的氧化胆固醇分子 20(S)-羟基胆固醇。该分子被 Tregs 吸收并激活其表面的受体 GPR132,进而开启一条内部信号链。随着该通路被触发,Tregs 变得“脆弱”,产生更少的抑制因子并失去对树突状细胞和杀伤性 T 细胞的抑制控制。
从“冷”肿瘤到“热”靶标
通过以这种方式削弱 Tregs,STK 有效地把肿瘤微环境从免疫沉默的“冷”态重编程为高度活跃的“热”态。树突状细胞成熟并显示出更多活化标志,而 CD8 T 细胞产生更多用于攻击癌细胞的分子。STK 治愈肿瘤的小鼠在再次遭遇肿瘤挑战时获得了更好的保护,表明可能形成了持久的免疫记忆。关键是,将 STK 与现有阻断 PD‑1 或 CTLA‑4 的检查点疗法联合使用,在小鼠模型中进一步改善了肿瘤控制,提示抑制 SOAT1 可能拓宽并加深当前免疫疗法的反应范围。
这对未来癌症治疗可能意味着什么
对非专业读者来说,结论是某些癌症通过重塑其胆固醇利用方式来掩护自己,尤其是在其干样核心细胞内。这项工作表明,关闭一个关键的胆固醇储存酶 SOAT1,不仅能削弱癌症干细胞,还会促使它们释放一种化学求救信号,从而解除抑制性 T 细胞的武装并召集其余免疫军队。在小鼠模型和早期患者来源的肿瘤中,这一策略使多种癌症更易被控制,并且与现有免疫治疗药物联合使用时效果尤其显著。尽管在广泛用于人类之前仍需大量测试,针对 SOAT1 及 20(S)-羟基胆固醇–GPR132 通路为将机体自身防御更可靠地转向抗癌提供了一个有前景的新途径。
引用: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
关键词: 癌症免疫治疗, 癌症干细胞, 胆固醇代谢, 调节性 T 细胞, 免疫检查点治疗