Clear Sky Science · ar
مثبِّط نقطة تفتيش مناعية لخلايا السرطان الجذعية SOAT1 يُضعِف وظائف الخلايا التائية المنظمة عبر مسار عبر خلوي 20(S)-هيدروكسيكوليستيرول–GPR132 في الفئران
تحويل حيل السرطان المتعلقة بالكوليستيرول ضده
غيّر العلاج المناعي موازين علاج السرطان، لكن العديد من المرضى لا يزالون يحصلون على فوائد محدودة لأن أورامهم تجد طرقًا للاختباء من جهاز المناعة. تكشف هذه الدراسة عن متواطئ غير متوقع في لعبة الاختباء هذه: إنزيم يتعامل مع الكوليستيرول داخل خلايا السرطان الجذعية. من خلال حجب هذا الإنزيم بدواء تجريبي جديد، وجد الباحثون طريقة لإيقاظ دفاعات الجسم وجعل الأورام العنيدة في الفئران أكثر عرضة للعلاج.
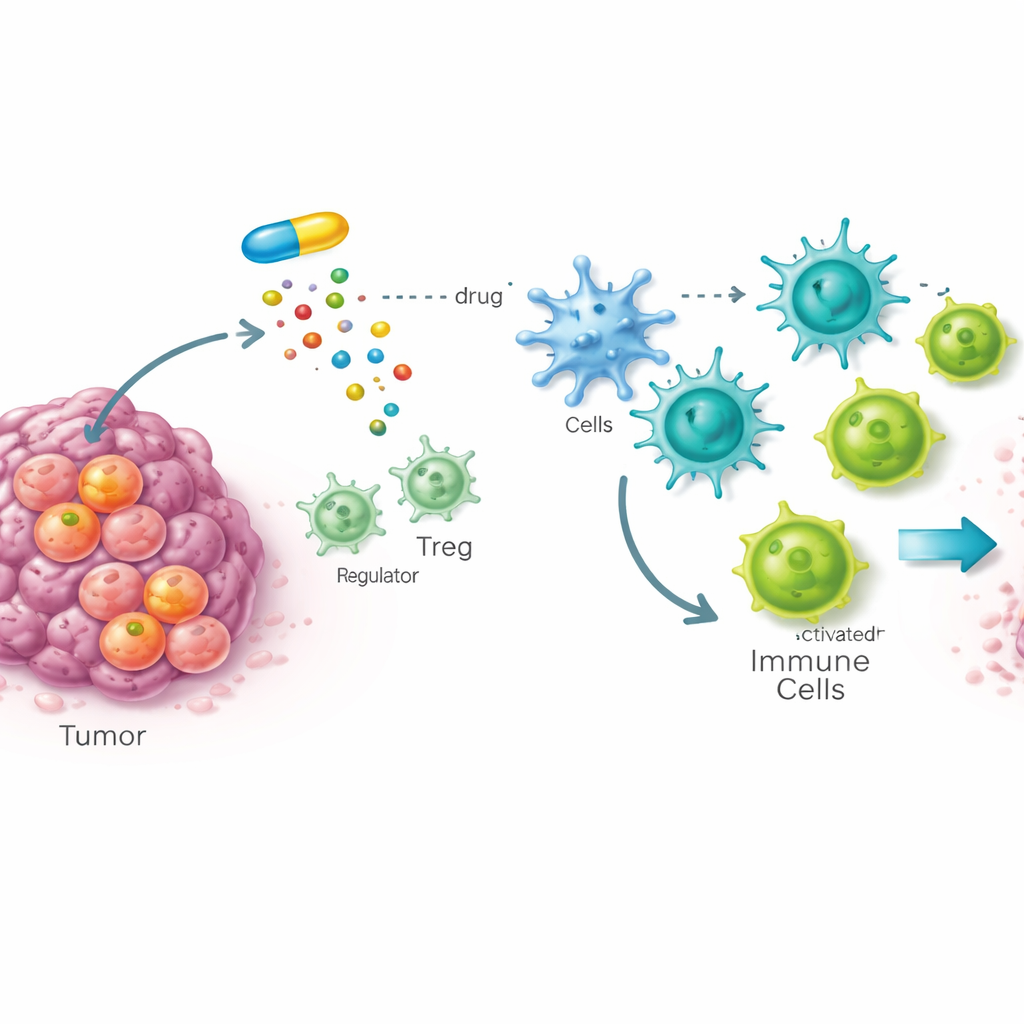
نقطة ضعف خفية في خلايا السرطان الجذعية
تحفّز العديد من الأورام بواسطة خلايا السرطان الجذعية، وهي مجموعة صغيرة من الخلايا القادرة على تجديد الورم وغالبًا ما تقاوم العلاج. أنشأ الفريق فحصًا دوائيًا شاملًا على الحيوان الكامل في ذبابة الفاكهة الحاملة لأورام شبيهة بالخلايا الجذعية للبحث عن مركبات تضر بهذه الخلايا الخطرة بشكل انتقائي مع الحفاظ على الأنسجة الطبيعية. من بين ما يقرب من عشرة آلاف مرشح، برز مركب واحد اسمه STK. أظهرت دراسات متابعة في خلايا سرطانية من الفئران والبشر أن STK يرتبط بقوة وبشكل محدد بأنزيم يُدعى SOAT1، الذي يساعد على تعبئة فائض الكوليستيرول في قطرات تخزين. والأهم أن SOAT1 وُجد بكميات أكبر بكثير في خلايا السرطان الجذعية مقارنة بالخلايا العادية، وكانت وجوديته مرتبطة بمرض متقدم وبانخفاض البقاء في عدة أنواع من السرطان البشري.
إبطاء الأورام عبر العديد من أنواع السرطان
عندما عالج الباحثون الفئران بـSTK، تقلصت الأورام أو نما نموها بوتيرة أبطأ بكثير في طيف واسع من النماذج، بما في ذلك سرطانات القولون والكبد والرئة والثدي والجلد. في فئران مهندسة وراثيًا تطوّر فيها السرطان في أعضائها الأصلية، قلّل STK من عدد خلايا السرطان الجذعية وخفض العبء الورمي وطوّل البقاء. في نماذج أورام مزروعة، بما في ذلك أورام مشتقة من مرضى نمت في فئران مُمَثلة إنسانياً، قَلّص STK نمو الورم أيضًا مع سُميّة ظاهرة قليلة. أكدت تجارب جينية أن هذه الفوائد تعتمد على SOAT1: عندما كان SOAT1 مُسكَّنًا بالفعل في خلايا الورم، لم يضف إعطاء STK فائدة إضافية. إجمالًا، تشير البيانات إلى أن SOAT1 يعمل كـ"نقطة تفتيش" أيضية شائعة تستخدمها الأورام لتزدهر وتتملص من السيطرة.
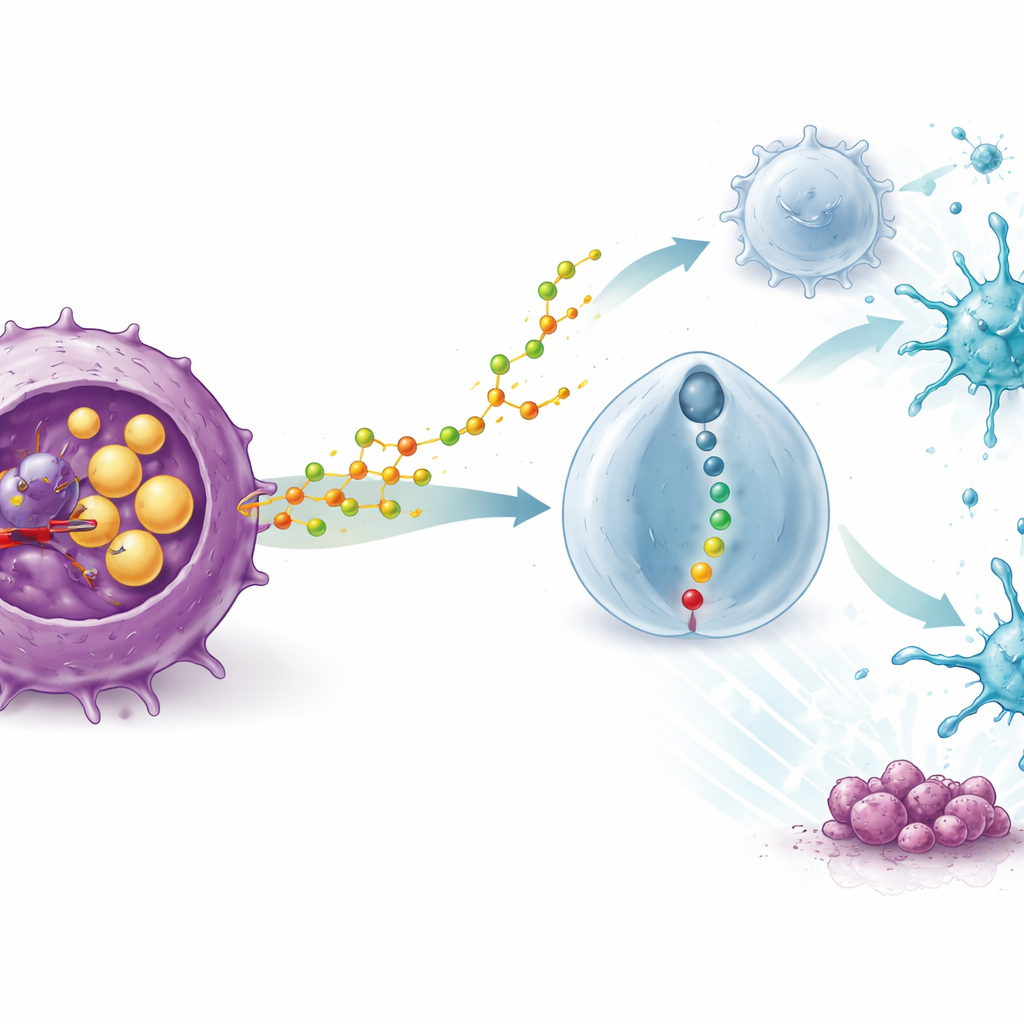
كيف يعيد ناتج ثانوي من الكوليستيرول تشكيل الخلايا المناعية
أبرز النتائج كانت أن فعالية STK اعتمدت على جهاز مناعي سليم. في فئران ناقصة المناعة، فقد الدواء تأثيره المضاد للورم، وإبطال دور الخلايا التائية ألغى فوائد الدواء. أظهر تسلسل الرنا الأحادي الخلوي لعينة الأورام أن علاج STK ملأ الأورام بخلايا مناعية مفيدة — لا سيما الخلايا الشجيرية (اللاصقة) التي تعرض مواد الورم والخلايا التائية القاتلة CD8 — بينما قلّص بشكل حاد عدد وقوة الخلايا التائية المنظمة (Tregs)، التي تعمل عادة كمكابح للاستجابات المناعية. كشفت دراسات آلية السبب: حجب SOAT1 في خلايا الورم دفعها إلى إطلاق المزيد من جزيء كوليستيرول مؤكسد محدد، 20(S)-هيدروكسيكوليستيرول. التقطت هذه الجزيئات الخلايا التائية المنظمة ونشّطت مستقبلًا على سطحها يُدعى GPR132، والذي بدوره شغّل سلسلة إشارات داخلية. ومع اشتعال هذا المسار، أصبحت الخلايا التائية المنظمة "هشة"، تُنتج عوامل مُخمِّدة أقل وتفقد تماسكها مع الخلايا الشجيرية والخلايا التائية القاتلة.
من أورام باردة إلى أهداف ساخنة
بإضعاف الخلايا التائية المنظمة بهذه الطريقة، أعاد STK فعليًا تشكيل البيئة الميكروية للورم من حالة صامتة مناعيًا أو "باردة" إلى حالة نشطة للغاية أو "ساخنة". نضجت الخلايا الشجيرية وأظهرت علامات تنشيط أكثر، بينما أنتجت خلايا CD8 مستويات أعلى من الجزيئات اللازمة لمهاجمة الخلايا السرطانية. الفئران التي تخلصت من الأورام بعد علاج STK كانت محمية بصورة أفضل عند تحدٍ ثانٍ للورم، مما يوحي بتشكّل ذاكرة مناعية دائمة. والأهم أن الجمع بين STK والعلاجات القائمة لنقاط التفتيش التي تحجب PD-1 أو CTLA-4 حسّن السيطرة على الورم في نماذج الفئران، مما يشير إلى أن تثبيط SOAT1 قد يوسّع ويُعمّق الاستجابات للعلاجات المناعية الحالية.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
لغير المتخصص، الرسالة هي أن بعض السرطانات تحمي نفسها بإعادة تشكيل طريقة استخدامها للكوليستيرول، لا سيما داخل خلاياها الشبيهة بالجذعية. تُظهر هذه العمل أن إيقاف إنزيم رئيسي لتخزين الكوليستيرول، SOAT1، لا يجوع خلايا السرطان الجذعية فحسب بل يدفعها أيضًا إلى إطلاق إشارة كيميائية استغاثية تعطل الخلايا التائية القمعية وتعبئ بقية جيش المناعة. في نماذج الفئران وأورام مبكرة مشتقة من مرضى، يجعل هذا النهج أنواعًا متعددة من السرطان أكثر قابلية للسيطرة ويعمل بشكل جيد خاصة عند الجمع معه أدوية المناعة الموجودة. وبينما تبقى اختبارات كثيرة قبل أن يُجرّب على نطاق واسع لدى البشر، فإن استهداف SOAT1 ومسار 20(S)-هيدروكسيكوليستيرول–GPR132 يقدم وسيلة واعدة جديدة لتحويل دفاعات الجسم ضده بشكل أكثر موثوقية.
الاستشهاد: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
الكلمات المفتاحية: العلاج المناعي للسرطان, خلايا السرطان الجذعية, تمثُّل الكوليستيرول, الخلايا التائية المنظمة, علاج نقاط التفتيش المناعية