Clear Sky Science · he
עיכוב נקודת הבקרה החיסונית של תאי גידול-גידול SOAT1 מדכא את תפקודי תאי T רגולטוריים דרך מסלול בין-תאי של 20(S)-הידרוקסיכולסטראול–GPR132 בעכברים
להפנות את טריקי הכולסטרול של הסרטן נגדו
הטיפול בסרטן השתנה בתכלית הודות לאימונותרפיה, אך רבים מהחולים עדיין נהנים ממעט תועלת משום שהגידולים מוצאים דרכים להתחבא ממערכת החיסון. מחקר זה חושף שותף בלתי צפוי במשחק המחבואים הזה: אנזים המטפל הכולסטרול בתוך תאי גידול-גידול. על‑ידי חסימת האנזים הזה עם תרופה ניסיונית חדשה, החוקרים מצאו דרך להפעיל מחדש את ההגנות של הגוף ולהפוך גידולים עקשניים בעכברים לפגיעים הרבה יותר לטיפול.
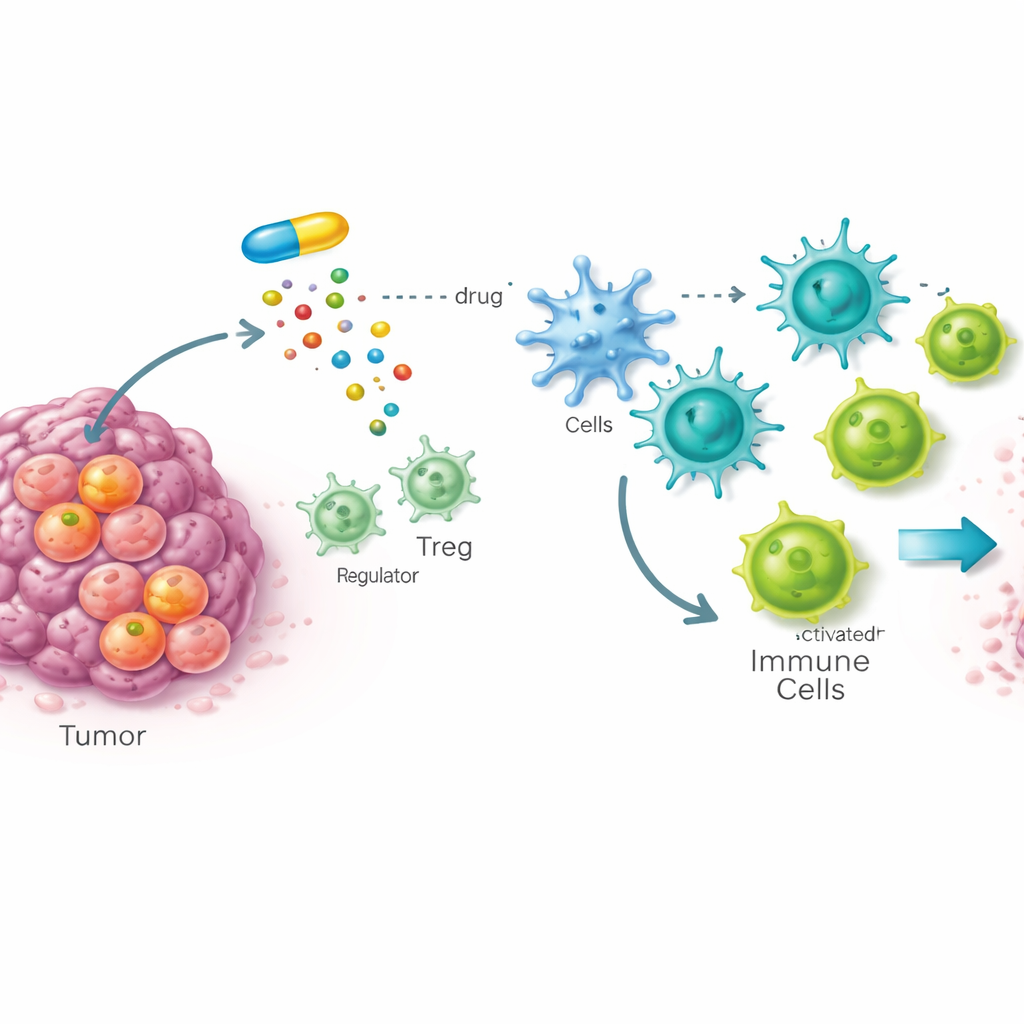
נקודת חולשה נסתרת בתאי גידול-גידול
רבים מהגידולים מונעים על ידי תאי גידול-גידול, קבוצה קטנה של תאים היכולים לחדש את הגידול ולעיתים לעמוד בפני טיפולים. הצוות בנה מסך תרופות על חיה שלמה בזבוב הפרי שנושאת גידולים בעלי מאפיינים של תאי גידול-גידול כדי לחפש תרכובות שפוגעות באופן סלקטיבי בתאים מסוכנים אלה ובו בזמן משמרות רקמה רגילה. מתוך כמעט עשרת אלפים מועמדים, תרכובת אחת בשם STK בלטה. עבודות המשך בתאי גידול של עכבר ואדם הראו כי STK נקשרת בחוזקה ובספציפיות לאנזים בשם SOAT1, שעוזר לארוז עודפי כולסטרול לטיפות אחסון. חשוב מכך, SOAT1 נמצא בשפע רב יותר בתאי גידול-גידול מאשר בתאים רגילים, ונוכחותו נקשרה למחלה מתקדמת ולתוחלת חיים קצרה במספר סוגי סרטן אנושיים.
האטת גידולים במגוון סוגי סרטן
כאשר החוקרים טיפלו בעכברים ב‑STK, הגידולים הצטמצמו או צמחו הרבה יותר לאט במגוון רחב של מודלים, כולל סרטן המעי הגס, בכבד, בריאות, שד ובעור. בעכברים מהונדסים גנטית שמפתחים גידולים באיבריהם המקוריים, STK הקטין את מספר תאי גידול-גידול, הפחית את העומס הגידולי והאריך את השרידה. במודלים של גידול מושתל, כולל גידולים ממטופלים שהושרו בעכברים מובנים אנושית, STK שוב צמצם צמיחה עם רעילות מועטה לכאורה. ניסויים גנטיים אישרו כי היתרונות הללו תלויים ב‑SOAT1: כאשר SOAT1 כבר הושתק בתאי הגידול, הוספת STK לא הביאה תועלת נוספת. בסך הכל הנתונים מצביעים על SOAT1 כ"נקודת בקרה" מטבולית שכיחה שהגידולים משתמשים בה כדי לשגשג ולהתחמק מבקרה.
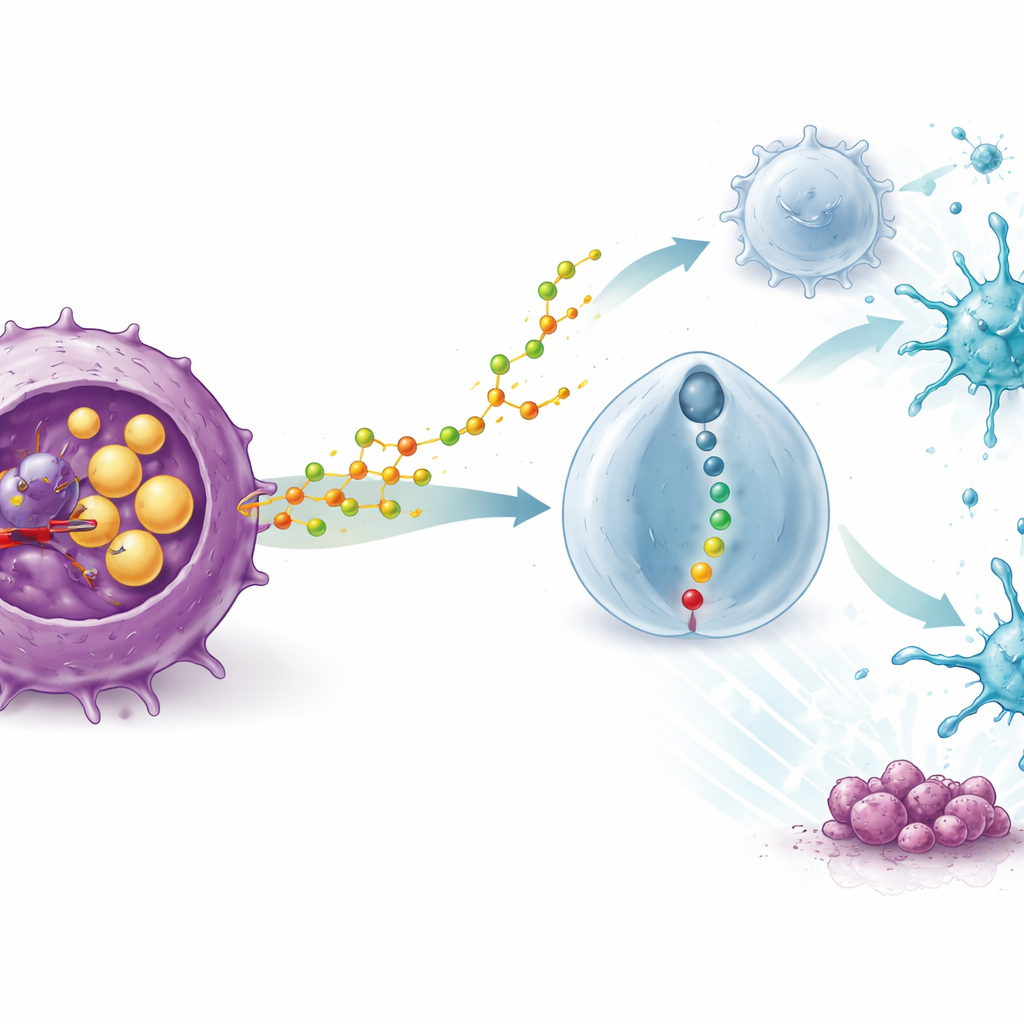
כיצד תוצר משנה של כולסטרול משנה את מירקם תאי החיסון
הממצא המרתק ביותר היה שעוצמתו של STK התבססה על מערכת חיסון שלמה. בעכברים חסרי חיסון, התרופה איבדה את האפקט האנטי‑גידולי שלה, וחסימת תאי T מחקה את יתרונותיה. ריצוף RNA של תא יחיד מדגימות גידול הראה שטיפול ב‑STK הציף את הגידולים בתאים חיסוניים מועילים — במיוחד תאים דנדריטים שמציגים חומר גידולי ותאי CD8 קטלניים — בעוד שהוא הקטין ברהיטות את מספרם ועוצמתם של תאי T רגולטוריים (Tregs), שפועלים בדרך כלל כבלמים על תגובות החיסון. מחקרים מכניסטיים חשפו מדוע: חסימת SOAT1 בתאי הגידול גרמה להם לשחרר יותר מולקולת כולסטרול מחמצנת ספציפית, 20(S)-הידרוקסיכולסטטרול. מולקולה זו נקלטה על ידי Tregs והפעילה קולט על פני השטח שלהם שנקרא GPR132, שהפעיל בתורו שרשרת איתות פנימית. כאשר מסלול זה הדליק, ה‑Tregs הפכו ל"שבריריים", ייצרו פחות גורמי דיכוי ואיבדו את אחיזתם בתאים דנדריטים ובתאי T קטלניים.
מגידולים קרים למטרות חמות
על‑ידי החלשת ה‑Tregs בדרך זו, STK למעשה שינה את סביבת המיקרו של הגידול ממצב שקט חסר תגובה חיסונית, "קר" , למצב פעיל מאוד, "חם". התאים הדנדריטים בשלו והציגו יותר סמני הפעלה, בעוד שתאי CD8 ייצרו רמות גבוהות יותר של מולקולות הנחוצות להתקפת תאי הסרטן. עכברים שניקו גידולים לאחר טיפול ב‑STK היו מוגנים טוב יותר מפני אתגר גידולי חוזר, מה שמרמז שנוצר זיכרון חיסוני מתמשך. באופן מכריע, שילוב של STK עם טיפולים קיימים שמחסמים PD‑1 או CTLA‑4 שיפר עוד יותר את השליטה בגידולים במודלים של עכבר, ויש בכך רמז כי עיכוב SOAT1 עשוי להרחיב ולהעמיק את התגובות לאימונותרפיות הנוכחיות.
מה זה עשוי להשפיע על טיפול בסרטן בעתיד
ללא מומחיות, המסר הוא שחלק מהסרטן מסתיר את עצמו על‑ידי עיצוב מחדש של הדרך שבה הוא משתמש בכללסטרול, במיוחד במרכזו הדמוי‑גידולי. עבודה זו מראה כי כיבוי אנזים מרכזי לאחסון כולסטרול, SOAT1, לא רק מרעיב תאי גידול-גידול אלא גם דוחף אותם לשחרר אות מצוקה כימי שמנטרל תאי T מדכאים ומגייס את שאר צבא החיסון. במודלים של עכבר ובגידולים של מטופלים מוקדמים, אסטרטגיה זו הופכת מספר סוגי סרטן לניתנים לשליטה יותר ופועלת במיוחד טוב לצד תרופות אימונותרפיה קיימות. אמנם נדרש עוד מבחן לפני שניתן יהיה ליישם זאת באופן נרחב בבני אדם, אך מיקוד ב‑SOAT1 ובמסלול 20(S)-הידרוקסיכולסטראול–GPR132 מציע דרך מבטיחה חדשה להפנות את ההגנות הטבעיות של הגוף נגד הסרטן באופן אמין יותר.
ציטוט: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
מילות מפתח: אימונותרפיה לסרטן, תאי גידול-גידול, מטבוליזם הכולסטרול, תאי T רגולטוריים, תרפיית נקודות בקרה חיסוניות