Clear Sky Science · pl
Hamowanie punktu kontrolnego komórek macierzystych nowotworu SOAT1 tłumi funkcje limfocytów T regulatorowych poprzez transkomórkową ścieżkę 20(S)-hydroksycholesterol–GPR132 u myszy
Wykorzystanie nowotworowych sztuczek z cholesterolem przeciwko nim
Terapia nowotworów uległa rewolucji dzięki immunoterapii, jednak u wielu pacjentów korzyści są wciąż ograniczone, ponieważ guzy znajdują sposoby ukrywania się przed układem odpornościowym. Badanie to ujawnia niespodziewanego wspólnika w tej grze w chowanego: enzym zajmujący się obrotem cholesterolu wewnątrz komórek macierzystych nowotworu. Hamując ten enzym nowym eksperymentalnym lekiem, badacze znaleźli sposób na pobudzenie obrony organizmu i znaczące zwiększenie wrażliwości opornych guzów u myszy na leczenie.
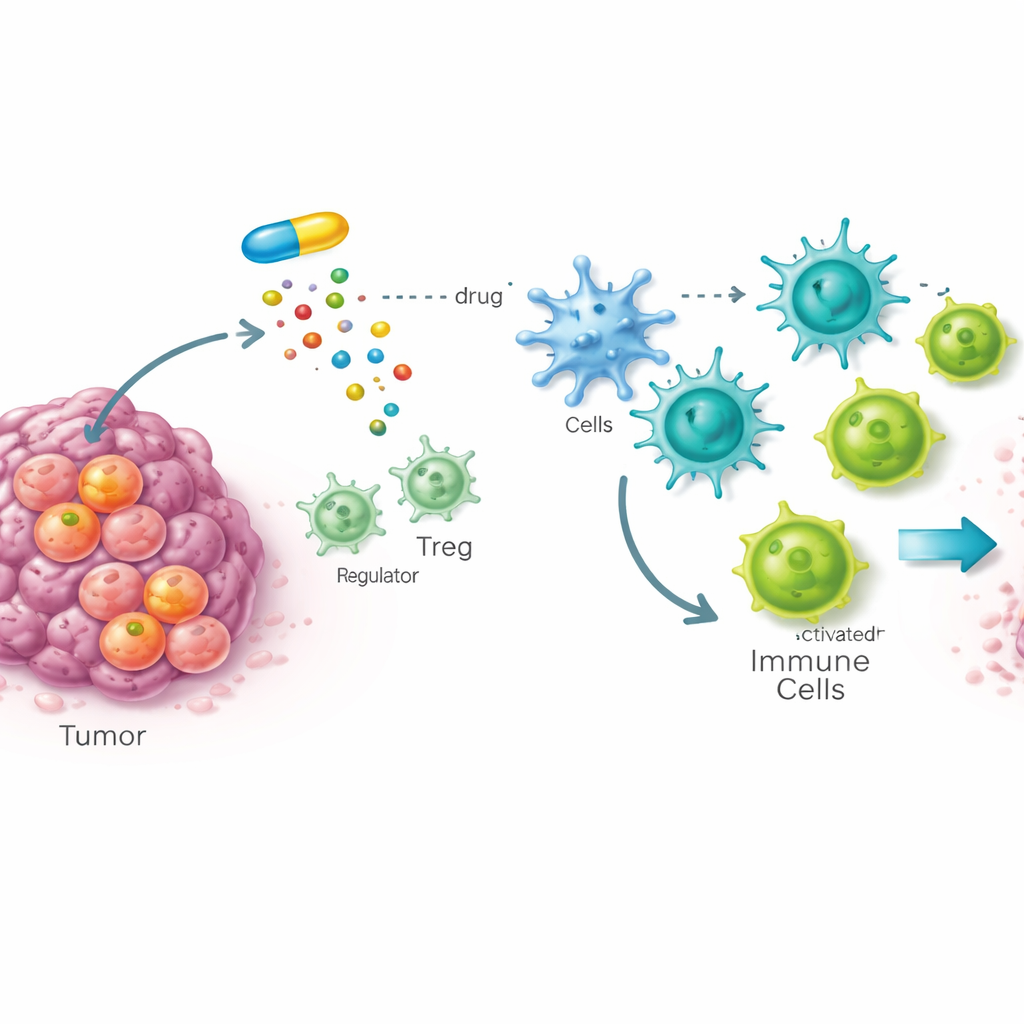
Ukryta słabość komórek macierzystych nowotworu
Wiele guzów napędzanych jest przez komórki macierzyste nowotworu — małą populację komórek, które potrafią odbudowywać guz i często są odporne na terapię. Zespół opracował przesiew leków obejmujący całe zwierzę (muszki owocowe) z nowotworami przypominającymi komórki macierzyste, aby wyszukać związki selektywnie niszczące te niebezpieczne komórki przy jednoczesnym oszczędzaniu tkanki zdrowej. Spośród prawie dziesięciu tysięcy kandydatów wyróżnił się jeden związek, nazwany STK. Badania u myszy i na komórkach ludzkich wykazały, że STK silnie i selektywnie wiąże się z enzymem SOAT1, który pomaga pakować nadmiar cholesterolu w krople magazynujące. Co ważne, SOAT1 okazał się znacznie bardziej obfity w komórkach macierzystych nowotworu niż w komórkach zwykłych, a jego obecność korelowała z zaawansowaną chorobą i gorszym przeżyciem w kilku rodzajach nowotworów u ludzi.
Hamowanie wzrostu guzów w różnych typach nowotworów
Gdy badacze leczyli myszy STK, guzy zmniejszały się lub rosły znacznie wolniej w szerokim zestawie modeli, w tym nowotworów jelita grubego, wątroby, płuca, piersi i skóry. W genetycznie modyfikowanych myszach rozwijających nowotwory w ich naturalnych narządach STK zmniejszał liczbę komórek macierzystych nowotworu, obciążenie nowotworem i wydłużał przeżycie. W modelach z przeszczepionymi guzami, w tym guzy pochodzące od pacjentów hodowane w humanizowanych myszach, STK ponownie ograniczał wzrost przy niewielkiej widocznej toksyczności. Eksperymenty genetyczne potwierdziły, że korzyści zależały od SOAT1: gdy SOAT1 był już wyciszony w komórkach nowotworowych, dodanie STK nie przynosiło dalszych korzyści. Łącznie dane wskazują na SOAT1 jako wspólny metaboliczny „punkt kontrolny”, którego guzy używają, by przetrwać i unikać kontroli.
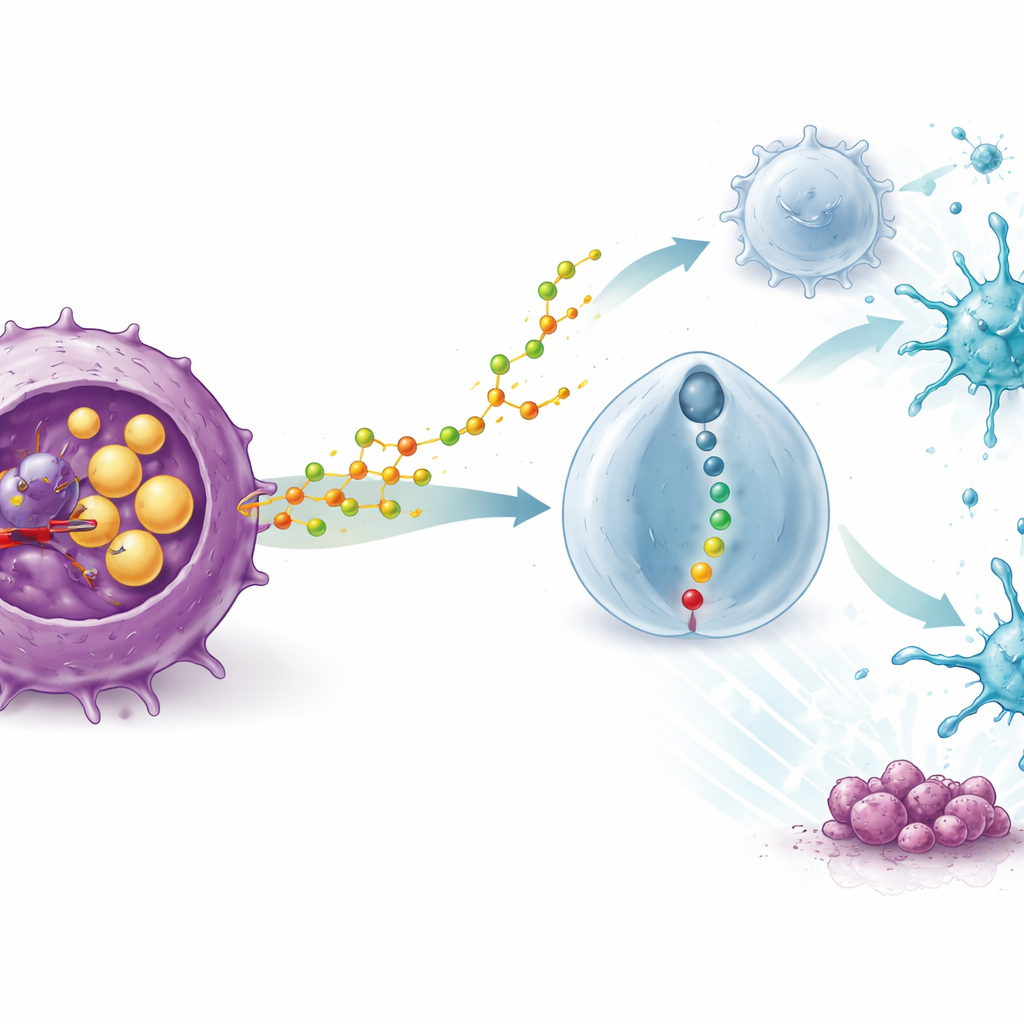
Jak produkt uboczny cholesterolu przeprogramowuje komórki odpornościowe
Najbardziej uderzające odkrycie polegało na tym, że skuteczność STK zależała od nieuszkodzonego układu odpornościowego. U myszy pozbawionych odporności lek tracił swój przeciwnowotworowy efekt, a zablokowanie komórek T likwidowało jego korzyści. Sekwencjonowanie RNA pojedynczych komórek z próbek guzów wykazało, że leczenie STK napływało do guzów z korzystnymi komórkami odpornościowymi — zwłaszcza komórkami dendrytycznymi prezentującymi materiał nowotworowy i zabójczymi limfocytami CD8 — przy jednoczesnym wyraźnym zmniejszeniu liczby i aktywności limfocytów T regulatorowych (Tregów), które normalnie działają jak hamulec odpowiedzi immunologicznej. Badania mechanistyczne wyjaśniły, dlaczego: zablokowanie SOAT1 w komórkach nowotworowych powodowało, że wydzielały one więcej określonej utlenionej cząsteczki cholesterolu, 20(S)-hydroksycholesterolu. Cząsteczka ta była przejmowana przez Tregi i aktywowała receptor na ich powierzchni zwany GPR132, co z kolei uruchamia wewnętrzny łańcuch sygnalizacyjny. W miarę aktywacji tej ścieżki Tregi stawały się „kruchymi” — wytwarzały mniej czynników supresyjnych i traciły zdolność hamowania komórek dendrytycznych i limfocytów cytotoksycznych.
Od „zimnych” guzów do gorących celów
Osłabiając Tregi w ten sposób, STK skutecznie przeprogramowywał mikrośrodowisko guza z immunologicznie cichego, czyli „zimnego”, stanu do wysoce aktywnego, „gorącego”. Komórki dendrytyczne dojrzewały i wykazywały więcej markerów aktywacji, podczas gdy limfocyty CD8 produkowały wyższe poziomy cząsteczek potrzebnych do ataku na komórki nowotworowe. Myszy, które oczyściły guzy po leczeniu STK, były lepiej chronione przed ponownym wyzwaniem nowotworowym, co sugeruje powstanie trwałej pamięci immunologicznej. Co kluczowe, łączenie STK z istniejącymi terapiami punktów kontrolnych blokującymi PD-1 lub CTLA-4 dodatkowo poprawiało kontrolę guza w modelach mysich, co sugeruje, że hamowanie SOAT1 mogłoby poszerzyć i pogłębić odpowiedzi na obecne immunoterapie.
Co to może oznaczać dla przyszłej opieki onkologicznej
Dla osoby niebędącej specjalistą przesłanie jest takie: niektóre nowotwory chronią się, przekształcając sposób wykorzystania cholesterolu, szczególnie w swoich komórkach o cechach macierzystych. Praca ta pokazuje, że wyłączenie kluczowego enzymu magazynującego cholesterol, SOAT1, nie tylko odcina źródła energii komórkom macierzystym nowotworu, ale także skłania je do uwolnienia chemicznego sygnału alarmowego, który unieszkodliwia supresyjne komórki T i mobilizuje resztę armii immunologicznej. W modelach mysich i wczesnych guzach pochodzących od pacjentów ta strategia ułatwia kontrolę wielu typów nowotworów i działa szczególnie dobrze w połączeniu z istniejącymi lekami immunoterapeutycznymi. Choć przed szerokim zastosowaniem u ludzi potrzebnych jest jeszcze wiele badań, ukierunkowanie na SOAT1 oraz szlak 20(S)-hydroksycholesterol–GPR132 oferuje obiecującą nową drogę do bardziej niezawodnego wykorzystania własnej odporności organizmu przeciwko rakowi.
Cytowanie: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
Słowa kluczowe: immunoterapia przeciwnowotworowa, komórki macierzyste nowotworu, metabolizm cholesterolu, limfocyty T regulatorowe, terapia punktów kontrolnych układu odpornościowego