Clear Sky Science · nl
Remming van de immuuncontrole in kankerstamcellen door SOAT1 onderdrukt regulatorische T‑cel functies via een trans‑cellulaire 20(S)-hydroxycholesterol‑GPR132‑route in muizen
De cholesteroltrucs van kanker tegen zichzelf gebruiken
De behandeling van kanker is door immunotherapie veranderd, maar veel patiënten profiteren nog steeds weinig omdat tumoren manieren vinden om zich te verbergen voor het immuunsysteem. Deze studie onthult een onverwachte medeplichtige in dat verstopspel: een cholesterolverwerkend enzym binnen kankerstamcellen. Door dit enzym met een nieuw experimenteel middel te blokkeren, vonden de onderzoekers een manier om de afweer van het lichaam te activeren en hardnekkige tumoren bij muizen veel kwetsbaarder voor behandeling te maken.
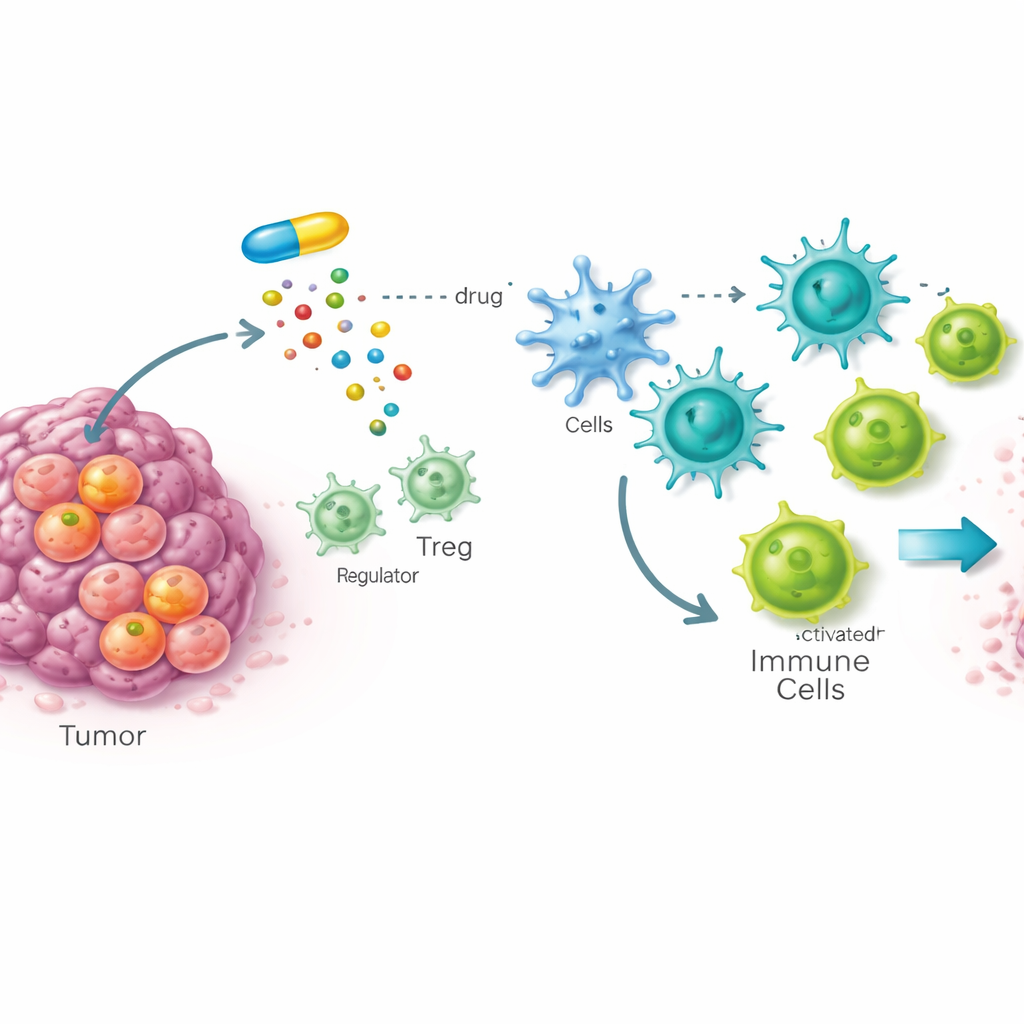
Een verborgen zwakke plek in kankerstamcellen
Veel tumoren worden aangestuurd door kankerstamcellen, een kleine groep cellen die de tumor kunnen regenereren en vaak therapie weerstaan. Het team ontwikkelde een hele‑dier drugscreen in fruitvliegen met stamcelachtige tumoren om verbindingen te vinden die deze gevaarlijke cellen selectief beschadigen en het normale weefsel sparen. Van bijna tienduizend kandidaten sprong één verbinding, STK genaamd, eruit. vervolgonderzoek in muis‑ en menselijke kankercellen toonde aan dat STK sterk en specifiek bindt aan een enzym genaamd SOAT1, dat helpt overtollig cholesterol in opslagdruppels te verpakken. Belangrijk is dat SOAT1 veel overvloediger bleek te zijn in kankerstamcellen dan in gewone cellen, en dat de aanwezigheid ervan werd geassocieerd met gevorderde ziektestadia en slechtere overleving bij meerdere menselijke kankers.
Tumoren vertragen in veel kankertypen
Wanneer de onderzoekers muizen behandelden met STK, krompen de tumoren of groeiden veel trager in een breed scala aan modellen, waaronder colon-, lever-, long-, borst‑ en huidkanker. In genetisch gemodificeerde muizen die kanker ontwikkelen in hun oorspronkelijke organen verminderde STK het aantal kankerstamcellen, verminderde de tumorlading en verlengde de overleving. In getransplanteerde tumormodellen, inclusief patiënt‑afgeleide tumoren gekweekt in gehumaniseerde muizen, remde STK opnieuw de groei met weinig schijnbare toxiciteit. Genetische experimenten bevestigden dat deze voordelen afhankelijk waren van SOAT1: wanneer SOAT1 al was uitgeschakeld in tumorcellen, gaf toevoeging van STK geen extra voordeel. Alles bij elkaar wijzen de gegevens op SOAT1 als een gemeenschappelijke metabole “checkpoint” die tumoren gebruiken om te gedijen en aan controle te ontsnappen.
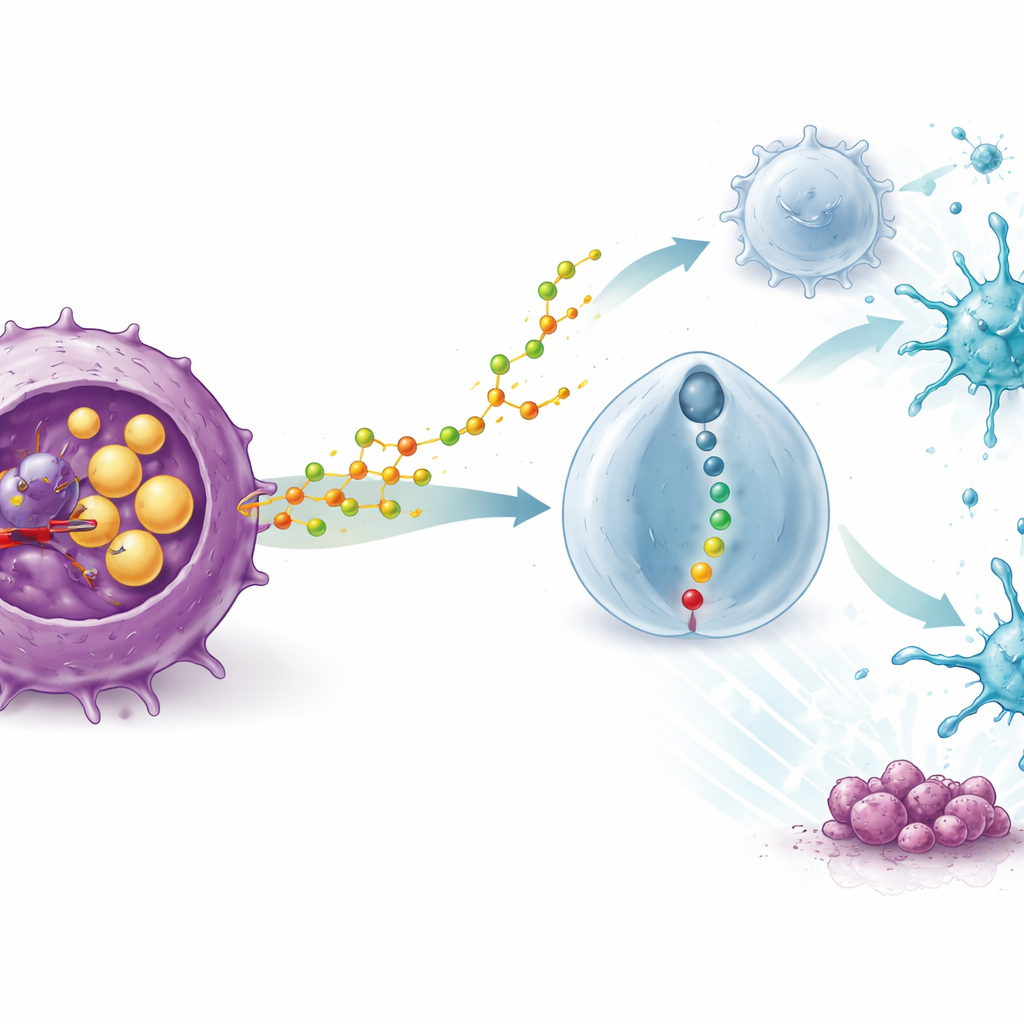
Hoe een cholesterolafbraakproduct immuuncellen herschakelt
De meest opvallende bevinding was dat STK’s effect afhankelijk was van een intact immuunsysteem. In immuundeficiënte muizen verloor het middel zijn antitumorale effect, en het blokkeren van T‑cellen wist de voordelen uit. Single‑cell RNA‑sequencing van tumormonsters liet zien dat STK‑behandeling tumoren overspoelde met behulpzame immuuncellen — vooral dendritische cellen die tumormateriaal presenteren en dodelijke CD8‑T‑cellen — terwijl het aantal en de kracht van regulatorische T‑cellen, of Tregs, sterk afnamen; deze Tregs fungeren normaal gesproken als remmen op immuunreacties. Mechanistische studies toonden waarom: het blokkeren van SOAT1 in tumorcellen zorgde ervoor dat ze meer van een specifiek geoxideerd cholesterolmolecuul vrijgaven, 20(S)‑hydroxycholesterol. Dit molecuul werd opgenomen door Tregs en activeerde een receptor op hun oppervlak genaamd GPR132, wat op zijn beurt een interne signaalcascade inschakelde. Toen dit pad werd geactiveerd, werden Tregs “fragiel”, produceerden ze minder suppressieve factoren en verloren ze hun greep op dendritische cellen en dodelijke T‑cellen.
Van koude tumoren naar hete doelwitten
Door Tregs op deze manier te verzwakken, herprogrammeerde STK effectief het tumor‑micro‑omgeving van een immuunsstilte, of “koude”, toestand naar een zeer actieve, “hete” toestand. Dendritische cellen rijpten en toonden meer activeringsmarkers, terwijl CD8‑T‑cellen hogere niveaus van moleculen produceerden die nodig zijn om kankercellen aan te vallen. Muizen die tumoren verwijderden na STK‑behandeling waren beter beschermd tegen een tweede tumoruitdaging, wat erop wijst dat een blijend immuungeheugen was gevormd. Cruciaal is dat het combineren van STK met bestaande checkpointtherapieën die PD‑1 of CTLA‑4 blokkeren de tumorcontrole in muismodellen verder verbeterde, wat suggereert dat SOAT1‑remming de reikwijdte en intensiteit van huidige immunotherapieën zou kunnen vergroten.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet‑specialisten komt de boodschap erop neer dat sommige kankers zich beschermen door te veranderen hoe ze cholesterol gebruiken, vooral binnen hun stamcelachtige kerncellen. Dit werk laat zien dat het uitschakelen van een sleutelenzym voor cholesterolopslag, SOAT1, niet alleen kankerstamcellen uithongert maar ze ook aanzet tot het vrijgeven van een chemisch alarmsignaal dat onderdrukkende T‑cellen ontwapent en de rest van het immuunleger mobiliseert. In muismodellen en vroege patiënt‑afgeleide tumoren maakt deze strategie meerdere kankertypen beter bestuurbaar en werkt ze bijzonder goed naast bestaande immunotherapie‑middelen. Hoewel nog veel tests nodig zijn voordat het breed bij mensen kan worden toegepast, biedt het richten op SOAT1 en de 20(S)‑hydroxycholesterol–GPR132‑route een veelbelovende nieuwe manier om de eigen verdediging van het lichaam betrouwbaarder tegen kanker in te zetten.
Bronvermelding: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
Trefwoorden: kankerimmunotherapie, kankerstamcellen, cholesterolmetabolisme, regulatorische T‑cellen, immuuncheckpointtherapie