Clear Sky Science · de
Hemmung des Krebs-Stammzell-Immunkontrollpunkts SOAT1 unterdrückt regulatorische T-Zell-Funktionen über einen transzellulären 20(S)-Hydroxycholesterin–GPR132-Weg bei Mäusen
Cancers Cholesterintricks gegen ihn selbst wenden
Die Krebstherapie wurde durch die Immuntherapie revolutioniert, doch viele Patientinnen und Patienten profitieren kaum, weil ihre Tumoren Wege finden, dem Immunsystem zu entgehen. Diese Studie enthüllt einen unerwarteten Komplizen in diesem Versteckspiel: ein cholesterinverarbeitendes Enzym in Krebsstammzellen. Durch Blockade dieses Enzyms mit einem neuen experimentellen Wirkstoff fanden die Forschenden einen Weg, die körpereigenen Abwehrkräfte zu reaktivieren und hartnäckige Tumoren bei Mäusen deutlich empfindlicher gegen Behandlung zu machen.
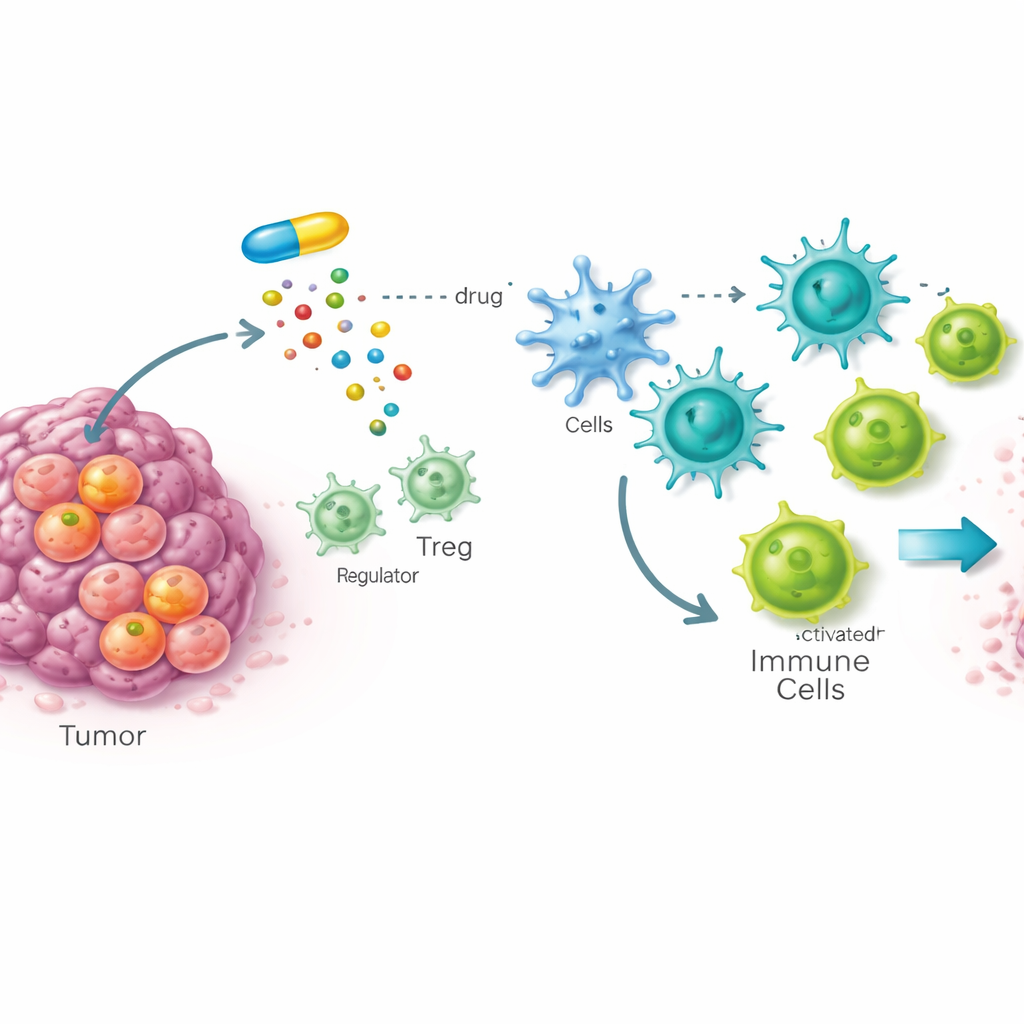
Eine verborgene Schwachstelle in Krebsstammzellen
Viele Tumoren werden von Krebsstammzellen angetrieben, einer kleinen Zellpopulation, die den Tumor regenerieren kann und oft therapieresistent ist. Das Team entwickelte ein Ganz-Tier-Wirkstoffscreening in Fruchtfliegen mit stamzellähnlichen Tumoren, um Verbindungen zu finden, die diese gefährlichen Zellen selektiv schädigen und normales Gewebe verschonen. Aus nahezu zehntausend Kandidaten stach eine Verbindung namens STK hervor. Nachfolgende Arbeiten an Maus- und menschlichen Krebszellen zeigten, dass STK mit hoher Spezifität an ein Enzym namens SOAT1 bindet, das hilft, überschüssiges Cholesterin in Speichertropfen zu verpacken. Wichtig ist, dass SOAT1 in Krebsstammzellen deutlich stärker exprimiert war als in normalen Zellen und mit fortgeschrittener Erkrankung sowie schlechterer Überlebensprognose in mehreren menschlichen Krebsarten assoziiert war.
Tumoren in vielen Krebsarten verlangsamen
Behandelten die Forschenden Mäuse mit STK, schrumpften Tumoren oder wuchsen deutlich langsamer in einer breiten Palette von Modellen, darunter Darm-, Leber-, Lungen-, Brust- und Hautkrebs. In genetisch veränderten Mäusen, die Tumoren in ihren Ursprungsorganen entwickeln, reduzierte STK die Zahl der Krebsstammzellen, verringerte die Tumorlast und verlängerte das Überleben. In transplantierten Tumormodellen, einschließlich patientenabgeleiteter Tumoren in humanisierten Mäusen, bremste STK ebenfalls das Wachstum bei gering ersichtlicher Toxizität. Genetische Experimente bestätigten, dass diese Effekte von SOAT1 abhingen: War SOAT1 in Tumorzellen bereits ausgeschaltet, brachte die Zugabe von STK keinen weiteren Vorteil. Insgesamt deuten die Daten darauf hin, dass SOAT1 ein gemeinsamer metabolischer „Checkpoint“ ist, den Tumoren zur Unterstützung und Immunflucht nutzen.
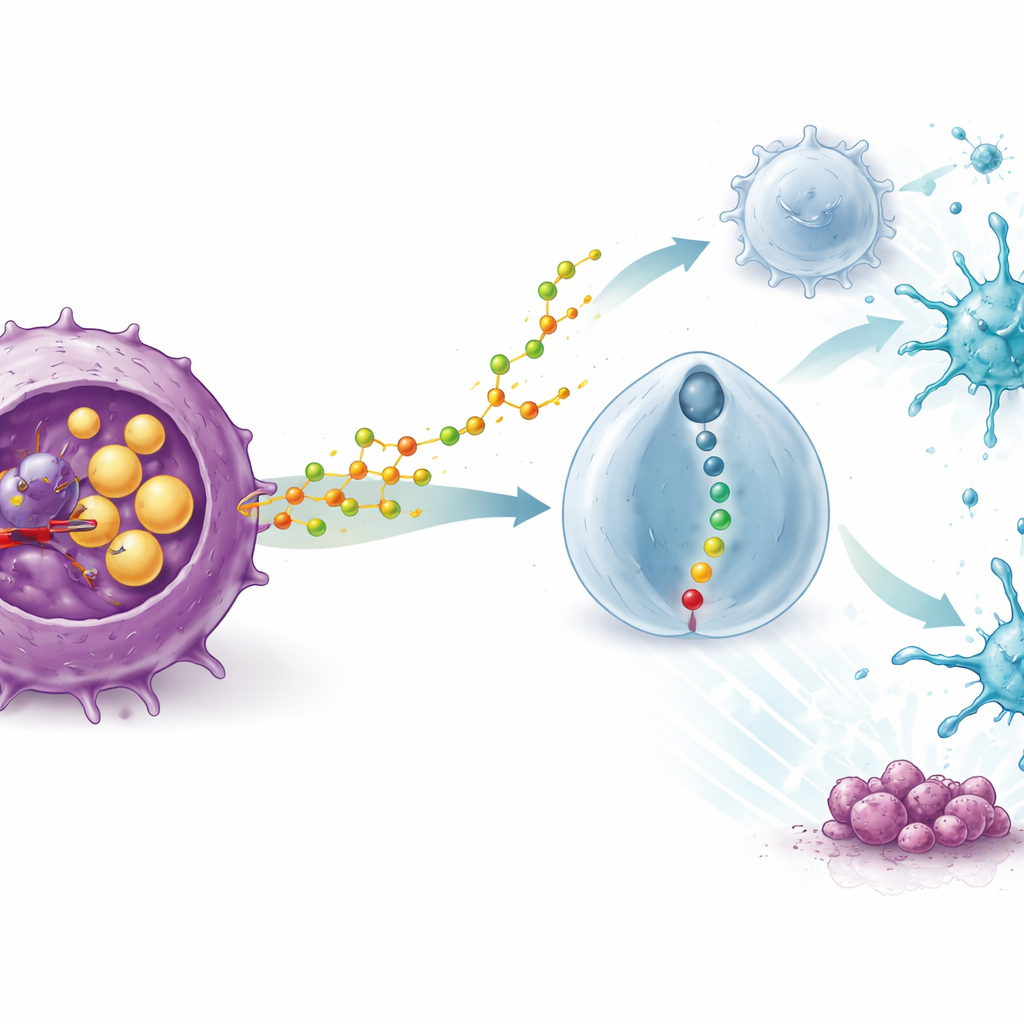
Wie ein Cholesterinabbauprodukt Immunzellen umprogrammiert
Die eindrücklichste Beobachtung war, dass STKs Wirkung auf ein intaktes Immunsystem angewiesen war. In immundefizienten Mäusen verlor der Wirkstoff seine anti-tumorale Wirkung, und die Blockade von T-Zellen beseitigte seinen Nutzen. Einzelzell-RNA-Sequenzierungen von Tumorproben zeigten, dass STK die Tumoren mit hilfreichen Immunzellen flutete – insbesondere mit dendritischen Zellen, die Tumormaterial präsentieren, und zytotoxischen CD8-T-Zellen – während es die Zahl und Aktivität regulatorischer T-Zellen (Tregs), die normalerweise als Bremse auf Immunantworten wirken, stark verringerte. Mechanistische Studien erklärten warum: Die Blockade von SOAT1 in Tumorzellen führte dazu, dass diese mehr eines spezifischen oxidierten Cholesterinmoleküls, 20(S)-Hydroxycholesterin, freisetzten. Dieses Molekül wurde von Tregs aufgenommen und aktivierte einen Rezeptor auf ihrer Oberfläche namens GPR132, der wiederum eine intrazelluläre Signalkette in Gang setzte. Mit Aktivierung dieses Wegs wurden Tregs „fragil“: Sie produzierten weniger suppressive Faktoren und verloren ihren Einfluss auf dendritische Zellen und zytotoxische T-Zellen.
Von kalten Tumoren zu heißen Zielen
Indem STK Tregs auf diese Weise schwächte, programmierte es die Tumormikroumgebung effektiv von einem immuninaktiven, „kalten“ Zustand in einen hochaktiven, „heißen“ Zustand um. Dendritische Zellen reiften und zeigten mehr Aktivierungsmarker, während CD8-T-Zellen höhere Mengen an Molekülen produzierten, die zum Angriff auf Krebszellen nötig sind. Mäuse, die Tumoren nach STK-Behandlung eliminiert hatten, waren besser gegen eine zweite Tumorherausforderung geschützt, was darauf hindeutet, dass eine anhaltende Immun‑Gedächtnisreaktion entstanden war. Entscheidend ist, dass die Kombination von STK mit bestehenden Checkpoint‑Therapien, die PD‑1 oder CTLA‑4 blockieren, die Tumorkontrolle in Mausmodellen weiter verbesserte, was nahelegt, dass die SOAT1‑Hemmung Antworten auf gegenwärtige Immuntherapien verbreitern und vertiefen könnte.
Was das für die künftige Krebsversorgung bedeuten könnte
Für Nicht‑Spezialisten lautet die Botschaft: Einige Tumoren schützen sich, indem sie die Nutzung von Cholesterin umgestalten, insbesondere in ihren stamzellähnlichen Kernzellen. Diese Arbeit zeigt, dass das Abschalten eines Schlüssel-Enzyms zur Cholesterinspeicherung, SOAT1, nicht nur Krebsstammzellen schwächt, sondern sie auch dazu bringt, ein chemisches Notsignal freizusetzen, das suppressive T‑Zellen entwaffnet und den Rest der Immunarmee mobilisiert. In Mausmodellen und frühen patientenabgeleiteten Tumoren macht diese Strategie mehrere Krebsarten besser kontrollierbar und wirkt besonders gut in Kombination mit bestehenden Immuntherapeutika. Zwar sind noch umfangreiche Tests nötig, bevor dies breit beim Menschen angewandt werden kann, doch das Anvisieren von SOAT1 und des 20(S)-Hydroxycholesterin–GPR132‑Wegs bietet einen vielversprechenden neuen Ansatz, die körpereigene Abwehr verlässlicher gegen Krebs zu richten.
Zitation: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
Schlüsselwörter: Krebsimmuntherapie, Krebsstammzellen, Cholesterinstoffwechsel, regulatorische T-Zellen, Immun-Checkpoint-Therapie