Clear Sky Science · sv
Hämning av cancerstamcells‑immunkontrollen SOAT1 dämpar regulatoriska T‑cellsfunktioner genom en trans‑cellulär 20(S)‑hydroxykolesterol‑GPR132‑väg i möss
Vända cancerns kolesterolknep emot den
Immunterapi har förändrat cancerbehandlingen, men många patienter får fortfarande liten nytta eftersom deras tumörer hittar sätt att gömma sig för immunsystemet. Denna studie avslöjar en oväntad medhjälpare i det spelet: ett kolesterolhanterande enzym inne i cancerstamceller. Genom att blockera detta enzym med ett nytt experimentellt läkemedel fann forskarna ett sätt att väcka kroppens försvar och göra envisa tumörer hos möss mycket mer sårbara för behandling.
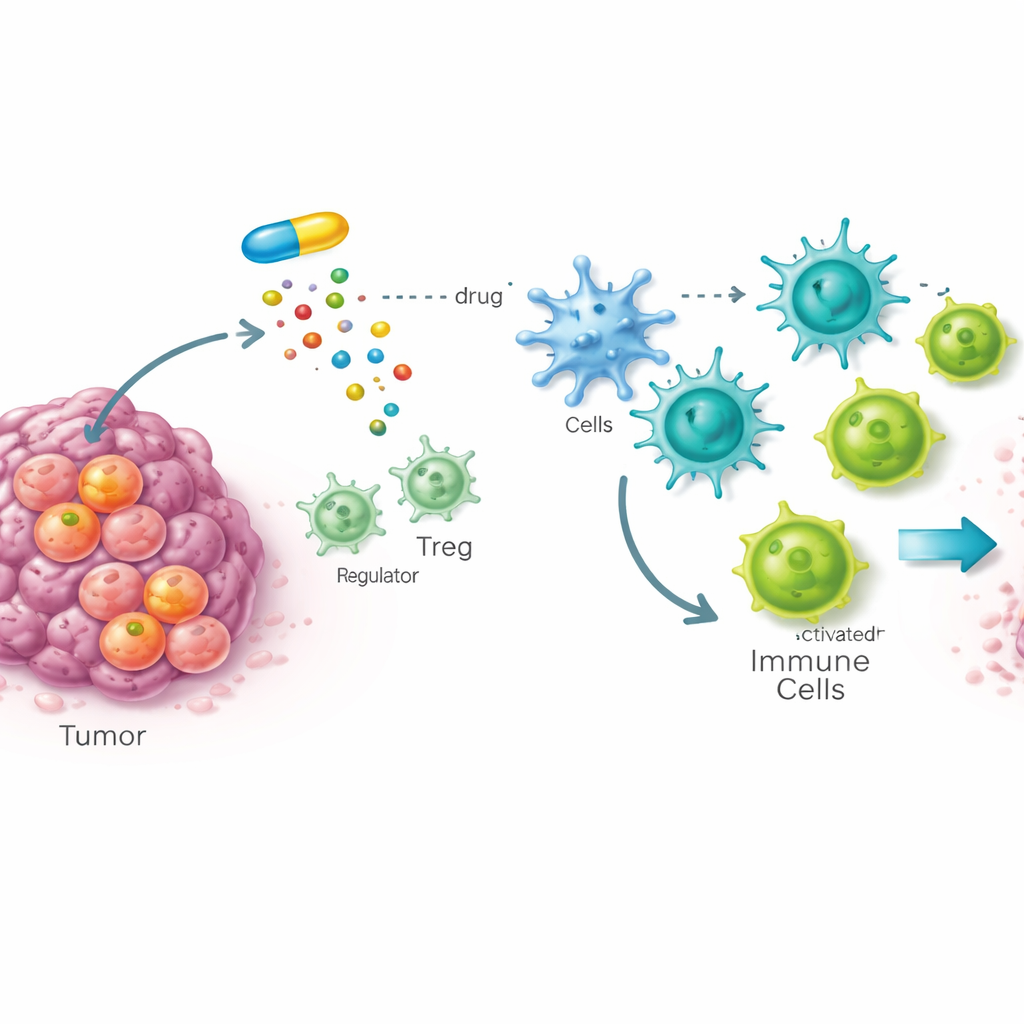
En dold svag punkt hos cancerstamceller
Många tumörer drivs av cancerstamceller, en liten cellgrupp som kan återbilda tumören och ofta motstå terapi. Forskarna byggde ett helorganism‑läkemedelsscreen i bananflugor med stamcells‑lika tumörer för att leta efter föreningar som selektivt skadar dessa farliga celler samtidigt som normal vävnad sparas. Av nästan tio tusen kandidater stack en förening, kallad STK, ut. Uppföljande arbete i mus‑ och humana cancerceller visade att STK binder tätt och specifikt till ett enzym som heter SOAT1, som hjälper till att paketera överskottskolesterol i lagringsdroppar. Viktigt är att SOAT1 visade sig vara mycket mer rikligt i cancerstamceller än i vanliga celler, och dess närvaro kopplades till avancerad sjukdom och sämre överlevnad i flera mänskliga cancerformer.
Fördröjning av tumörtillväxt över många cancerformer
När forskarna behandlade möss med STK krympte tumörer eller växte mycket långsammare i ett brett spektrum av modeller, inklusive tjocktarms‑, lever‑, lunga‑, bröst‑ och hudcancer. I genetiskt modifierade möss som utvecklar cancer i sina ursprungliga organ minskade STK antalet cancerstamceller, reducerade tumörbördan och förlängde överlevnaden. I transplanterade tumörmodeller, inklusive patient‑härledda tumörer som växte i humaniserade möss, begränsade STK återigen tillväxten med liten uppenbar toxicitet. Genetiska experiment bekräftade att dessa fördelar var beroende av SOAT1: när SOAT1 redan tystats i tumörceller gav tillägg av STK ingen ytterligare fördel. Sammantaget pekar data på SOAT1 som en gemensam metabolisk ”kontrollpunkt” som tumörer använder för att frodas och undkomma kontroll.
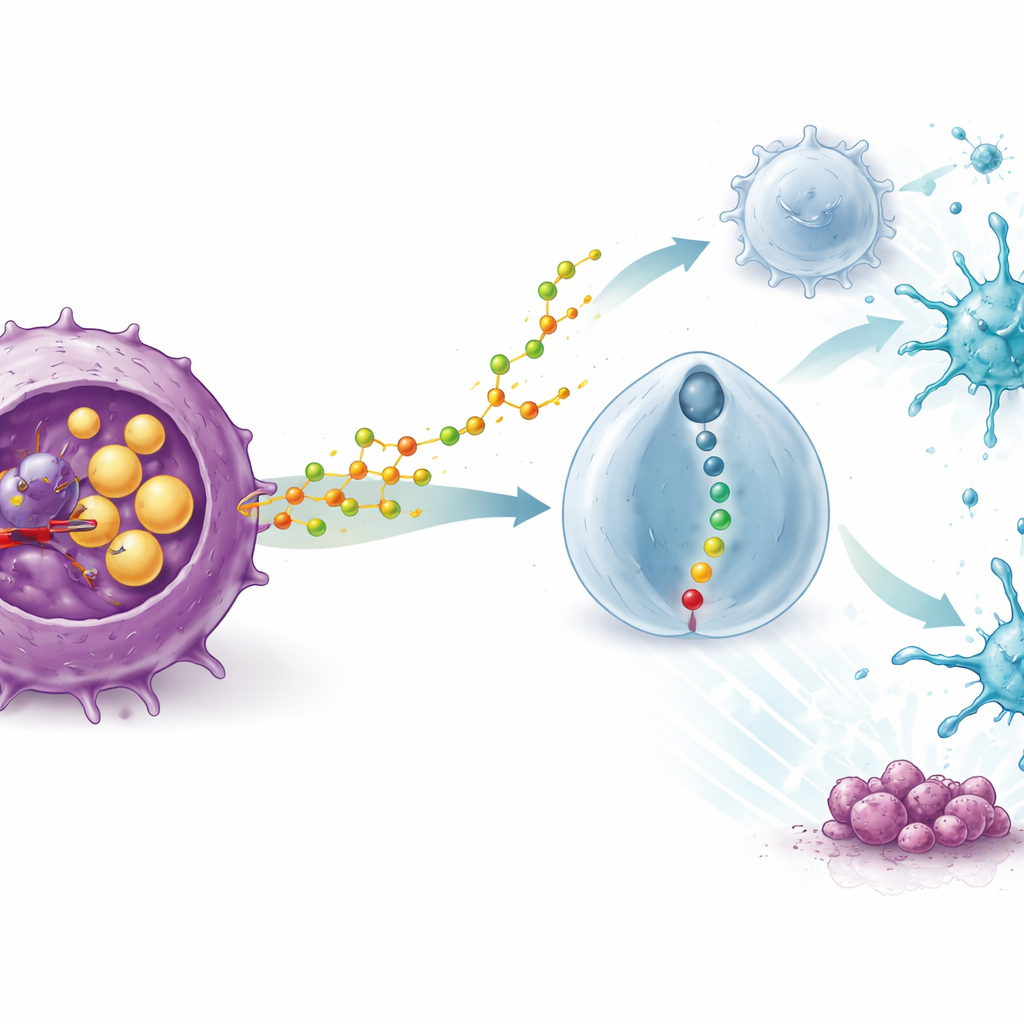
Hur en kolesterolbiprodukt omprogrammerar immunceller
Det mest slående fyndet var att STK:s effekt beroende av ett intakt immunsystem. I immundefekta möss förlorade läkemedlet sin antitumörkraft, och blockad av T‑celler utplånade dess fördelar. Enkelcells‑RNA‑sekvensering av tumörprover visade att STK‑behandling översvämmade tumörerna med hjälpsamma immunceller—särskilt dendritiska celler som presenterar tumörmaterial och cytotoxiska CD8‑T‑celler—samtidigt som antalet och styrkan hos regulatoriska T‑celler, eller Tregs, minskade kraftigt. Mekanistiska studier visade varför: blockad av SOAT1 i tumörceller fick dem att frisätta mer av en specifik oxiderad kolesterolmolekyl, 20(S)‑hydroxykolesterol. Denna molekyl togs upp av Tregs och aktiverade en receptor på deras yta kallad GPR132, vilket i sin tur slog på en intern signalväg. När denna väg aktiverades blev Tregs ”sköra”, producerade färre hämmande faktorer och förlorade sitt grepp om dendritiska celler och cytotoxiska T‑celler.
Från kalla tumörer till heta mål
Genom att försvaga Tregs på detta sätt omprogrammerade STK effektivt tumörmikromiljön från ett immunsilt eller ”kallt” tillstånd till ett mycket aktivt, ”hett” sådant. Dendritiska celler mognade och visade fler aktiveringsmarkörer, medan CD8‑T‑celler producerade högre nivåer av molekyler som krävs för att attackera cancerceller. Möss som rensade tumörer efter STK‑behandling var bättre skyddade mot en andra tumörutmaning, vilket tyder på att bestående immunologiskt minne hade bildats. Avgörande var att kombinera STK med befintliga kontrollpunktsterapier som blockerar PD‑1 eller CTLA‑4 ytterligare förbättrade tumörkontrollen i musmodeller, vilket antyder att SOAT1‑hämning kan bredda och fördjupa svaren på nuvarande immunterapier.
Vad detta kan innebära för framtida cancervård
För en icke‑specialist är budskapet att vissa cancerformer skyddar sig genom att omforma hur de använder kolesterol, särskilt inom sina stamcellsliknande kärnceller. Detta arbete visar att stänga ner ett nyckelenzym för kolesterol‑lagring, SOAT1, inte bara svälter cancerstamceller utan också får dem att släppa ett kemiskt nödsignal som avväpnar hämmande T‑celler och samlar resten av immunarmén. I musmodeller och tidiga patient‑härledda tumörer gör denna strategi flera cancertyper mer hanterbara och fungerar särskilt väl tillsammans med befintliga immunterapidroger. Mycket testande återstår innan det kan prövas brett på människor, men att rikta in sig på SOAT1 och 20(S)‑hydroxykolesterol–GPR132‑vägen erbjuder ett lovande nytt sätt att få kroppens egna försvar att mer tillförlitligt bekämpa cancer.
Citering: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
Nyckelord: cancerimmunterapi, cancerstamceller, kolesterolmetabolism, regulatoriska T‑celler, immunkontrollsterapi