Clear Sky Science · it
Inibizione del checkpoint immunitario delle cellule staminali tumorali SOAT1 sopprime le funzioni delle cellule T regolatorie tramite una via trans‑cellulare 20(S)-Idrossicoleterolo‑GPR132 nei topi
Usare i trucchi del colesterolo del cancro contro il tumore
Il trattamento del cancro è stato trasformato dall’immunoterapia, ma molti pazienti ottengono ancora pochi benefici perché i loro tumori trovano modi per nascondersi al sistema immunitario. Questo studio rivela un complice inaspettato in quel gioco di nascondino: un enzima che gestisce il colesterolo all’interno delle cellule staminali tumorali. Bloccando questo enzima con un nuovo farmaco sperimentale, i ricercatori hanno trovato un modo per risvegliare le difese dell’organismo e rendere tumori ostinati nei topi molto più vulnerabili al trattamento.
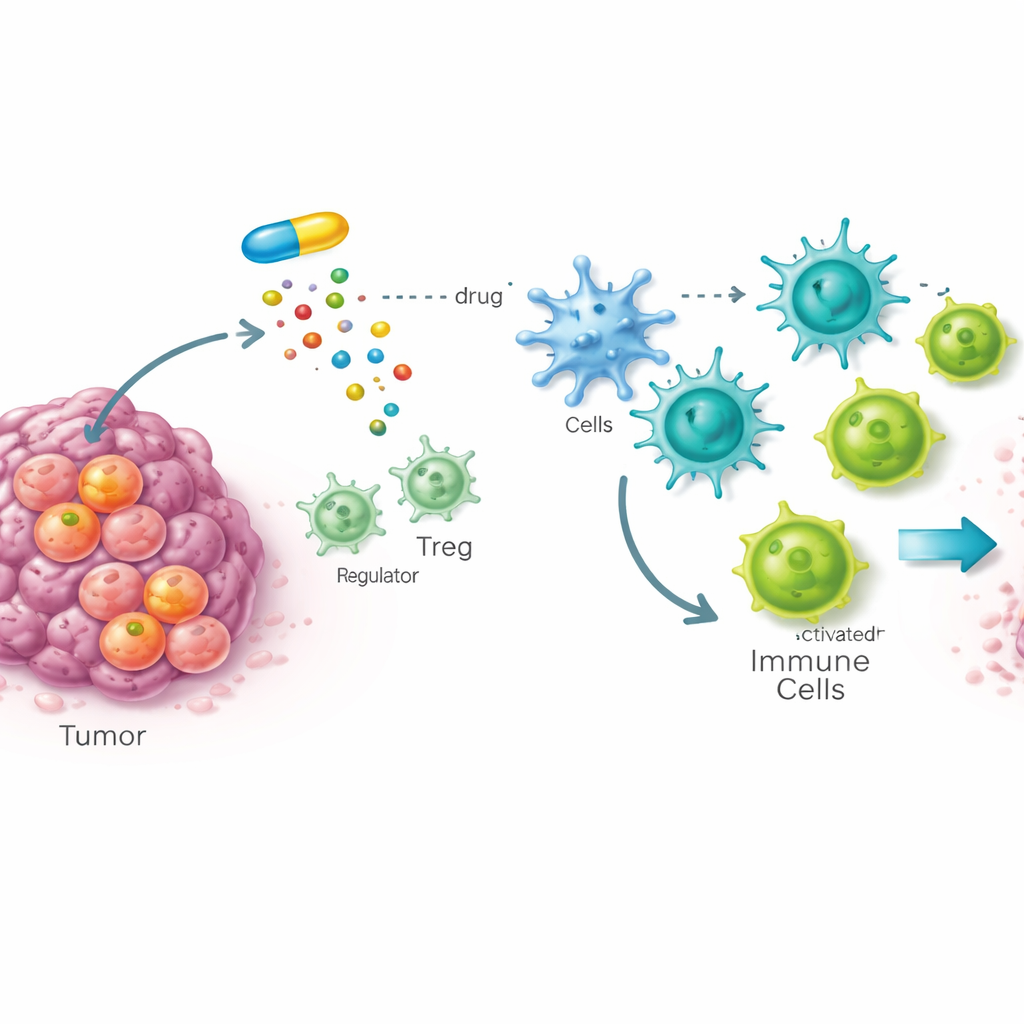
Un punto debole nascosto nelle cellule staminali tumorali
Molti tumori sono guidati da cellule staminali tumorali, un piccolo gruppo di cellule in grado di rigenerare il tumore e spesso resistenti alle terapie. Il gruppo ha messo a punto uno screening di farmaci sull’intero organismo usando mosche della frutta portatrici di tumori con caratteristiche simili alle cellule staminali per cercare composti che danneggino selettivamente queste cellule pericolose, risparmiando i tessuti normali. Tra quasi diecimila candidati, un composto chiamato STK è emerso chiaramente. Studi successivi su cellule tumorali di topo e umane hanno mostrato che STK si lega in modo forte e specifico a un enzima chiamato SOAT1, che aiuta a confezionare il colesterolo in eccesso in goccioline di deposito. È importante sottolineare che SOAT1 è risultato molto più abbondante nelle cellule staminali tumorali rispetto alle cellule ordinarie, e la sua presenza è stata associata a malattia avanzata e a una sopravvivenza peggiore in diversi tumori umani.
Rallentare i tumori in molti tipi di cancro
Quando i ricercatori hanno trattato i topi con STK, i tumori si sono ridotti o sono cresciuti molto più lentamente in un’ampia gamma di modelli, inclusi cancro del colon, del fegato, del polmone, della mammella e della pelle. In topi geneticamente modificati che sviluppano tumori nei loro organi d’origine, STK ha ridotto il numero di cellule staminali tumorali, diminuito il carico tumorale e prolungato la sopravvivenza. In modelli con tumori trapiantati, inclusi tumori derivati da pazienti cresciuti in topi umanizzati, STK ha nuovamente frenato la crescita con scarsa tossicità apparente. Esperimenti genetici hanno confermato che questi benefici dipendono da SOAT1: quando SOAT1 era già silenziato nelle cellule tumorali, l’aggiunta di STK non apportava vantaggi ulteriori. Complessivamente i dati indicano SOAT1 come un comune “checkpoint” metabolico che i tumori usano per prosperare ed eludere il controllo.
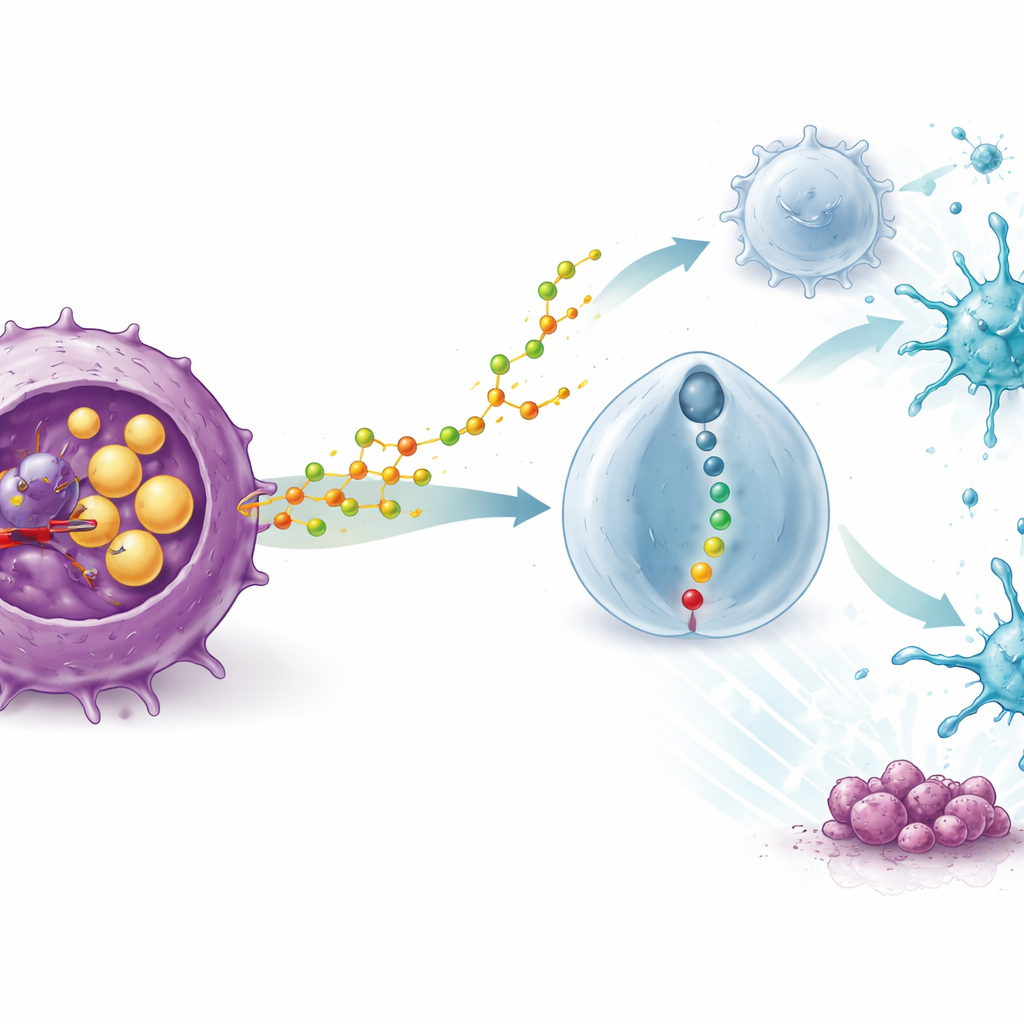
Come un prodotto del colesterolo riallinea le cellule immunitarie
La scoperta più sorprendente è stata che l’efficacia di STK dipende da un sistema immunitario integro. In topi immunodeficienti il farmaco perdeva il suo effetto antitumorale, e la deplezione delle cellule T annullava i benefici. Il sequenziamento dell’RNA a singola cellula dei campioni tumorali ha mostrato che il trattamento con STK ha inondato i tumori di cellule immunitarie utili — in particolare cellule dendritiche che presentano materiale tumorale e cellule T CD8 citotossiche — riducendo drasticamente numero e funzionalità delle cellule T regolatorie, o Treg, che normalmente agiscono come freni sulle risposte immunitarie. Studi meccanicistici hanno rivelato il perché: il blocco di SOAT1 nelle cellule tumorali le ha spinte a rilasciare più di una specifica molecola ossidata del colesterolo, il 20(S)-idrossicoleterolo. Questa molecola veniva captata dalle Treg e attivava un recettore sulla loro superficie chiamato GPR132, che a sua volta accendeva una catena di segnalazione interna. Con l’attivazione di questa via, le Treg diventavano “fragili”, producendo meno fattori soppressivi e perdendo la presa su cellule dendritiche e cellule T citotossiche.
Da tumori freddi a bersagli caldi
Indebolendo le Treg in questo modo, STK ha effettivamente riprogrammato il microambiente tumorale da uno stato immunologicamente silente, o “freddo”, a uno altamente attivo, o “caldo”. Le cellule dendritiche maturavano e mostravano più marcatori di attivazione, mentre le cellule T CD8 producevano livelli più elevati di molecole necessarie per attaccare le cellule tumorali. I topi che hanno eliminato i tumori dopo il trattamento con STK erano meglio protetti contro una seconda sfida tumorale, suggerendo la formazione di memoria immunitaria duratura. Crucialmente, la combinazione di STK con le terapie a checkpoint esistenti che bloccano PD‑1 o CTLA‑4 ha ulteriormente migliorato il controllo tumorale nei modelli murini, lasciando intendere che l’inibizione di SOAT1 potrebbe ampliare e potenziare le risposte alle immunoterapie correnti.
Cosa potrebbe significare per la cura del cancro in futuro
Per un non specialista, il messaggio è che alcuni tumori si proteggono rimodellando il modo in cui usano il colesterolo, soprattutto all’interno delle loro cellule centrali di tipo staminale. Questo lavoro mostra che spegnere un enzima chiave di deposito del colesterolo, SOAT1, non solo affama le cellule staminali tumorali ma le induce anche a rilasciare un segnale chimico di allarme che disarma le cellule T soppressive e raduna il resto dell’esercito immunitario. Nei modelli murini e nei primi tumori derivati da pazienti, questa strategia rende più controllabili diversi tipi di cancro e funziona particolarmente bene insieme ai farmaci immunoterapici esistenti. Pur richiedendo ancora molti test prima di poter essere applicata su larga scala nelle persone, mirare a SOAT1 e alla via 20(S)-idrossicoleterolo–GPR132 offre un nuovo e promettente modo per rendere le difese dell’organismo più efficaci contro il cancro.
Citazione: Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat Commun 17, 4102 (2026). https://doi.org/10.1038/s41467-026-69305-3
Parole chiave: immunoterapia del cancro, cellule staminali tumorali, metabolismo del colesterolo, cellule T regolatorie, terapia dei checkpoint immunitari