Clear Sky Science · zh
SOD1 乳酰化通过构象改变损害其酶活性并加剧椎间盘退变
为什么背痛来得如此之早
下背痛是全球致残的主要原因之一,而且往往在生命的早期就出现。在许多病例的核心,是位于脊椎之间的缓冲结构——椎间盘的缓慢退化。本研究揭示了椎间盘细胞内一种先前被忽视的化学变化,将一种常见的代谢副产物乳酸与这些脊柱减震器的早期衰老和功能失效联系起来——并指出了一种有针对性的潜在治疗策略。
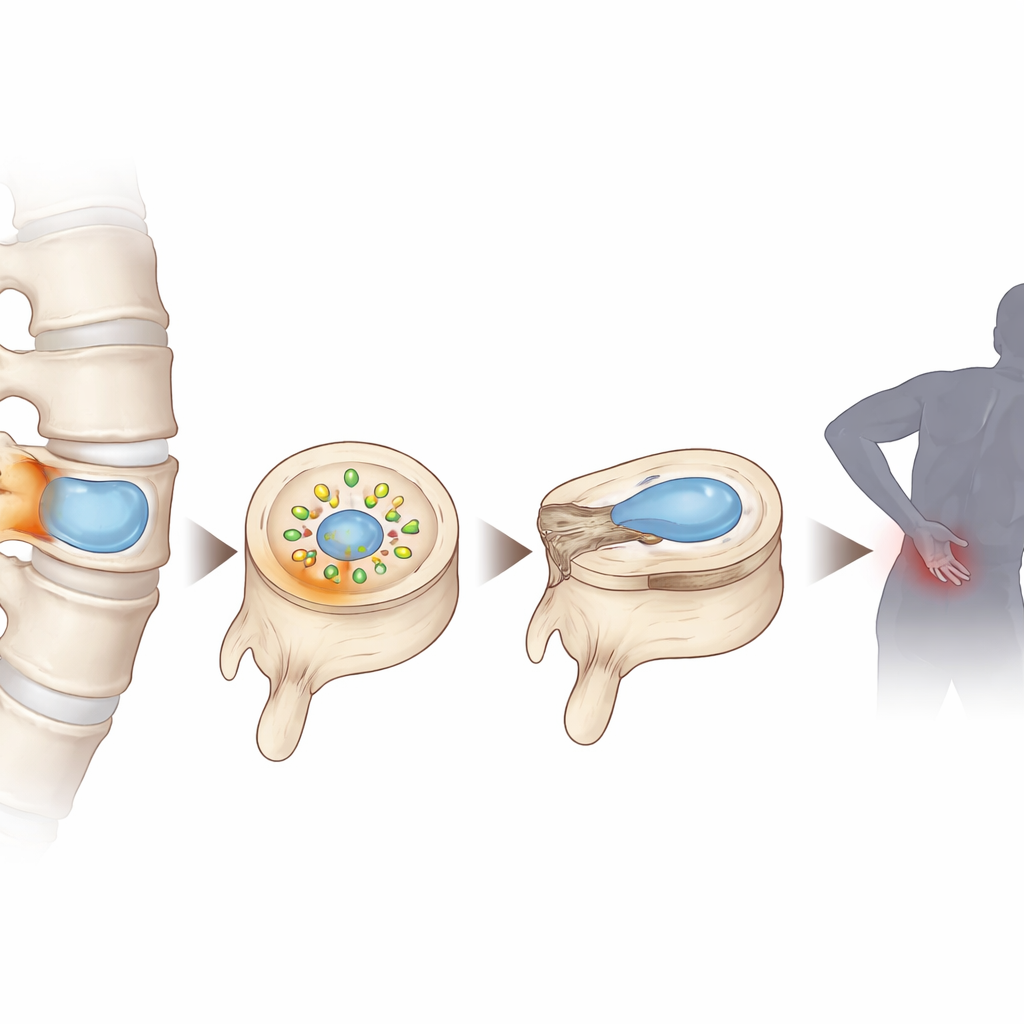
脊柱缓冲体内的隐秘世界
每个椎间盘都有一个柔软、凝胶状的中心称为髓核,它在低氧、低营养的环境中生存,因为几乎没有直接的血液供应。随着椎间盘退变,这种环境变得更加缺氧和缺乏营养,废物开始堆积。通过分析不同退变阶段的人体椎间盘组织,并结合先进的单细胞测序和代谢组学,研究人员发现乳酸——与剧烈运动时在肌肉中累积的相同分子——在受损椎间盘内升高到异常水平。他们还观察到,在这些条件下,椎间盘细胞出现氧化应激、DNA 损伤和过早细胞衰老的迹象。
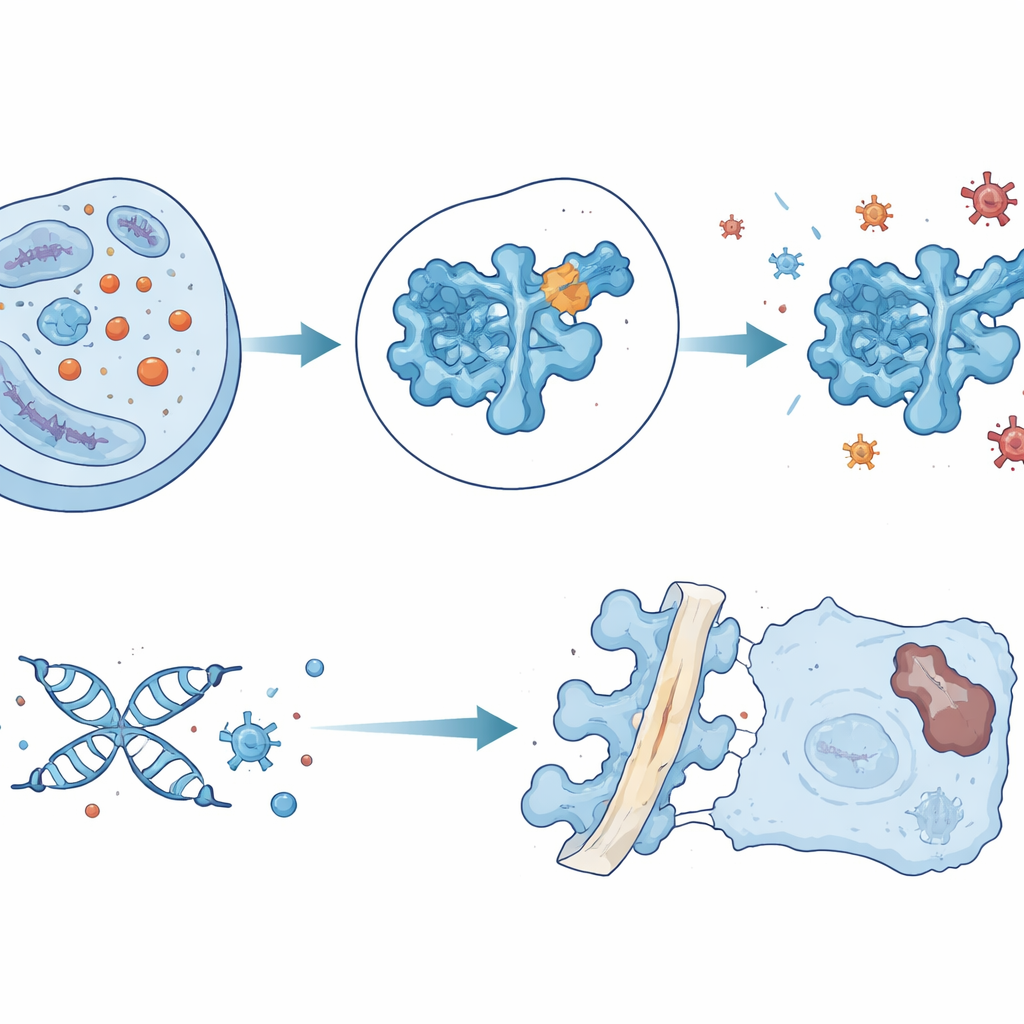
当乳酸开始重写蛋白质时
乳酸不仅仅是简单累积:它可以通过一种称为乳酰化的化学修饰改变蛋白质,在特定位点上附加一个来自乳酸的小标签。通过对大鼠椎间盘数千个蛋白片段进行“乳酰组”调查,团队绘制出这些标签在椎间盘退变过程中出现的位置。许多受影响的蛋白参与处理活性氧(ROS)——这些不稳定分子会损伤 DNA、脂质和蛋白质。其中一类酶,超氧化物歧化酶1(SOD1),格外引人注目。SOD1 通常中和一种高度活泼的氧形式,是椎间盘细胞内至关重要的抗氧化防御。在退变的椎间盘中,SOD1 上的一个特定位点——名为赖氨酸123的氨基酸——发生了大量乳酰化。
一个微小化学标签如何解除细胞盾牌
为了解这种修饰的作用,研究者构建了在赖氨酸123位置被替换为不能被乳酰化的氨基酸的椎间盘细胞和大鼠。这些“受保护”的 SOD1 即便在乳酸水平很高时仍保持酶活性,减轻了氧化应激,降低了 DNA 损伤和细胞衰老。在受损椎间盘的大鼠体内,携带不可乳酰化 SOD1 的动物在 MRI 和组织学分析中表现出较轻的椎间盘退变。对 SOD1 三维结构的计算机模拟给出了解释:位于123位的乳酰标签在铜含活性位点附近微妙地重塑了酶的表面,削弱了其与活性氧分子的相互作用并使整个蛋白更不稳定。
关闭损伤开关
这一结构改变的后果延伸到椎间盘细胞的基因调控系统。当 SOD1 被乳酰化削弱时,活性氧积聚并激活 p53 通路——细胞应激与衰老的核心调控器。细胞进入一种损伤锁定状态,不再正常功能并促成组织破坏。相比之下,在赖氨酸123位阻断乳酰化可以抑制 p53 的激活及其下游目标,有助于细胞维持氧化还原平衡并推迟退变改变。这表明 SOD1 的乳酰化是将代谢压力与椎间盘结构失效连接起来的关键分子开关。
一种精确药物递送的构想
基于这一洞见,团队在计算机中筛选了160万种小分子,寻找可结合 SOD1 易损赖氨酸123 疏水口袋附近的化合物。他们鉴定出一种名为 ZL-01 的分子,它能直接与该区域相互作用并减少 SOD1 的乳酰化,同时对其他常见蛋白修饰影响不大。在培养的椎间盘细胞中,ZL-01 恢复了 SOD1 活性,降低了氧化应激,并减少了 DNA 损伤和衰老标志物。注入受损大鼠椎间盘后,它延缓了退变,但该药物在组织中的清除较快。为提高滞留时间和靶向性,研究者将 ZL-01 装载到带有能强烈结合 II 型胶原肽的微小细胞外囊泡中。该递送系统延长了 ZL-01 在椎间盘内的滞留时间,进一步降低了 SOD1 乳酰化和氧化应激,并显著改善了动物的椎间盘结构和功能。
这对背痛患者意味着什么
综上,这项工作揭示了一条链式事件:在营养不足的椎间盘内乳酸累积化学性地解除了一种关键抗氧化酶 SOD1 的防护,从而触发氧化损伤、应激信号和加速的椎间盘退变。通过证明阻断单一乳酰化位点可以保护椎间盘细胞,并设计出一种有针对性的小分子来实现这一点,研究指向了这样一种未来:我们或许可以不用仅仅缓解症状或通过手术切除受损组织,而是直接纠正导致椎间盘过早磨损的底层分子错误,从而治疗背痛。
引用: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
关键词: 椎间盘退变, 乳酸, 蛋白质乳酰化, 氧化应激, SOD1