Clear Sky Science · nl
SOD1-lactylatie vermindert de enzymatische activiteit door conformationele verandering en verergert de tussenwervelschijfdegeneratie
Waarom rugpijn zo vroeg begint
Lagere rugpijn behoort wereldwijd tot de belangrijkste oorzaken van invaliditeit en begint vaak verrassend vroeg in het leven. In veel gevallen ligt de langzame afbraak van de schokdempers tussen onze wervels — de tussenwervelschijven — aan de basis. Deze studie onthult een eerder verborgen chemische verandering binnen schijfcellen die een veelvoorkomend metabool bijproduct, lactaat, koppelt aan het vroegtijdig verouderen en falen van deze wervelschokdempers — en wijst op een gerichte nieuwe behandelingsstrategie.
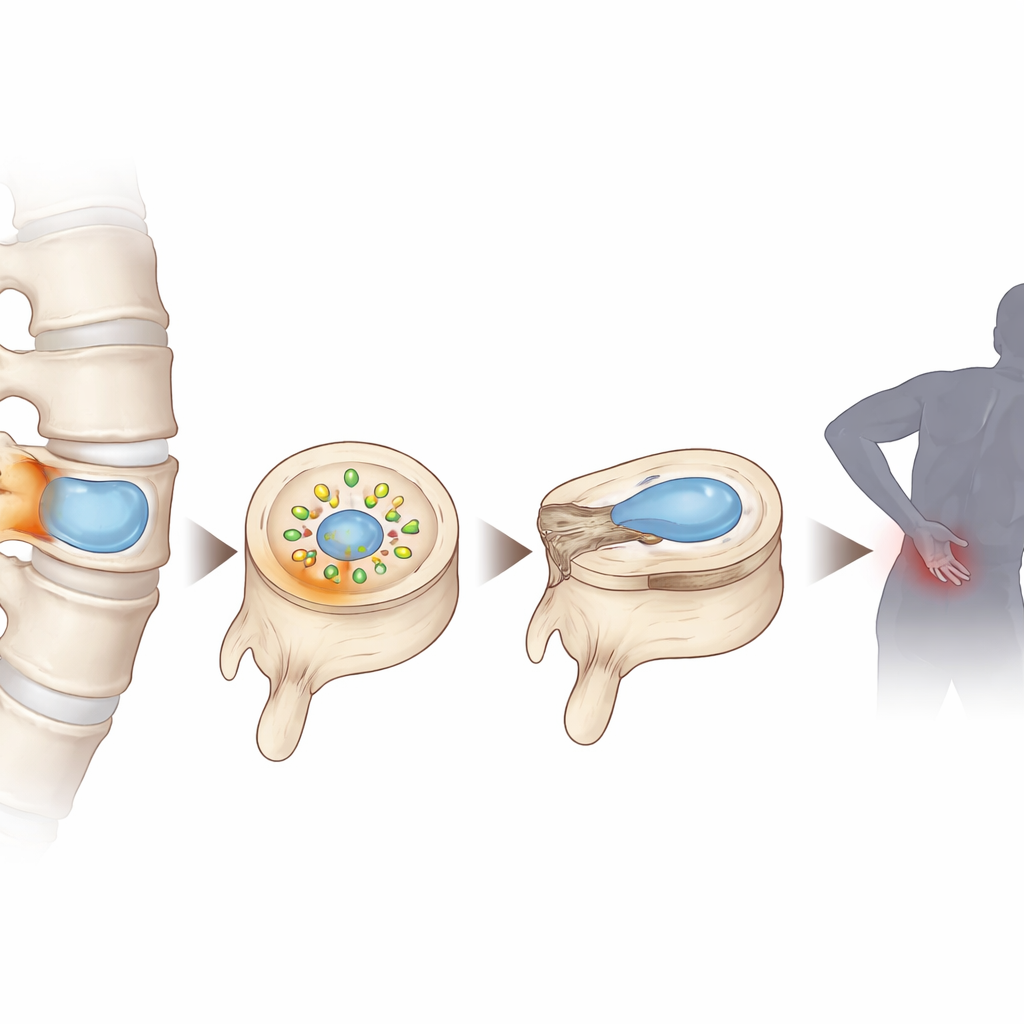
De verborgen wereld binnen wervelschijfkussentjes
Elke tussenwervelschijf heeft een zacht, gelachtig centrum dat nucleus pulposus heet en dat overleeft in een zuurstof- en voedingsstoffarme omgeving omdat het bijna geen directe bloedvoorziening heeft. Naarmate schijven degenereren, raakt deze omgeving nog schaarser aan zuurstof en voedingsstoffen, waardoor afvalstoffen zich ophopen. Door menselijk schijfweefsel in verschillende stadia van degeneratie te analyseren en geavanceerde single-cell sequencing en metabolomics te combineren, vonden de onderzoekers dat lactaat — dezelfde molecule die zich tijdens zware inspanning in spieren ophoopt — ongewoon hoge niveaus bereikt in beschadigde schijven. Ze zagen ook dat schijfcellen onder deze omstandigheden tekenen vertoonden van oxidatieve stress, DNA-schade en voortijdige cellulaire veroudering.
Wanneer lactaat eiwitten begint te herschrijven
Lactaat doet meer dan alleen ophopen: het kan eiwitten chemisch modificeren in een proces dat lactylatie heet, waarbij een klein, door lactaat afgeleid label aan specifieke plaatsen op eiwitten wordt gehecht. Met een "lactyloom"-onderzoek van duizenden eiwitfragmenten uit rattenwervelschijven bracht het team in kaart waar deze labels verschijnen tijdens schijfdegeneratie. Veel van de aangetaste eiwitten zijn betrokken bij de omgang met reactieve zuurstofsoorten — instabiele moleculen die DNA, vetten en eiwitten kunnen beschadigen. Eén enzym viel daarbij bijzonder op: superoxide dismutase 1 (SOD1). SOD1 neutraliseert normaal gesproken een zeer reactieve vorm van zuurstof en fungeert als een cruciale antioxidantverdediging binnen schijfcellen. In degenererende schijven werd een specifieke plaats op SOD1, het aminozuur lysine 123, sterk gelactyleerd.
Hoe een klein chemisch label een cellulaire schild ontwapent
Om te begrijpen wat deze modificatie doet, creëerden de onderzoekers schijfcellen en ratten waarbij lysine 123 was vervangen door een ander aminozuur dat niet gelactyleerd kan worden. Deze "beschermde" versies van SOD1 behielden hun enzymactiviteit zelfs bij hoge lactaatniveaus, verminderden oxidatieve stress en verminderden DNA-schade en cellulaire veroudering in schijfcellen. Bij levende ratten met schijfinfectie vertoonden dieren met het niet-lactyleerbare SOD1 mildere schijfdegeneratie op MRI en weefselanalyse. Computersimulaties van de 3D-structuur van SOD1 suggereerden waarom: het lactyllabel op positie 123 vervormt subtiel het oppervlak van het enzym nabij de koperhoudende actieve plaats, verzwakt de binding aan reactieve zuurstofmoleculen en maakt het hele eiwit minder stabiel.
Het uitschakelen van de schadeknop
De gevolgen van deze structurele aanpassing strekken zich uit tot de genetische controlesystemen van de schijfcel. Wanneer SOD1 door lactylatie verzwakt raakt, hoopt reactieve zuurstof zich op en activeert het het p53-pad, een centrale regulator van cellulaire stress en senescentie. Cellen raken in een schade-gefocuste staat, functioneren niet langer goed en dragen bij aan weefselafbraak. Daarentegen dempt het blokkeren van lactylatie op lysine 123 de activering van p53 en zijn downstream-doelen, waardoor cellen het redoxevenwicht beter behouden en degeneratieve veranderingen worden vertraagd. Dit positioneert SOD1-lactylatie als een belangrijke moleculaire schakelaar die metabole stress verbindt met structureel falen in tussenwervelschijven.
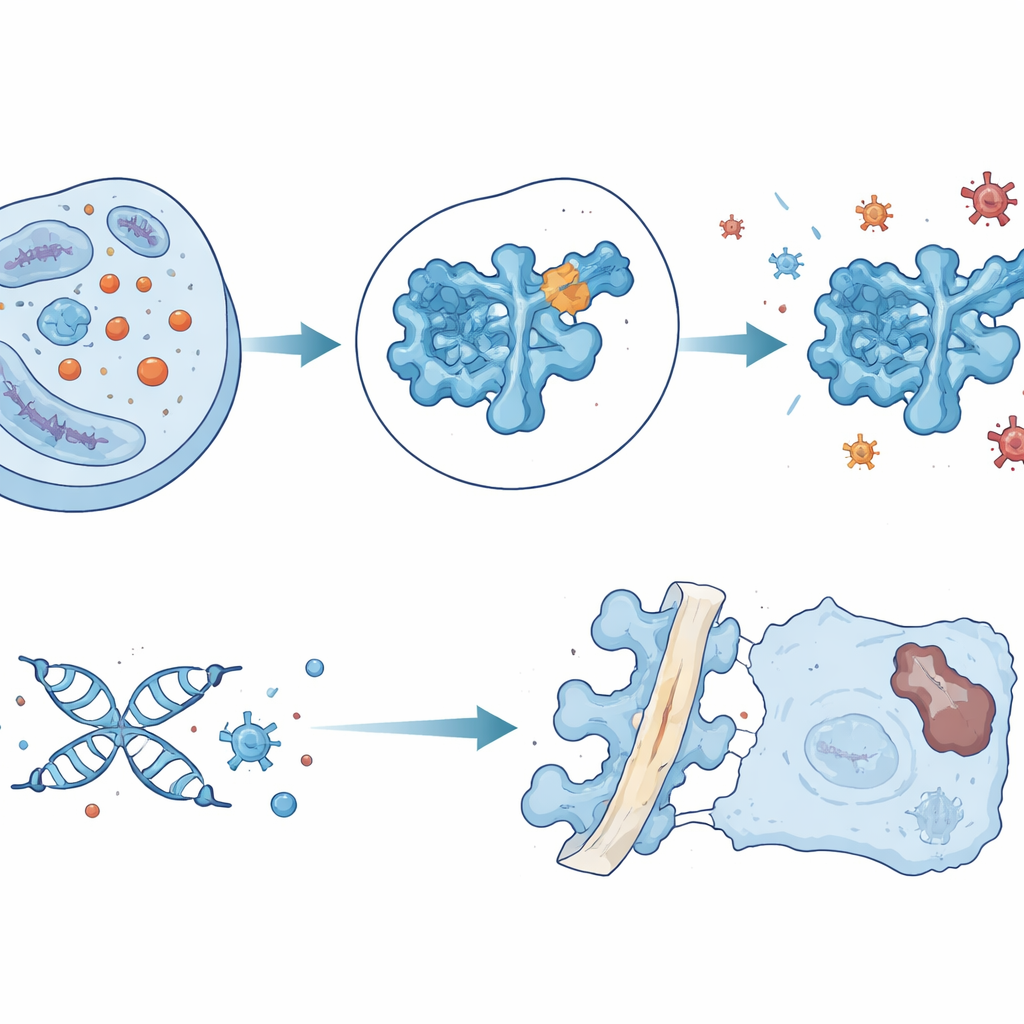
Een idee voor gerichte medicijnafgifte
Met deze inzichten doorzochten de onderzoekers in silico 1,6 miljoen kleine moleculen op verbindingen die nabij de kwetsbare lysine 123-pocket van SOD1 zouden binden. Ze identificeerden één stof, gedoopt ZL-01, die direct met dat gebied interageert en SOD1-lactylatie vermindert zonder andere veelvoorkomende eiwitmodificaties merkbaar te beïnvloeden. In gekweekte schijfcellen herstelde ZL-01 de SOD1-activiteit, verlaagde oxidatieve stress en verminderde markers van DNA-schade en senescentie. Geïnjecteerd in beschadigde rattschijven remde het de degeneratie, maar het middel werd snel uit het weefsel verwijderd. Om de verblijftijd en targeting te verbeteren, laadden de onderzoekers ZL-01 in kleine extracellulaire vesicles die waren ontworpen met een peptide dat sterk bindt aan collageen type II, een belangrijk bestanddeel van het schijfcentrum. Dit afgiftesysteem hield ZL-01 langer in de schijf, verminderde SOD1-lactylatie en oxidatieve stress verder, en verbeterde aanzienlijk de schijfstructuur en -functie bij de dieren.
Wat dit betekent voor mensen met rugpijn
Samengevat onthult het werk een keten van gebeurtenissen waarin lactaatophoping in slecht gevoede schijven een sleutel-antioxidantenzym, SOD1, chemisch ontwapent, wat oxidatieve schade, stresssignalisatie en versnelde schijfdegeneratie veroorzaakt. Door aan te tonen dat het blokkeren van één enkele lactylatieplaats schijfcellen kan beschermen en door een gerichte kleine molecule te ontwerpen die dat bewerkstelligt, wijst de studie op een toekomst waarin we rugpijn niet alleen behandelen door symptomen te verlichten of beschadigd weefsel chirurgisch te verwijderen, maar door de onderliggende moleculaire fouten die schijven te vroeg doen verslijten, direct te corrigeren.
Bronvermelding: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Trefwoorden: tussenwervelschijfdegeneratie, lactaat, eiwitlactylatie, oxidatieve stress, SOD1