Clear Sky Science · fr
La lactylation de SOD1 altère son activité enzymatique par un changement conformationnel et aggrave la dégénérescence des disques intervertébraux
Pourquoi le mal de dos commence si tôt
La lombalgie est l’une des principales causes d’incapacité dans le monde, et elle débute souvent étonnamment tôt dans la vie. Au cœur de nombreux cas se trouve la dégradation progressive des coussinets entre nos vertèbres, appelés disques intervertébraux. Cette étude met en lumière un changement chimique jusque-là caché à l’intérieur des cellules discales qui relie un sous-produit métabolique courant, le lactate, au vieillissement prématuré et à la défaillance de ces amortisseurs rachidiens — et suggère une stratégie thérapeutique ciblée.
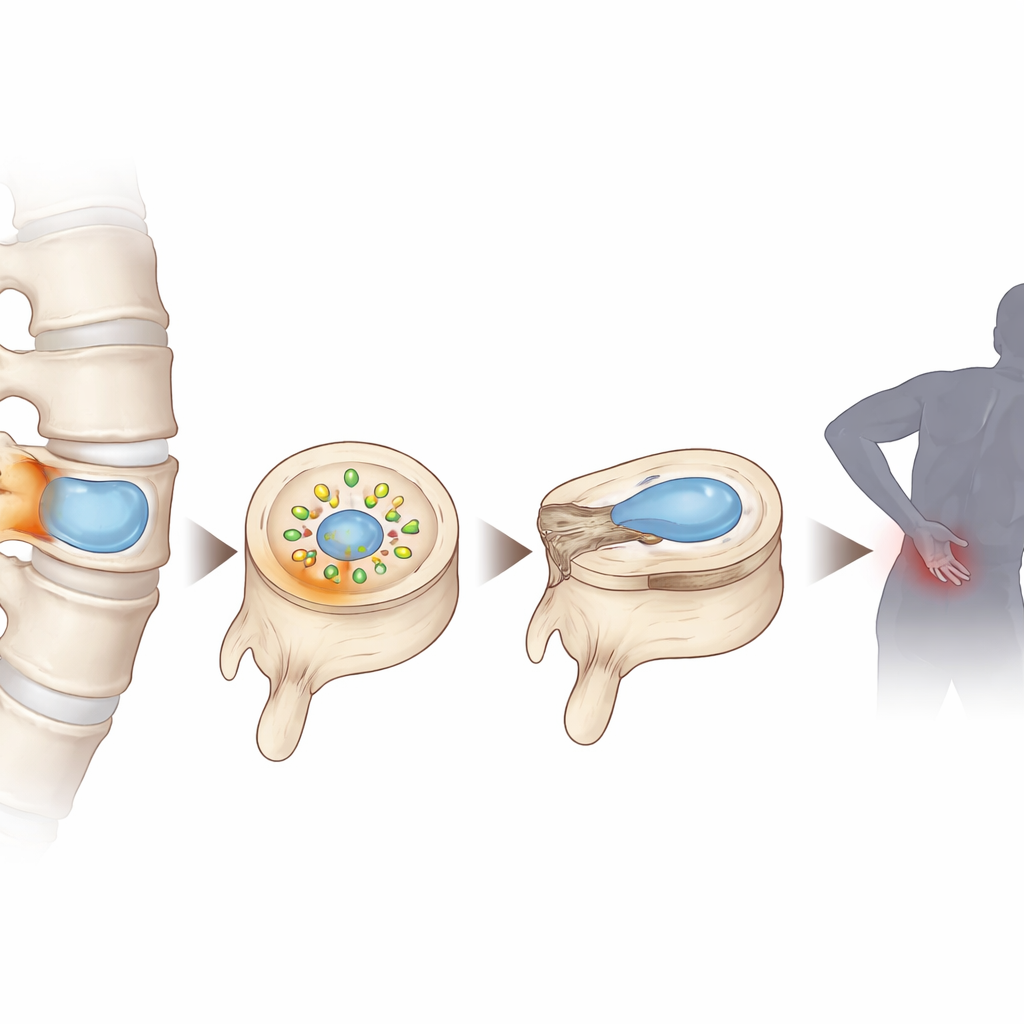
Le monde caché à l’intérieur des coussins spinaux
Chaque disque intervertébral possède un centre mou et gélatineux appelé noyau pulpeux, qui survit dans un environnement pauvre en oxygène et en nutriments car il bénéficie de très peu d’apport sanguin direct. À mesure que les disques se détériorent, cet environnement devient encore plus appauvri en oxygène et en nutriments, entraînant l’accumulation de déchets. En analysant des tissus discaux humains à différents stades de dégénérescence et en combinant des techniques avancées de séquençage unicellulaire et de métabolomique, les chercheurs ont constaté que le lactate — la même molécule qui s’accumule dans les muscles lors d’un exercice intense — atteint des niveaux exceptionnellement élevés à l’intérieur des disques endommagés. Ils ont également observé que les cellules discales dans ces conditions présentaient des signes de stress oxydatif, de dommages à l’ADN et de vieillissement cellulaire prématuré.
Quand le lactate commence à réécrire les protéines
Le lactate ne se contente pas de s’accumuler : il peut modifier chimiquement les protéines par un processus appelé lactylation, en ajoutant une petite étiquette dérivée du lactate à des sites spécifiques. À l’aide d’une analyse du « lactylome » sur des milliers de fragments protéiques issus de disques de rat, l’équipe a cartographié l’apparition de ces étiquettes pendant la dégénérescence discale. Beaucoup des protéines affectées participent à la gestion des espèces réactives de l’oxygène — des molécules instables qui peuvent endommager l’ADN, les lipides et les protéines. Une enzyme en particulier, la superoxyde dismutase 1 (SOD1), s’est distinguée. La SOD1 neutralise normalement une forme d’oxygène très réactive, constituant une défense antioxydante cruciale à l’intérieur des cellules discales. Dans les disques en dégénérescence, un site spécifique de la SOD1, un acide aminé appelé lysine 123, était fortement lactylé.
Comment une petite étiquette chimique désarme un bouclier cellulaire
Pour comprendre l’effet de cette modification, les chercheurs ont créé des cellules discales et des rats dans lesquels la lysine 123 avait été remplacée par un autre acide aminé incapable d’être lactylé. Ces versions « protégées » de la SOD1 ont conservé leur activité enzymatique même lorsque les taux de lactate étaient élevés, réduisant le stress oxydatif ainsi que les dommages à l’ADN et le vieillissement cellulaire. Chez des rats vivants soumis à une lésion discale, les animaux portant la SOD1 non lactylable présentaient une dégénérescence discale plus légère à l’IRM et à l’analyse tissulaire. Des simulations informatiques de la structure 3D de la SOD1 ont suggéré pourquoi : l’étiquette lactyl au niveau 123 remodèle subtilement la surface de l’enzyme près de son site actif contenant du cuivre, affaiblissant son interaction avec les molécules d’oxygène réactives et rendant l’ensemble de la protéine moins stable.
Éteindre l’interrupteur de la détérioration
Les conséquences de cette altération structurelle s’étendent aux systèmes de contrôle génétique de la cellule discale. Lorsque la SOD1 est affaiblie par la lactylation, les espèces réactives de l’oxygène s’accumulent et activent la voie p53, un régulateur central du stress cellulaire et du sénescence. Les cellules entrent dans un état verrouillé par les dommages, ne fonctionnent plus correctement et contribuent à la dégradation tissulaire. En revanche, bloquer la lactylation à la lysine 123 atténue l’activation de p53 et de ses cibles en aval, aidant les cellules à maintenir l’équilibre redox et à retarder les changements dégénératifs. Cela place la lactylation de la SOD1 comme un interrupteur moléculaire clé qui relie le stress métabolique à la défaillance structurelle des disques intervertébraux.
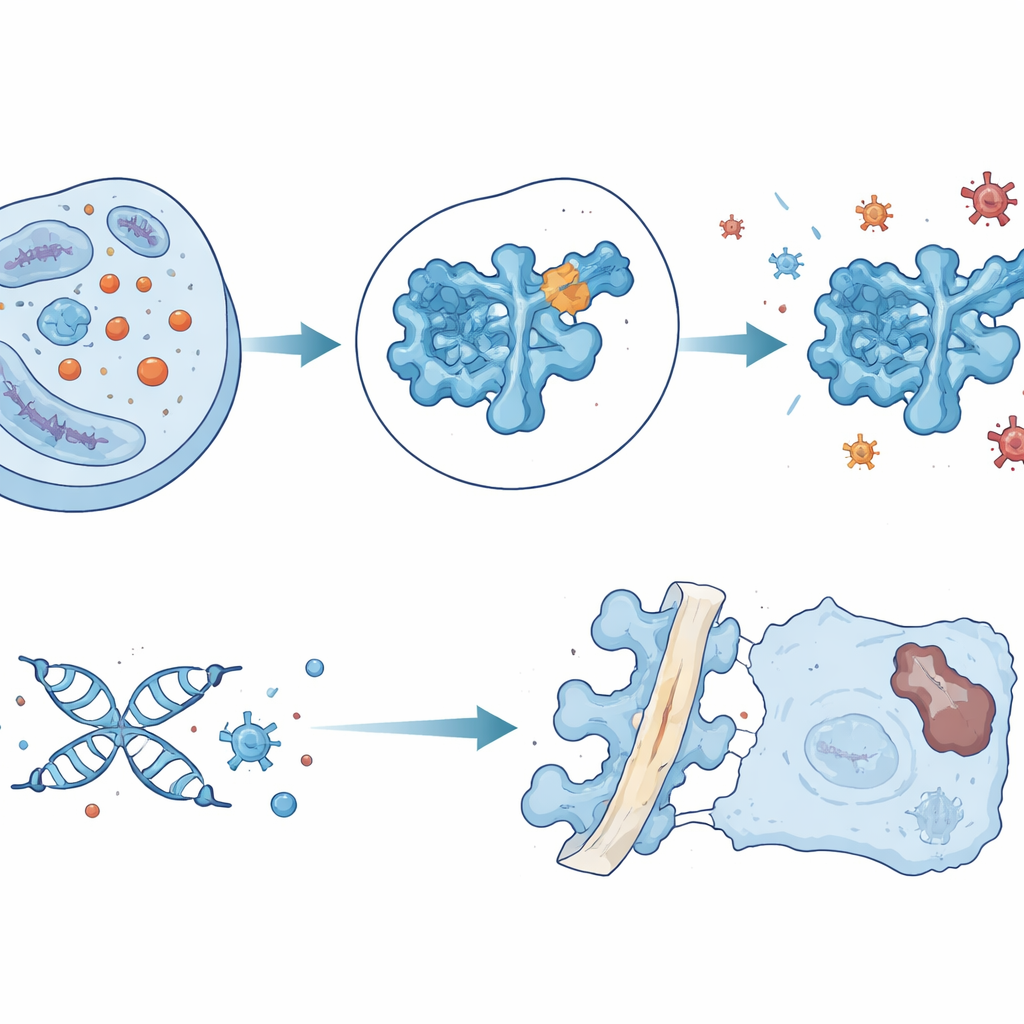
Une idée de délivrance médicamenteuse de précision
Munie de cette connaissance, l’équipe a scruté 1,6 million de petites molécules in silico pour trouver des composés susceptibles de se lier près de la poche vulnérable de la lysine 123 de la SOD1. Ils en ont identifié une, baptisée ZL-01, qui interagit directement avec cette région et réduit la lactylation de la SOD1 sans affecter de manière notable d’autres modifications protéiques courantes. En culture de cellules discales, ZL-01 a restauré l’activité de la SOD1, diminué le stress oxydatif et réduit les marqueurs de dommages à l’ADN et de sénescence. Injecté dans des disques de rats lésés, il a ralenti la dégénérescence, mais le médicament était rapidement éliminé du tissu. Pour augmenter sa durée d’action et son ciblage, les chercheurs ont chargé ZL-01 dans de minuscules vésicules extracellulaires conçues avec un peptide se liant fortement au collagène de type II, un composant majeur du centre discal. Ce système de délivrance a maintenu ZL-01 plus longtemps dans le disque, réduit encore la lactylation de la SOD1 et le stress oxydatif, et amélioré de manière significative la structure et la fonction discale chez les animaux.
Ce que cela signifie pour les personnes souffrant de maux de dos
Pris dans leur ensemble, ces travaux révèlent une chaîne d’événements dans laquelle l’accumulation de lactate à l’intérieur de disques mal nourris désarme chimiquement une enzyme antioxydante clé, la SOD1, déclenchant des dommages oxydatifs, une signalisation de stress et une dégénérescence discale accélérée. En montrant que le blocage d’un seul site de lactylation peut protéger les cellules discales et en concevant une petite molécule ciblée pour le faire, l’étude ouvre la voie à un avenir où l’on pourrait traiter le mal de dos non seulement en soulagant les symptômes ou en retirant chirurgicalement le tissu endommagé, mais en corrigeant directement les défaillances moléculaires sous-jacentes qui font que les disques s’usent trop tôt.
Citation: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Mots-clés: dégénérescence des disques intervertébraux, lactate, lactylation des protéines, stress oxydatif, SOD1