Clear Sky Science · it
La lattilazione di SOD1 ne compromette l’attività enzimatica tramite cambiamento conformazionale e aggrava la degenerazione del disco intervertebrale
Perché il mal di schiena inizia così presto
Il dolore lombare è una delle principali cause di disabilità nel mondo e spesso comincia sorprendentemente presto nella vita. Al centro di molti casi c’è il lento deterioramento degli ammortizzatori tra le vertebre, noti come dischi intervertebrali. Questo studio rivela un cambiamento chimico finora nascosto all’interno delle cellule del disco che collega un comune prodotto metabolico, il lattato, all’invecchiamento precoce e al fallimento di questi ammortizzatori spinali — e indica una strategia terapeutica mirata.
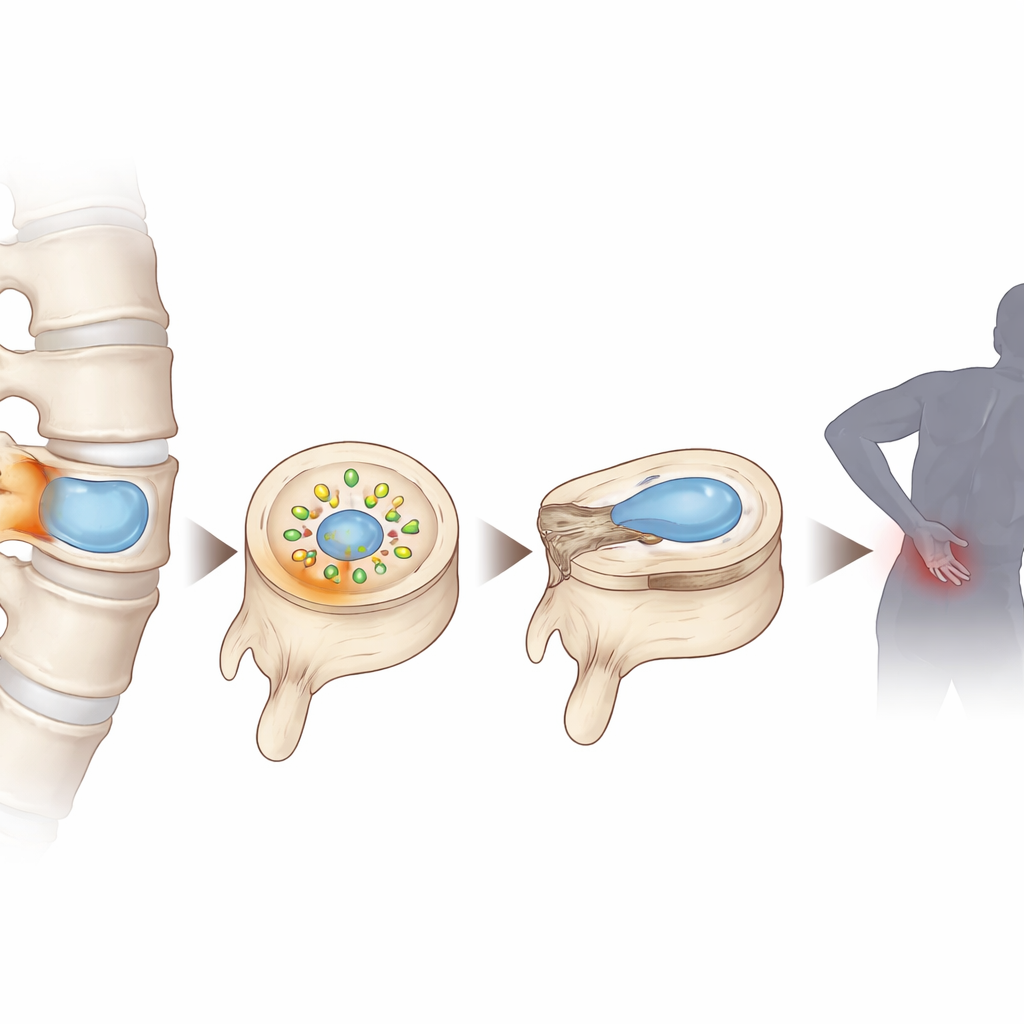
Il mondo nascosto all’interno degli ammortizzatori spinali
Ogni disco intervertebrale ha un centro morbido e gelatinoso chiamato nucleo polposo, che sopravvive in un ambiente a basso contenuto di ossigeno e nutrienti perché dispone di quasi nessun apporto diretto di sangue. Con la degenerazione, questo ambiente diventa ancora più povero di ossigeno e nutrienti, causando l’accumulo di prodotti di scarto. Analizzando tessuto umano di disco in differenti stadi di degenerazione e combinando sequenziamento cellulare avanzato a singola cellula e metabolomica, i ricercatori hanno scoperto che il lattato — lo stesso molecola che si accumula nei muscoli durante l’esercizio intenso — aumenta a livelli insolitamente elevati all’interno dei dischi danneggiati. Hanno inoltre osservato che le cellule discali in queste condizioni presentavano segni di stress ossidativo, danno al DNA e invecchiamento cellulare prematuro.
Quando il lattato comincia a riscrivere le proteine
Il lattato non si limita ad accumularsi: può modificare chimicamente le proteine in un processo chiamato lattilazione, attaccando un piccolo gruppo derivato dal lattato a siti specifici su di esse. Utilizzando un’indagine del “lattiloma” su migliaia di frammenti proteici provenienti da dischi di ratto, il team ha mappato dove compaiono questi marcatori durante la degenerazione del disco. Molte delle proteine interessate sono coinvolte nella gestione delle specie reattive dell’ossigeno — molecole instabili che possono danneggiare DNA, grassi e proteine. Un enzima in particolare, la superossido dismutasi 1 (SOD1), è emerso come significativo. SOD1 normalmente neutralizza una forma altamente reattiva dell’ossigeno, fungendo da difesa antiossidante cruciale nelle cellule del disco. Nei dischi in degenerazione, un sito specifico di SOD1, un amminoacido chiamato lisina 123, risultava fortemente lattilato.
Come un piccolo marcatore chimico disarma uno scudo cellulare
Per comprendere l’effetto di questa modifica, i ricercatori hanno creato cellule discali e ratti in cui la lisina 123 è stata sostituita con un altro amminoacido che non può essere lattilato. Queste versioni “protette” di SOD1 hanno mantenuto l’attività enzimatica anche con alti livelli di lattato, riducendo lo stress ossidativo e attenuando il danno al DNA e l’invecchiamento cellulare nelle cellule del disco. Nei ratti viventi sottoposti a lesione del disco, gli animali portatori della SOD1 non lattilabile mostravano una degenerazione discale più lieve all’analisi MRI e istologica. Simulazioni al computer della struttura 3D di SOD1 suggerivano il perché: il gruppo lattilico in posizione 123 rimodella sottilmente la superficie dell’enzima vicino al sito attivo contenente rame, indebolendo la sua capacità di trattenere le molecole di ossigeno reattive e rendendo l’intera proteina meno stabile.
Spegnere l’interruttore del danno
Le conseguenze di questo ritocco strutturale si estendono ai sistemi di controllo genetico della cellula del disco. Quando SOD1 è indebolita dalla lattilazione, le specie reattive dell’ossigeno si accumulano e attivano la via di p53, un regolatore centrale dello stress cellulare e della senescenza. Le cellule entrano in uno stato di danno bloccato, non funzionano più correttamente e contribuiscono alla degradazione del tessuto. Al contrario, bloccare la lattilazione sulla lisina 123 attenua l’attivazione di p53 e dei suoi bersagli a valle, aiutando le cellule a mantenere l’equilibrio redox e a ritardare i cambiamenti degenerativi. Questo pone la lattilazione di SOD1 come un interruttore molecolare chiave che collega lo stress metabolico al cedimento strutturale nei dischi intervertebrali.
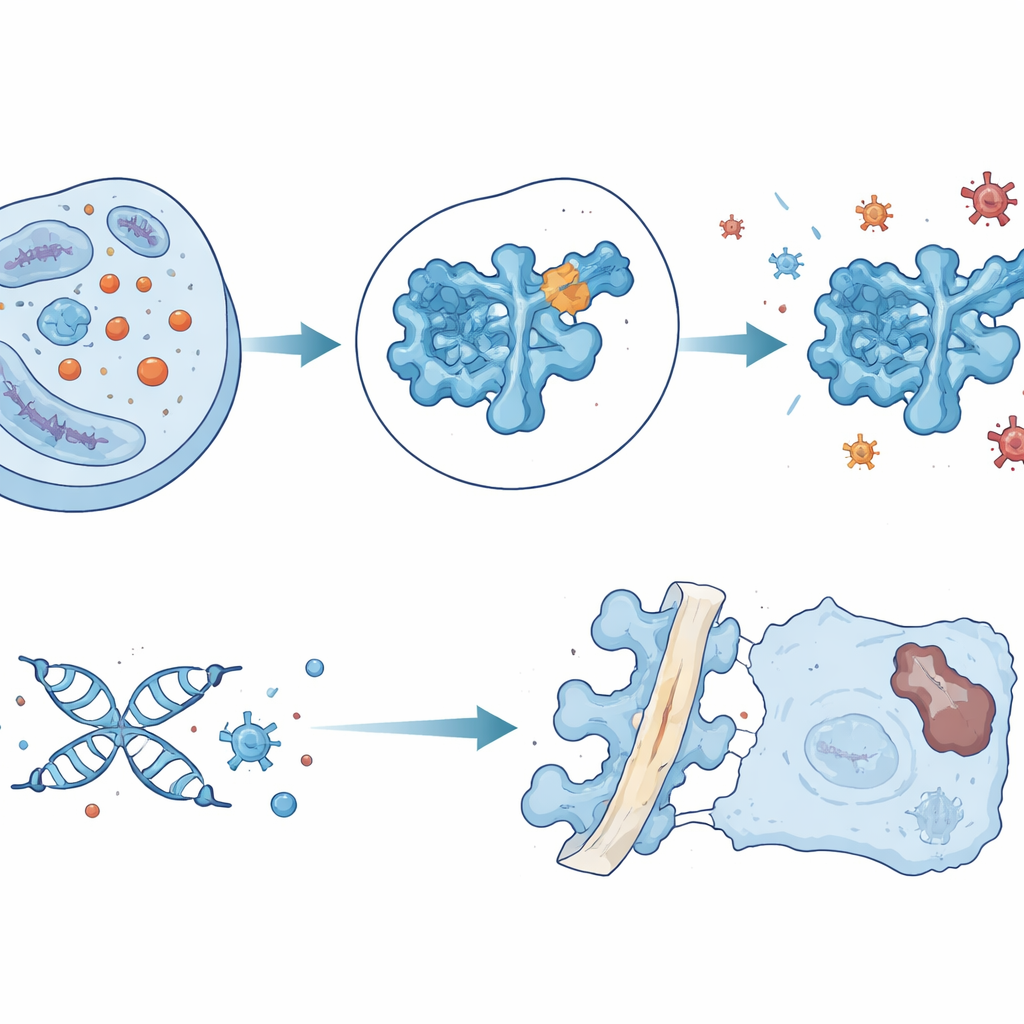
Un’idea per una somministrazione farmacologica di precisione
Con questa intuizione, il team ha cercato in silico tra 1,6 milioni di piccole molecole composti che si legherebbero vicino alla tasca vulnerabile della lisina 123 di SOD1. Hanno identificato una molecola, chiamata ZL-01, che interagisce direttamente con quella regione e riduce la lattilazione di SOD1 senza influenzare in modo evidente altre modificazioni proteiche comuni. In cellule discali coltivate, ZL-01 ha ripristinato l’attività di SOD1, ridotto lo stress ossidativo e diminuito i marcatori di danno al DNA e senescenza. Iniettato nei dischi lesi di ratti, ha rallentato la degenerazione, ma il farmaco veniva rapidamente eliminato dal tessuto. Per aumentarne la persistenza e il targeting, i ricercatori hanno caricato ZL-01 in piccole vescicole extracellulari ingegnerizzate con un peptide che si lega fortemente al collagene di tipo II, un componente principale del centro del disco. Questo sistema di somministrazione ha mantenuto ZL-01 nel disco più a lungo, ridotto ulteriormente la lattilazione di SOD1 e lo stress ossidativo, e migliorato significativamente struttura e funzione del disco negli animali.
Cosa significa per le persone con mal di schiena
Nel complesso, il lavoro rivela una catena di eventi in cui l’accumulo di lattato all’interno di dischi mal nutriti disarma chimicamente un enzima antiossidante chiave, SOD1, innescando danni ossidativi, segnalazione di stress e accelerazione della degenerazione discale. Mostrando che bloccare un singolo sito di lattilazione può proteggere le cellule del disco e progettando una piccola molecola mirata per farlo, lo studio indica un futuro in cui potremmo trattare il mal di schiena non solo alleviando i sintomi o rimuovendo chirurgicamente il tessuto danneggiato, ma correggendo direttamente gli errori molecolari che portano all’usura precoce dei dischi.
Citazione: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Parole chiave: degenerazione del disco intervertebrale, lattato, lattilazione delle proteine, stress ossidativo, SOD1