Clear Sky Science · pl
Laktylacja SOD1 upośledza jego aktywność enzymatyczną przez zmianę konformacyjną, zaostrzając zwyrodnienie krążków międzykręgowych
Dlaczego ból pleców zaczyna się tak wcześnie
Ból dolnej części pleców jest jedną z głównych przyczyn niepełnosprawności na świecie i często pojawia się zaskakująco wcześnie w życiu. U podstaw wielu przypadków leży powolny rozpad amortyzatorów między kręgami, znanych jako krążki międzykręgowe. Badanie ujawnia wcześniej ukrytą zmianę chemiczną w komórkach krążków, która łączy powszechny produkt uboczny metabolizmu — mleczan — z przedwczesnym starzeniem się i niewydolnością tych struktur — i wskazuje na ukierunkowaną strategię terapeutyczną.
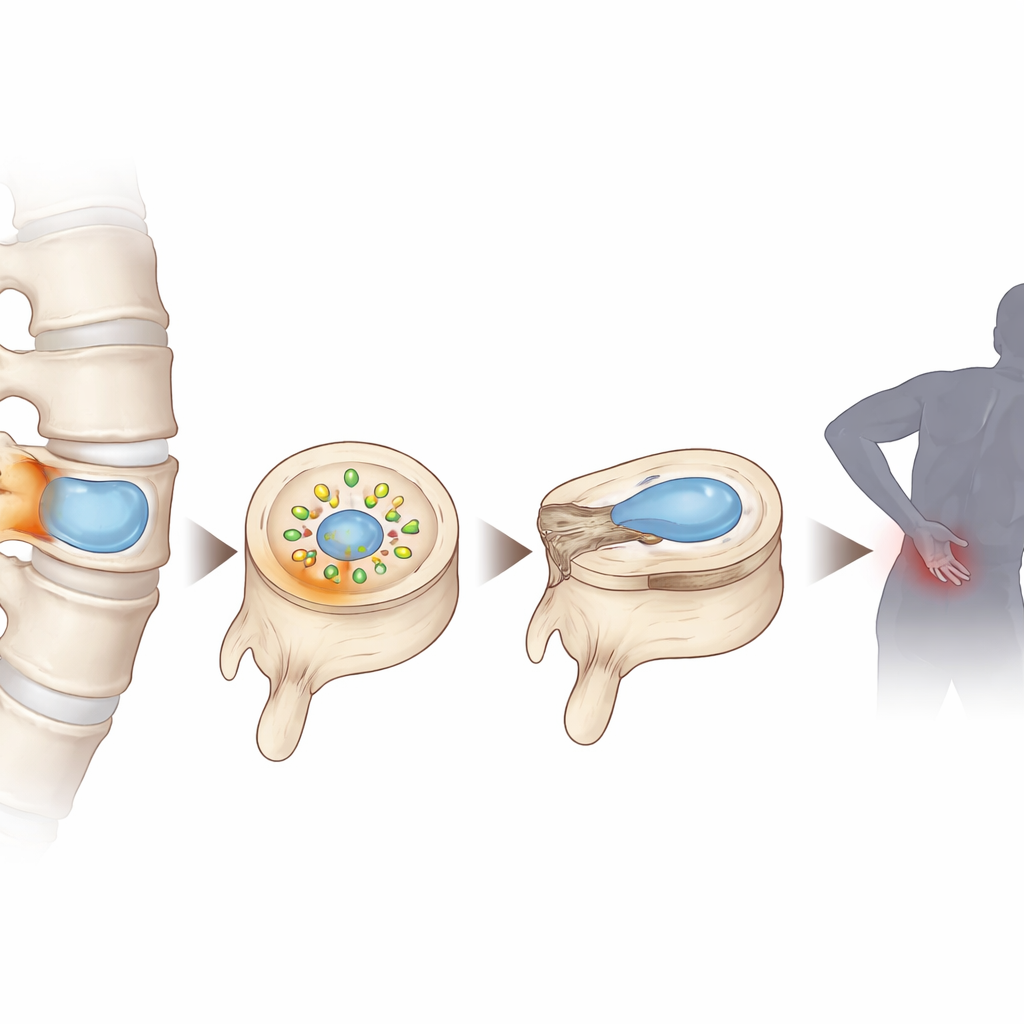
Ukryty świat wewnątrz krążków międzykręgowych
Każdy krążek ma miękkie, żelopodobne jądro miażdżyste, które funkcjonuje w warunkach niskiego stężenia tlenu i składników odżywczych, ponieważ niemal nie ma bezpośredniego unaczynienia. W miarę jak krążki się degenerują, środowisko to staje się jeszcze bardziej pozbawione tlenu i substancji odżywczych, co powoduje gromadzenie się produktów przemiany materii. Analiza ludzkiej tkanki krążków na różnych etapach zwyrodnienia przy użyciu zaawansowanego sekwencjonowania pojedynczych komórek i metabolomiki wykazała, że mleczan — ta sama cząsteczka, która gromadzi się w mięśniach podczas intensywnego wysiłku — osiąga wyjątkowo wysokie stężenia w uszkodzonych krążkach. Zaobserwowano również, że komórki krążków w takich warunkach wykazują oznaki stresu oksydacyjnego, uszkodzeń DNA i przedwczesnego starzenia komórkowego.
Kiedy mleczan zaczyna przepisywać białka
Mleczan robi więcej niż tylko się kumuluje: może chemicznie modyfikować białka w procesie zwanym laktylacją, przyłączając małą grupę pochodzącą od mleczanu do określonych miejsc na białkach. W badaniu „laktylomu” obejmującym tysiące fragmentów białek z krążków szczurów zespół sporządził mapę występowania tych znaczników podczas degeneracji. Wiele dotkniętych białek bierze udział w neutralizowaniu reaktywnych form tlenu — niestabilnych cząsteczek, które mogą uszkadzać DNA, lipidy i białka. Szczególnie wyróżnił się jeden enzym, dysmutaza ponadtlenkowa 1 (SOD1). SOD1 normalnie neutralizuje wysoce reaktywną formę tlenu, działając jako kluczowa obrona antyoksydacyjna w komórkach krążków. W degenerujących krążkach konkretne miejsce na SOD1 — aminokwas lizyna 123 — stało się silnie laktylowane.
Jak drobny chemiczny znacznik rozbraja komórkową tarczę
Aby zrozumieć, co ta modyfikacja powoduje, badacze stworzyli komórki krążków i szczury, w których lizyna 123 została zastąpiona innym aminokwasem, który nie może być laktylowany. Te „chronione” wersje SOD1 zachowały aktywność enzymatyczną nawet przy wysokich poziomach mleczanu, zmniejszały stres oksydacyjny oraz ograniczały uszkodzenia DNA i starzenie się komórek krążków. U żywych szczurów poddanych urazowi krążka zwierzęta niosące nielaktylowalną wersję SOD1 wykazywały łagodniejsze zmiany zwyrodnieniowe w badaniach MRI i analizie tkankowej. Symulacje komputerowe trójwymiarowej struktury SOD1 zasugerowały, dlaczego: grupa laktylowa na pozycji 123 subtelnie przekształca powierzchnię enzymu w pobliżu miedzianego centrum aktywnego, osłabiając jego zdolność wiązania reaktywnych form tlenu i zmniejszając ogólną stabilność białka.
Wyłączanie przełącznika uszkodzeń
Konsekwencje tej zmiany strukturalnej sięgają układów kontroli genetycznej komórki krążka. Gdy SOD1 jest osłabiony przez laktylację, reaktywne formy tlenu kumulują się i aktywują szlak p53, centralnego regulatora stresu komórkowego i senescencji. Komórki wchodzą w stan zablokowanego uszkodzenia, przestają prawidłowo funkcjonować i przyczyniają się do rozpadu tkanki. Przeciwnie, blokowanie laktylacji w lizynie 123 tłumi aktywację p53 i jej cele pośrednie, pomagając komórkom utrzymać równowagę redoks i opóźniać zmiany zwyrodnieniowe. To stawia laktylację SOD1 jako kluczowy molekularny przełącznik łączący stres metaboliczny z utratą strukturalnej integralności krążków międzykręgowych.
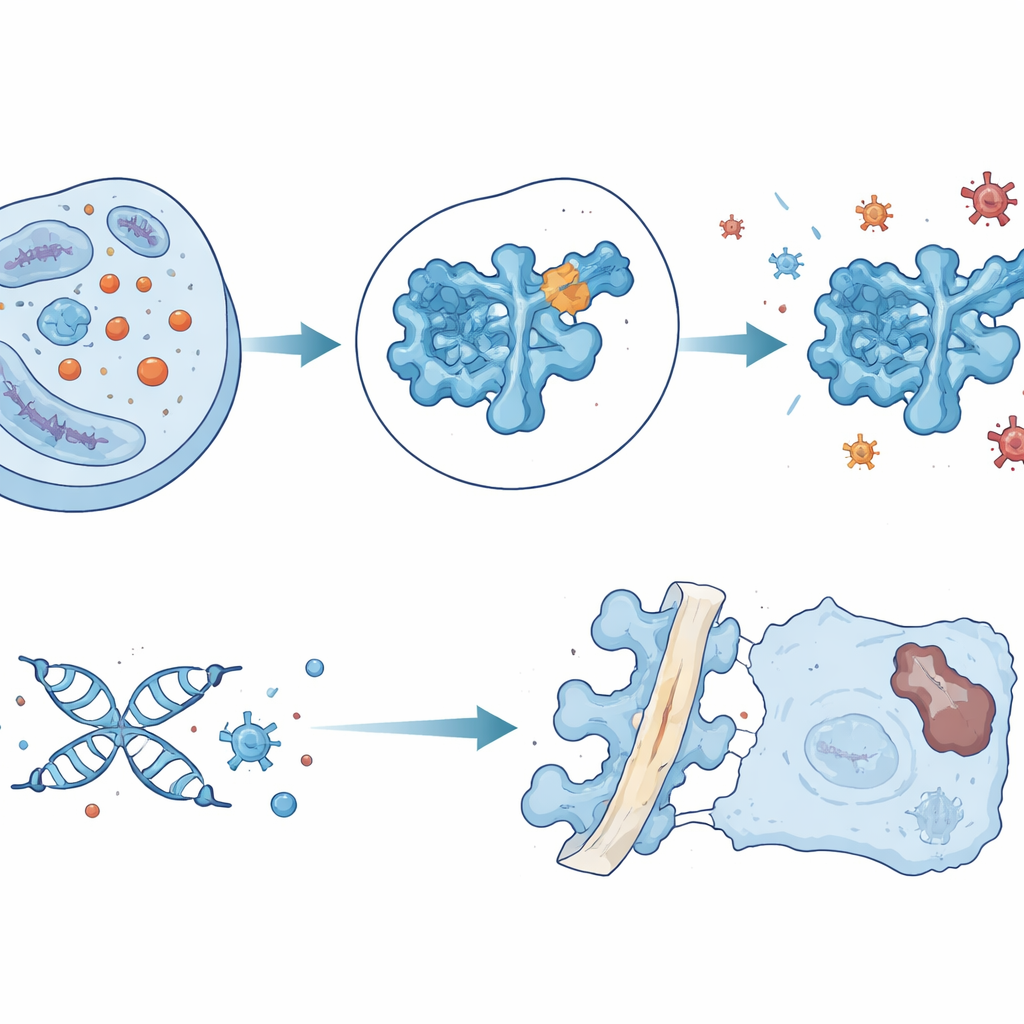
Koncepcja precyzyjnego dostarczania leku
Wyposażeni w tę wiedzę, badacze przeszukali in silico 1,6 miliona małych cząsteczek w poszukiwaniu związków, które wiązałyby się w pobliżu podatnej kieszeni lizyny 123 w SOD1. Zidentyfikowali jeden związek nazwany ZL-01, który oddziałuje bezpośrednio z tym regionem i zmniejsza laktylację SOD1 bez wyraźnego wpływu na inne powszechne modyfikacje białek. W hodowanych komórkach krążków ZL-01 przywracał aktywność SOD1, obniżał stres oksydacyjny oraz zmniejszał markery uszkodzeń DNA i senescencji. Podany do uszkodzonych krążków szczurów spowalniał degenerację, lecz lek był szybko usuwany z tkanki. Aby zwiększyć czas zalegania i celowanie, badacze załadowali ZL-01 do małych pęcherzyków pozakomórkowych inżynieryjnie wyposażonych w peptyd silnie wiążący kolagen typu II, główny składnik jądra krążka. Ten system dostarczania utrzymywał ZL-01 dłużej w krążku, dodatkowo zmniejszał laktylację SOD1 i stres oksydacyjny oraz znacząco poprawiał strukturę i funkcję krążków u zwierząt.
Co to oznacza dla osób z bólem pleców
W sumie praca ujawnia łańcuch zdarzeń, w którym nagromadzenie mleczanu w źle odżywianych krążkach chemicznie rozbraja kluczowy enzym antyoksydacyjny SOD1, wywołując uszkodzenia oksydacyjne, sygnalizację stresu i przyspieszone zwyrodnienie krążków. Pokazując, że zablokowanie pojedynczego miejsca laktylacji może chronić komórki krążków oraz projektując ukierunkowaną małą cząsteczkę zdolną to osiągnąć, badanie wskazuje na przyszłość, w której leczenie bólu pleców mogłoby polegać nie tylko na łagodzeniu objawów lub chirurgicznym usuwaniu uszkodzonych tkanek, ale na bezpośrednim korygowaniu molekularnych błędów prowadzących do przedwczesnego zużywania się krążków.
Cytowanie: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Słowa kluczowe: zwyrodnienie krążków międzykręgowych, mleczan, laktylacja białek, stre s oksydacyjny, SOD1