Clear Sky Science · de
SOD1-Lactylierung beeinträchtigt seine enzymatische Aktivität durch Konformationsänderung und verschlimmert die Bandscheibendegeneration
Warum Rückenschmerzen so früh beginnen
Nackenschmerzen und Kreuzschmerzen gehören zu den weltweit führenden Ursachen für Beeinträchtigungen, und sie treten oft überraschend früh im Leben auf. Im Zentrum vieler Fälle steht der langsame Abbau der Puffer zwischen unseren Wirbeln, die sogenannten Bandscheiben. Diese Studie deckt eine bisher verborgene chemische Veränderung in Bandscheibenzellen auf, die ein gängiges Stoffwechselnebenprodukt, Laktat, mit vorzeitiger Alterung und dem Versagen dieser stoßdämpfenden Strukturen verbindet — und sie weist auf eine gezielte neue Behandlungsstrategie hin.
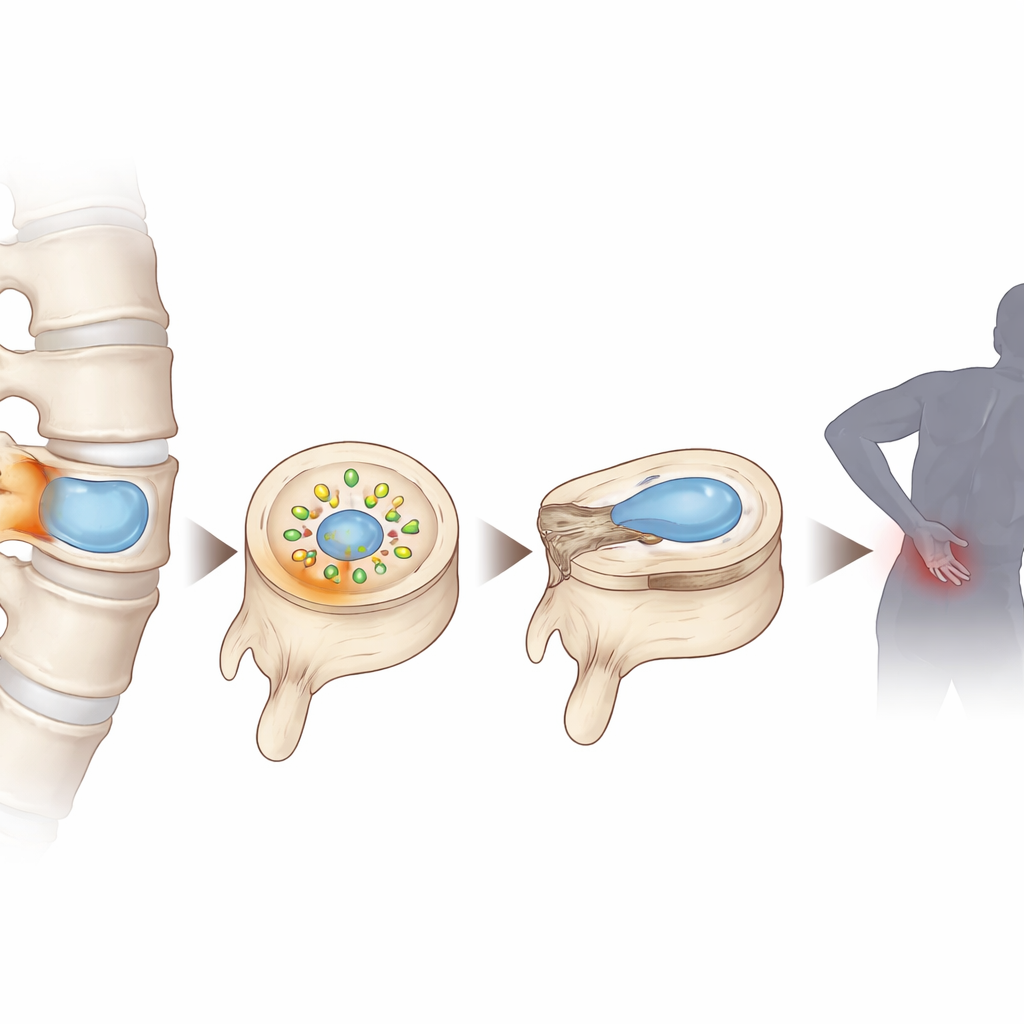
Die verborgene Welt innerhalb der Bandscheiben
Jede Bandscheibe besitzt ein weiches, gelartiges Zentrum, den Nukleus pulposus, der in einer sauerstoff- und nährstoffarmen Umgebung überlebt, weil er kaum direkte Blutversorgung hat. Wenn Bandscheiben degenerieren, wird diese Umgebung noch stärker von Sauerstoff und Nährstoffen beraubt, wodurch sich Stoffwechselabfälle ansammeln. Durch die Analyse menschlichen Bandscheibengewebes in verschiedenen Degenerationsstadien und die Kombination von fortgeschrittener Einzelzellsequenzierung und Metabolomik fanden die Forschenden heraus, dass Laktat — dasselbe Molekül, das sich bei intensiver Muskelarbeit ansammelt — in geschädigten Bandscheiben ungewöhnlich hohe Konzentrationen erreicht. Sie beobachteten außerdem, dass Bandscheibenzellen unter diesen Bedingungen Zeichen von oxidativem Stress, DNA-Schäden und vorzeitiger zellulärer Alterung zeigten.
Wenn Laktat beginnt, Proteine umzuschreiben
Laktat tut mehr als sich nur anzusammeln: Es kann Proteine chemisch modifizieren in einem Prozess, der Lactylierung genannt wird, wobei ein kleines, vom Laktat abgeleitetes Etikett an spezifische Stellen angehängt wird. Mithilfe einer „Lactylom“-Untersuchung tausender Proteinfragmente aus Rattenbandscheiben kartierte das Team, wo diese Markierungen während der Bandscheibendegeneration auftreten. Viele der betroffenen Proteine sind an der Kontrolle reaktiver Sauerstoffspezies beteiligt — instabile Moleküle, die DNA, Lipide und Proteine schädigen können. Besonders ein Enzym stach hervor: Superoxiddismutase 1 (SOD1). SOD1 neutralisiert normalerweise hochreaktive Sauerstoffformen und fungiert als zentrale antioxidative Verteidigung in Bandscheibenzellen. In degenerierenden Scheiben zeigte eine bestimmte Stelle auf SOD1, die Aminosäure Lysin 123, starke Lactylierung.
Wie ein winziges chemisches Etikett einen zellulären Schild außer Kraft setzt
Um zu verstehen, was diese Modifikation bewirkt, erzeugten die Forschenden Bandscheibenzellen und Ratten, bei denen Lysin 123 durch eine andere Aminosäure ersetzt wurde, die nicht lactyliert werden kann. Diese „geschützten“ Varianten von SOD1 behielten ihre Enzymaktivität selbst bei hohen Laktatspiegeln, verringerten den oxidativen Stress und reduzierten DNA-Schäden sowie zelluläre Alterungsanzeichen in Bandscheibenzellen. In lebenden Ratten mit Bandscheibenverletzungen zeigten Tiere mit der nicht-lactylierbaren SOD1 auf MRT und Gewebeanalyse eine mildere Degeneration. Computersimulationen der 3D-Struktur von SOD1 lieferten eine Erklärung: Der Lactyl-Anhang an Position 123 verändert subtil die Enzymoberfläche in der Nähe der kupferhaltigen aktiven Stelle, schwächt die Bindung an reaktive Sauerstoffmoleküle und macht das Gesamtprotein weniger stabil.
Den Schadensschalter ausschalten
Die Folgen dieser strukturellen Veränderung reichen bis in die genetischen Kontrollsysteme der Bandscheibenzelle. Wenn SOD1 durch Lactylierung geschwächt ist, sammelt sich reaktiver Sauerstoff an und schaltet den p53-Weg ein, einen zentralen Regulator für zellulären Stress und Seneszenz. Zellen treten in einen schadenhaften Zustand ein, funktionieren nicht mehr richtig und tragen zum Gewebeabbau bei. Im Gegensatz dazu dämpft die Blockade der Lactylierung an Lysin 123 die Aktivierung von p53 und dessen nachgeschaltete Ziele, hilft Zellen, das Redoxgleichgewicht zu erhalten, und verzögert degenerative Veränderungen. Dies positioniert die SOD1-Lactylierung als einen wichtigen molekularen Schalter, der metabolischen Stress mit strukturellem Versagen in Bandscheiben verbindet.
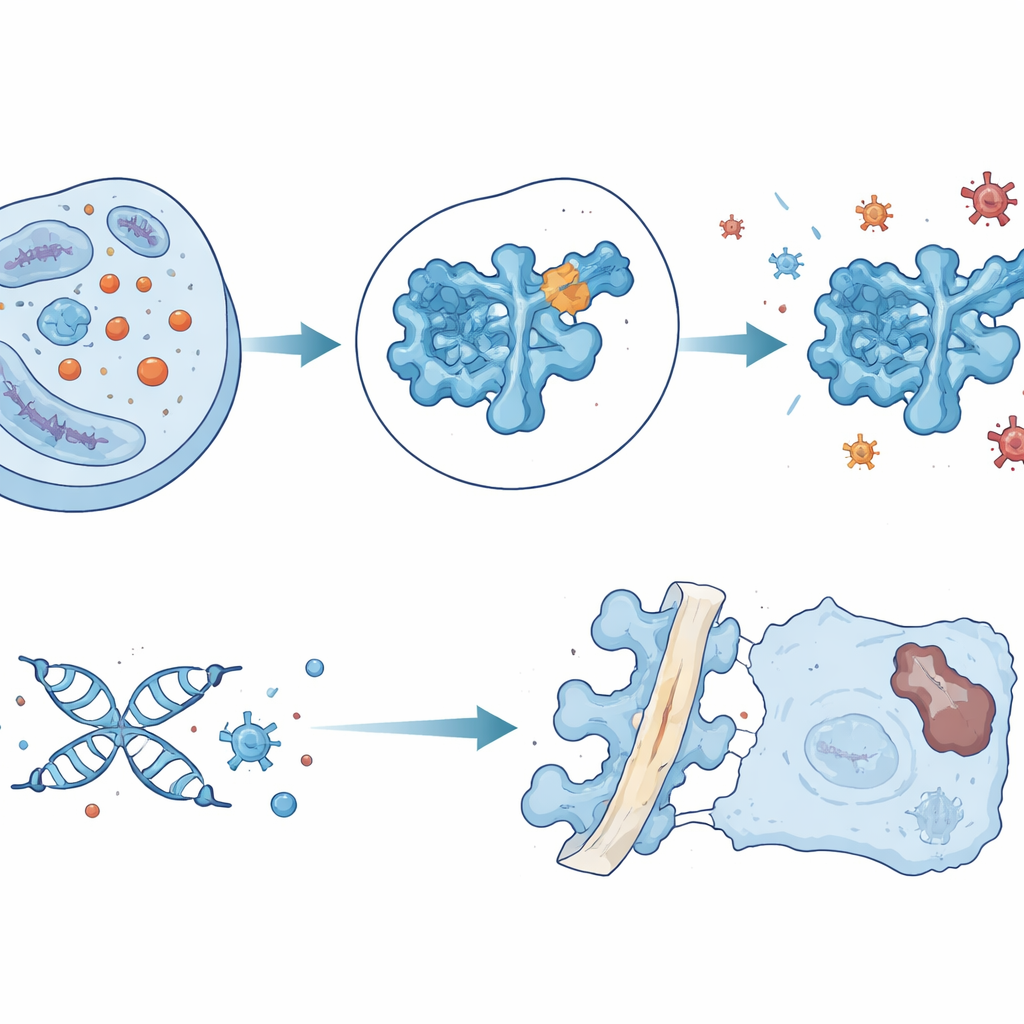
Eine Idee für präzise Wirkstoffabgabe
Mit dieser Einsicht durchsuchte das Team 1,6 Millionen kleine Moleküle in silico nach Verbindungen, die nahe der verwundbaren Lysin-123-Tasche von SOD1 binden könnten. Sie identifizierten eines, genannt ZL-01, das direkt mit diesem Bereich interagiert und die SOD1-Lactylierung reduziert, ohne andere häufige Proteinmodifikationen merklich zu beeinflussen. In kultivierten Bandscheibenzellen stellte ZL-01 die SOD1-Aktivität wieder her, senkte oxidativen Stress und verringerte Marker für DNA-Schäden und Seneszenz. In verletzte Rattenbandscheiben injiziert bremste es die Degeneration, wurde aber schnell aus dem Gewebe eliminiert. Um die Verweildauer und Zielgenauigkeit zu erhöhen, luden die Forschenden ZL-01 in winzige extrazelluläre Vesikel, die mit einem Peptid versehen waren, das stark an Kollagen Typ II bindet, einen Hauptbestandteil des Bandscheibenzentrums. Dieses Abgabesystem hielt ZL-01 länger in der Bandscheibe, verringerte SOD1-Lactylierung und oxidativen Stress weiter und verbesserte Struktur und Funktion der Bandscheiben in den Versuchstieren signifikant.
Was das für Menschen mit Rückenschmerzen bedeutet
Insgesamt zeigt die Arbeit eine Ereigniskette, in der sich Laktatansammlung in schlecht ernährten Bandscheiben dazu eignet, ein entscheidendes antioxidatives Enzym, SOD1, chemisch zu deaktivieren, was oxidativen Schaden, Stresssignale und beschleunigte Bandscheibendegeneration auslöst. Indem gezeigt wird, dass die Blockade einer einzelnen Lactylierungsstelle Bandscheibenzellen schützen kann, und indem ein gezieltes kleines Molekül entwickelt wurde, das genau dies erreicht, deutet die Studie auf eine Zukunft hin, in der wir Rückenschmerzen nicht nur symptomatisch lindern oder geschädigtes Gewebe operativ entfernen, sondern die zugrunde liegenden molekularen Fehlsteuerungen direkt korrigieren könnten, die dazu führen, dass Bandscheiben zu früh verschleißen.
Zitation: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Schlüsselwörter: Bandscheibendegeneration, Laktat, Protein-Lactylierung, oxidativer Stress, SOD1