Clear Sky Science · es
La lactilación de SOD1 reduce su actividad enzimática por un cambio conformacional y agrava la degeneración del disco intervertebral
Por qué el dolor de espalda empieza tan pronto
El dolor lumbar es una de las principales causas de discapacidad en todo el mundo y, a menudo, comienza sorprendentemente temprano en la vida. En el centro de muchos casos está la lenta degradación de los cojines entre nuestras vértebras, conocidos como discos intervertebrales. Este estudio revela un cambio químico previamente oculto dentro de las células del disco que conecta un subproducto metabólico común, el lactato, con el envejecimiento prematuro y el fallo de estos amortiguadores espinales, y apunta hacia una nueva estrategia de tratamiento dirigida.
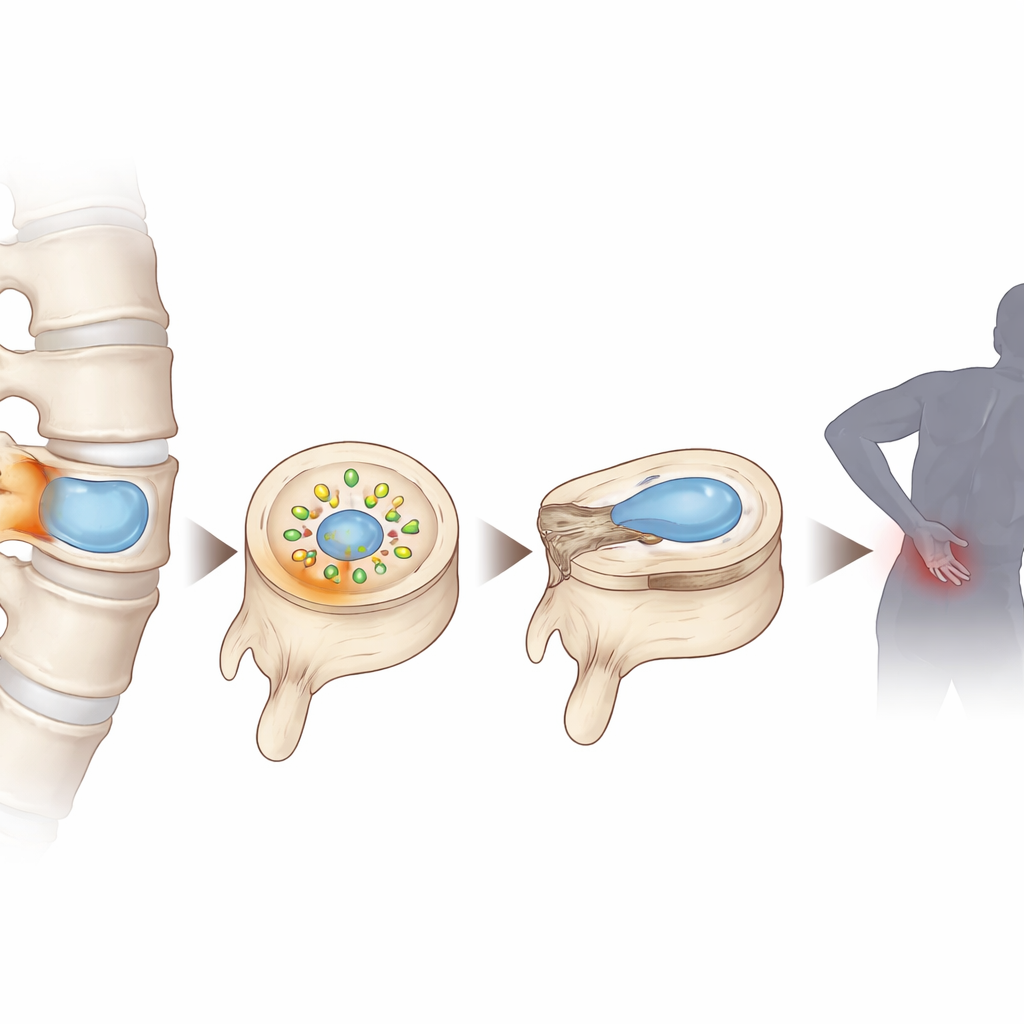
El mundo oculto dentro de los cojines espinales
Cada disco intervertebral tiene un centro blando y gelatinoso llamado núcleo pulposo, que sobrevive en un ambiente con poco oxígeno y pocos nutrientes porque prácticamente no tiene suministro sanguíneo directo. A medida que los discos se degeneran, este entorno se empobrece aún más en oxígeno y nutrientes, provocando la acumulación de productos de desecho. Al analizar tejido humano de disco en diferentes estadios de degeneración y combinar secuenciación unicelular avanzada y metabolómica, los investigadores encontraron que el lactato —la misma molécula que se acumula en los músculos durante el ejercicio intenso— aumenta a niveles inusualmente altos dentro de los discos dañados. También observaron que las células del disco en estas condiciones mostraban signos de estrés oxidativo, daño en el ADN y envejecimiento celular prematuro.
Cuando el lactato comienza a reescribir proteínas
El lactato hace más que acumularse: puede modificar químicamente proteínas en un proceso llamado lactilación, añadiendo una pequeña etiqueta derivada del lactato en sitios específicos. Mediante un estudio del “lactiloma” de miles de fragmentos proteicos de discos de rata, el equipo mapeó dónde aparecen estas etiquetas durante la degeneración del disco. Muchas de las proteínas afectadas participan en el manejo de especies reactivas de oxígeno —moléculas inestables que pueden dañar ADN, lípidos y proteínas. Una enzima en particular, la superóxido dismutasa 1 (SOD1), destacó. SOD1 normalmente neutraliza una forma altamente reactiva del oxígeno, actuando como una defensa antioxidante crucial dentro de las células del disco. En discos degenerativos, un sitio específico en SOD1, un aminoácido llamado lisina 123, mostró una marcada lactilación.
Cómo una pequeña etiqueta química desarma un escudo celular
Para entender qué hace esta modificación, los investigadores crearon células de disco y ratas en las que la lisina 123 fue reemplazada por otro aminoácido que no puede ser lactilado. Estas versiones “protegidas” de SOD1 mantuvieron su actividad enzimática incluso cuando los niveles de lactato eran altos, redujeron el estrés oxidativo y disminuyeron el daño en el ADN y el envejecimiento celular en las células del disco. En ratas vivas sometidas a lesión discal, los animales que portaban la SOD1 no lactilable mostraron una degeneración discal más leve en resonancia magnética y en el análisis tisular. Simulaciones por ordenador de la estructura 3D de SOD1 sugirieron por qué: la etiqueta lactil en la posición 123 remodela sutilmente la superficie de la enzima cerca de su sitio activo que contiene cobre, debilitando su capacidad para atrapar moléculas reactivas de oxígeno y haciendo que la proteína sea menos estable.
Apagar el interruptor del daño
Las consecuencias de este ajuste estructural se extienden a los sistemas de control genético de la célula del disco. Cuando SOD1 queda debilitada por la lactilación, las especies reactivas se acumulan y activan la vía p53, un regulador central del estrés celular y la senescencia. Las células entran en un estado de daño bloqueado, dejan de funcionar correctamente y contribuyen a la degradación del tejido. Por el contrario, bloquear la lactilación en la lisina 123 atenúa la activación de p53 y sus dianas a valle, ayudando a las células a mantener el equilibrio redox y retrasar los cambios degenerativos. Esto sitúa a la lactilación de SOD1 como un interruptor molecular clave que vincula el estrés metabólico con el fallo estructural en los discos intervertebrales.
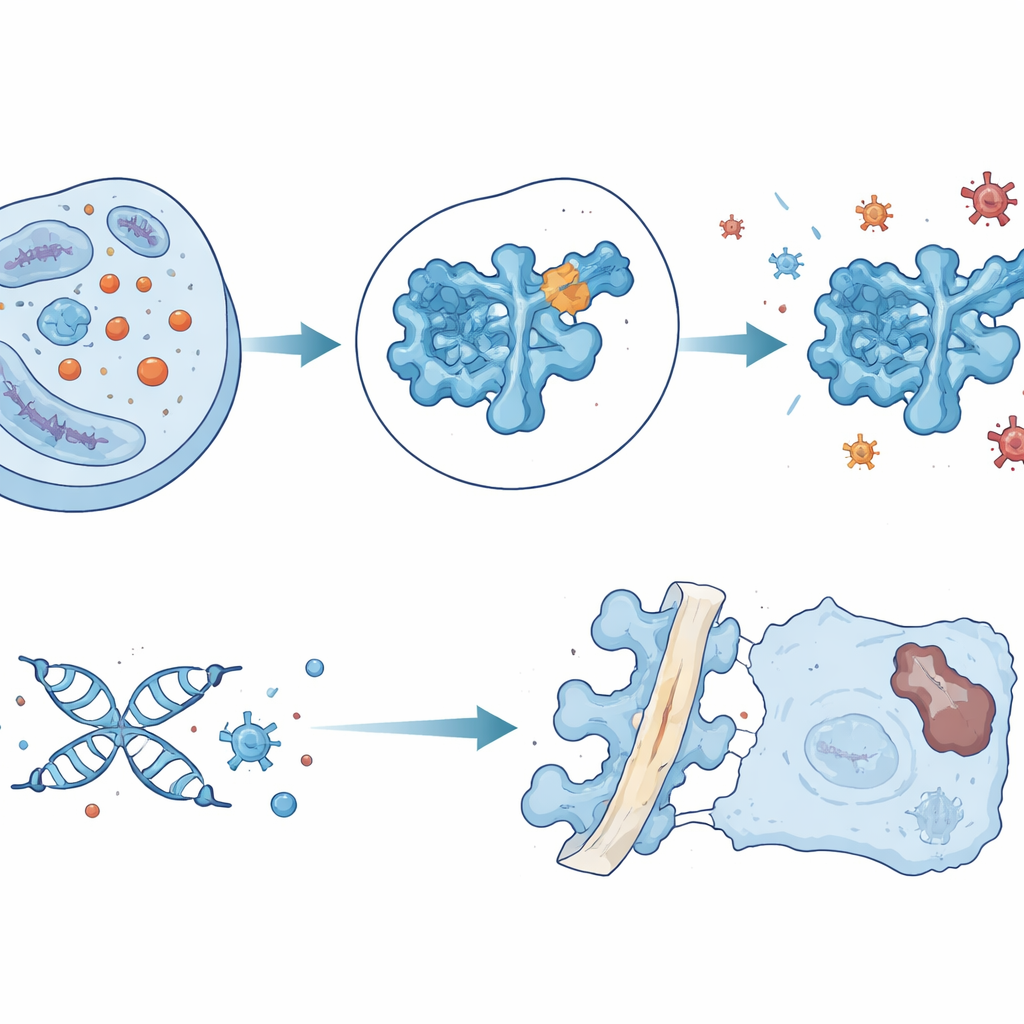
Una idea de administración farmacológica de precisión
Con este conocimiento, el equipo examinó 1,6 millones de pequeñas moléculas in silico en busca de compuestos que se unirían cerca del bolsillo vulnerable de la lisina 123 de SOD1. Identificaron una, denominada ZL-01, que interactúa directamente con esa región y reduce la lactilación de SOD1 sin afectar notablemente otras modificaciones proteicas comunes. En células de disco en cultivo, ZL-01 restauró la actividad de SOD1, redujo el estrés oxidativo y disminuyó marcadores de daño en el ADN y senescencia. Al inyectarlo en discos lesionados de rata, ralentizó la degeneración, pero el fármaco se eliminó con rapidez del tejido. Para aumentar su persistencia y especificidad, los investigadores cargaron ZL-01 en pequeñas vesículas extracelulares diseñadas con un péptido que se une fuertemente al colágeno tipo II, un componente principal del centro del disco. Este sistema de entrega mantuvo ZL-01 más tiempo en el disco, redujo aún más la lactilación de SOD1 y el estrés oxidativo, y mejoró de forma significativa la estructura y función del disco en los animales.
Qué significa esto para las personas con dolor de espalda
En conjunto, el trabajo revela una cadena de acontecimientos en la que la acumulación de lactato dentro de discos mal nutridos desactiva químicamente una enzima antioxidante clave, SOD1, desencadenando daño oxidativo, señalización de estrés y una degeneración acelerada del disco. Al demostrar que bloquear un único sitio de lactilación puede proteger las células del disco y al diseñar una pequeña molécula dirigida para lograrlo, el estudio apunta a un futuro en el que podríamos tratar el dolor de espalda no solo aliviando los síntomas o extirpando quirúrgicamente el tejido dañado, sino corrigiendo directamente los errores moleculares subyacentes que hacen que los discos se desgasten prematuramente.
Cita: Zhang, Y., Zhai, Y., Liu, C. et al. SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration. Nat Commun 17, 3318 (2026). https://doi.org/10.1038/s41467-026-69127-3
Palabras clave: degeneración del disco intervertebral, lactato, lactilación de proteínas, estrés oxidativo, SOD1