Clear Sky Science · zh
通过光/钴协同催化实现多氟烷基化合物与烯烃的自由基去氟烯丙基化反应
为何改造难以动手的富氟分子很重要
富含氟的化学品渗透于现代生活的各个方面,从药物和农用防护剂到耐污涂层。它们的威力来自碳—氟键——有机化学中最牢固的键之一,使这些化合物在体内和环境中异常稳定。然而,正是这种坚固性让有意改造它们变得非常困难。本研究提出了一种温和的方法,可以在长链含氟分子上断开一个特定的碳—氟键,并将其替换为有用的碳—碳键,从而有望帮助化学家用这些顽固分子设计更好的药物和材料。
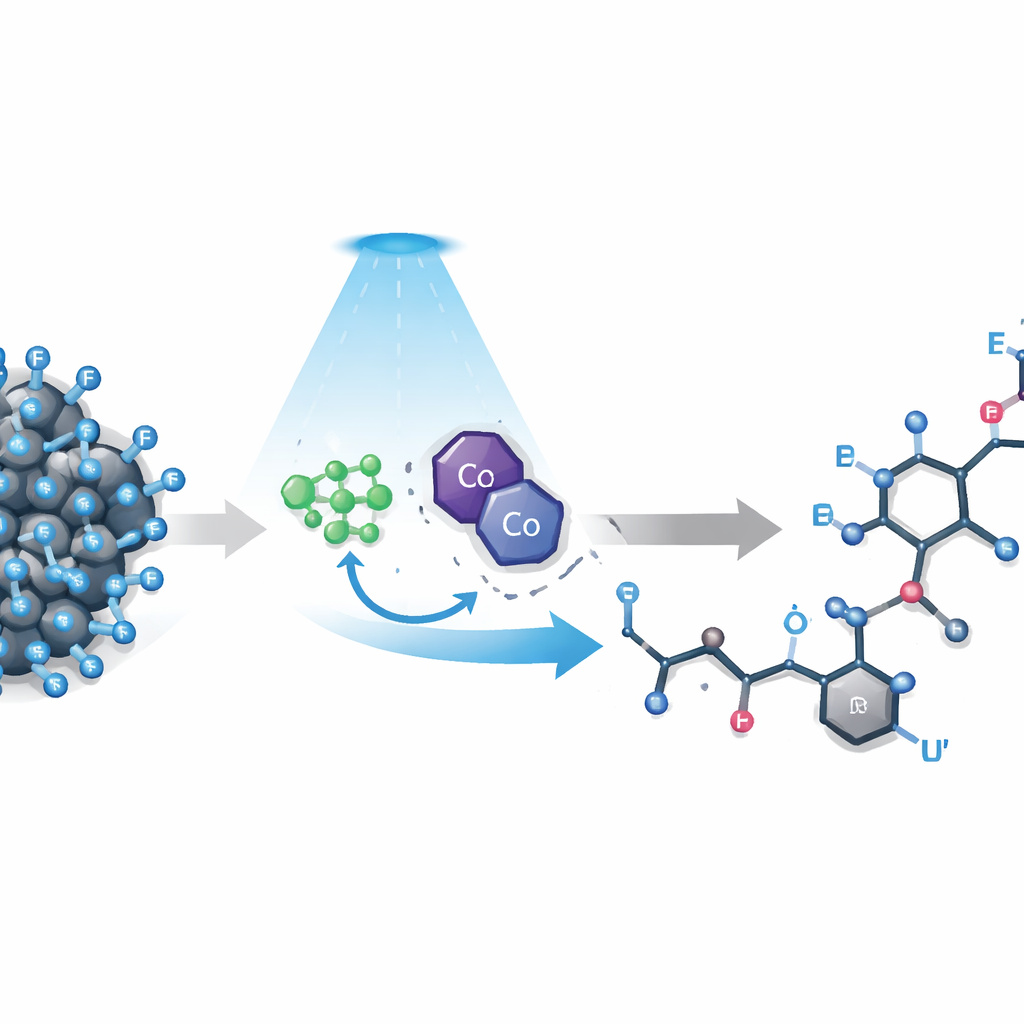
切断最强键的挑战
多氟烷基化合物含有许多氢被氟取代的链段。这些链段赋予分子拒水性和化学抗性,对于技术和医药上很有吸引力,但在化学家希望微调其性能时却成了麻烦。现有方法通常侧重于最简单的含氟基团CF3,或需要高度活泼的添加剂和预先构建的偶联伙伴。更长的链——在实际产品中很常见——则更难驾驭:强烈的氟原子拉电子效应会使活性中间体不稳定,体积庞大的氟原子阻碍反应位点的接近,而且电子可能回流,撤销早期步骤。因此,尝试断开一个特定的碳—氟键常常导致产物混杂或彻底失败。
由光驱动的双催化策略
作者们开发了一种利用两种协同催化剂和可见光来驯服这些难以反应分子的策略。一个感光的铱配合物首先向多氟烷基化合物提供一个电子,适度弱化某一碳—氟键,促使其断裂生成短寿命的含氟自由基。与此同时,一个以维生素B12为模型的钴催化剂则引导将来将被引入的氢原子的位点。一个简单的硼试剂充当“氟离子海绵”,捕获被释放的氟,防止其重组或引发电子回流。在温和的蓝光LED照射下,这一系列助剂将反应引导到高选择性的理想路径上。
用简单烯烃构建新键
一旦生成,含氟自由基会加成到常见的烯烃——那些含碳碳双键的小分子——在一步之内形成新的碳—碳键。随后钴催化剂向特定的邻位转移一个氢原子,固定一个“烯丙”片段,同时保留有用的双键。在数十次试验中,该方法对多种烯烃(包括复杂的天然萜类)以及多种含三至十个碳链的富氟起始物或氟代酰胺类底物均有效。显著的是,即便烯烃含有数个几乎相同的烯丙C–H位点,反应仍以超过20比1的选择性优先发生在一个位点,避免了此类化学常见的异构体混杂问题。
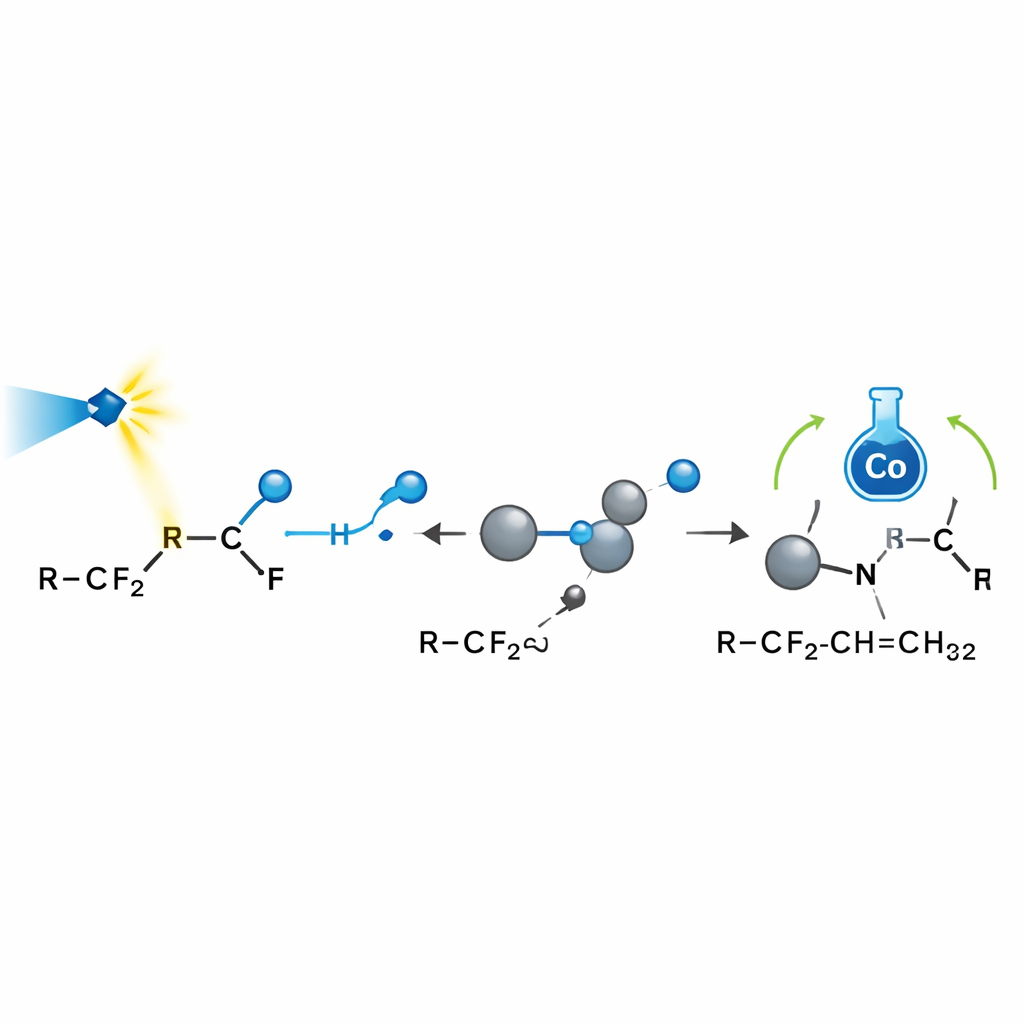
探究选择性如何产生
为了解该反应为何如此具有选择性,团队将实验探针与计算机模拟结合起来。化学“自由基捕获剂”和开环实验证实了含氟自由基是关键中间体。电子自旋测量显示二氧化碳也可被还原为有反应性的阴离子,帮助活化某些含氟酰胺。核磁共振信号证明硼试剂确实捕获了游离氟离子。量子化学计算描绘了各步的能量图景,显示在自由基加成到烯烃之后,钴更倾向于向某一特定位点供给氢,因为那里受到的空间阻碍较小并且存在有利的吸引相互作用。这就解释了为何只有一个烯丙位被反应以及产物在双键周围为何强烈偏向单一构型。
这一进展在实践中的意义
通过协同运用光、金属催化剂和一个结合氟的添加剂,这项工作在不使用苛刻条件或复杂起始物的情况下,将一些最难断开的碳—氟键转化为可设计的碳—碳连接。通俗来说,该方法把极其惰性的含氟片段变成可预测地附着到简单烯烃上的灵活构建模块。这为定制含氟骨架以用于药物、农用化学品和先进材料开辟了道路,同时也提供了新的工具,让人们重新思考如何转化而非被动容忍持久的含氟物质。
引用: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
关键词: 含氟分子, 光氧化还原催化, 钴催化, 自由基反应, 烯烃官能团化