Clear Sky Science · pt
Defluoroalilação radicalar de compostos polifluoroalquil com alcenos via catálise sinérgica fotoredox/cobalto
Por que transformar moléculas ricas em flúor importa
Compostos ricos em flúor estão por toda parte na vida moderna, de medicamentos e agrotóxicos a revestimentos resistentes a manchas. Seu poder vem das ligações carbono–flúor, que estão entre as mais fortes na química orgânica, tornando esses compostos incomumente estáveis no organismo e no ambiente. Essa mesma resistência, porém, dificulta modificá‑los deliberadamente. Este estudo apresenta uma maneira suave de romper uma ligação carbono–flúor específica em cadeias fluoradas longas e substituí‑la por uma ligação carbono–carbono útil, potencialmente ajudando químicos a projetar medicamentos e materiais melhores a partir dessas moléculas teimosas.
O desafio de cortar a ligação mais forte
Compostos polifluoroalquil contêm cadeias nas quais muitos hidrogênios foram substituídos por flúor. Essas cadeias tornam as moléculas repelentes à água e quimicamente resilientes, o que é atraente para tecnologia e medicina, mas problemático quando químicos querem ajustar seu comportamento. Métodos existentes tendem a focar no grupo fluorado mais simples, CF3, ou exigem aditivos altamente reativos e parceiros de acoplamento pré‑preparados. Cadeias mais longas, comuns em produtos reais, são ainda mais difíceis de controlar: a forte atração do flúor desestabiliza intermediários reativos, átomos volumosos de flúor bloqueiam o acesso e elétrons podem fluir de volta, desfazendo etapas iniciais. Como resultado, tentativas de quebrar uma ligação carbono–flúor escolhida frequentemente levam a misturas confusas ou fracassos completos.
Uma abordagem com dois catalisadores ativada pela luz
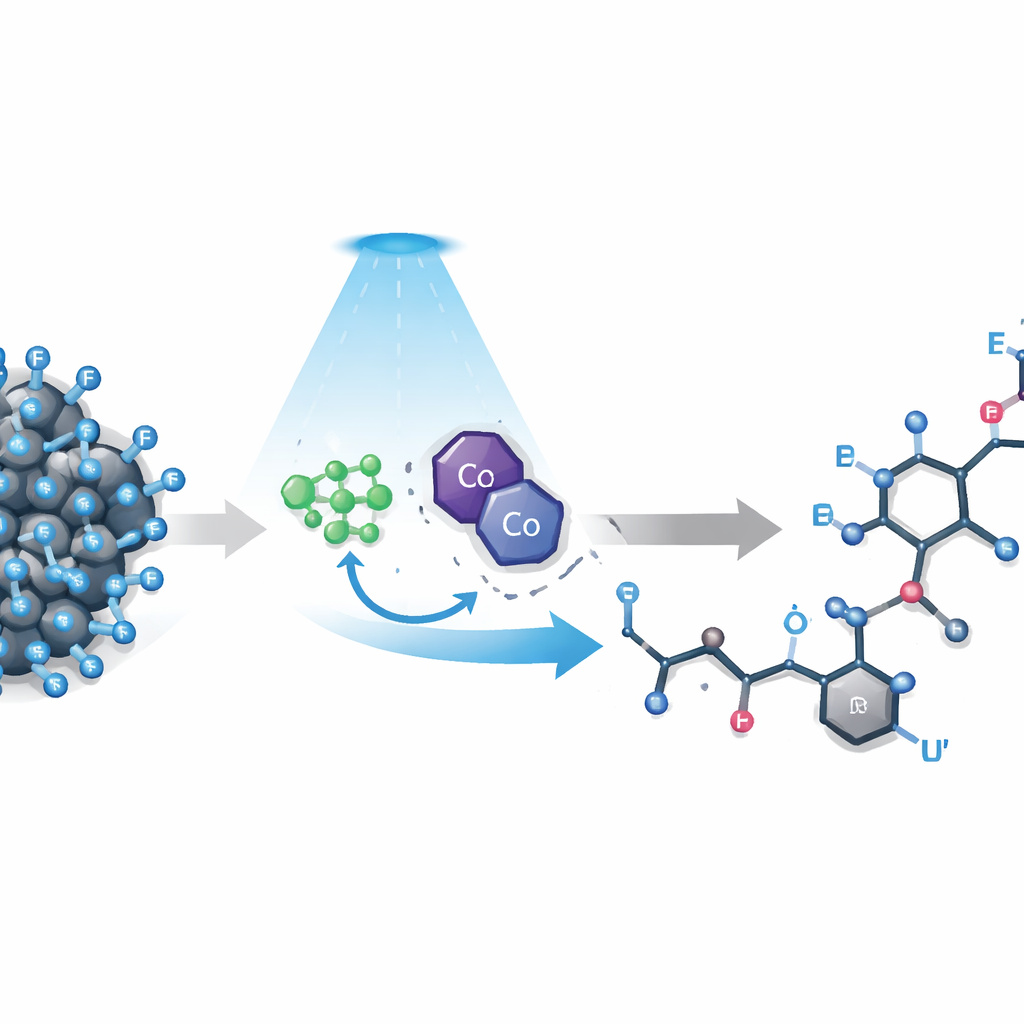
Os autores desenvolveram uma estratégia que usa dois catalisadores cooperativos e luz visível para domar essas moléculas difíceis. Um complexo de irídio fotossensível doa primeiro um único elétron para um composto polifluoroalquil, enfraquecendo uma ligação carbono–flúor o suficiente para que ela se rompa e libere um fragmento fluorado de curta vida útil conhecido como radical. Ao mesmo tempo, um catalisador de cobalto modelado no vitamina B12 orienta onde um átomo de hidrogênio será finalmente adicionado. Um reagente simples à base de boro atua como uma “esponja de fluoreto”, capturando o flúor expulso e impedindo que ele recombine ou direcione elétrons de volta. Sob iluminação suave por LEDs azuis, essa rede de auxiliares canaliza a reação por um caminho produtivo e altamente seletivo.
Construindo novas ligações com alcenos simples
Uma vez formados, os radicais fluorados adicionam‑se a alcenos comuns — pequenas moléculas com uma dupla ligação carbono–carbono — criando novas ligações carbono–carbono em um único passo. O catalisador de cobalto então transfere um átomo de hidrogênio para uma posição vizinha específica, fixando um fragmento “alílico” enquanto preserva a dupla ligação útil. Em dezenas de testes, o método funcionou com uma ampla gama de alcenos, incluindo terpenos naturais complexos, e com muitos materiais inicias ricos em flúor contendo cadeias de três a dez carbonos ou grupos amida fluorados. De forma notável, mesmo quando os alcenos continham vários sítios alílicos C–H quase idênticos, a reação escolheu uma posição com seletividade superior a 20 para 1, evitando o emaranhado de isômeros que normalmente atormenta essa química.
Investigando como surge a seletividade
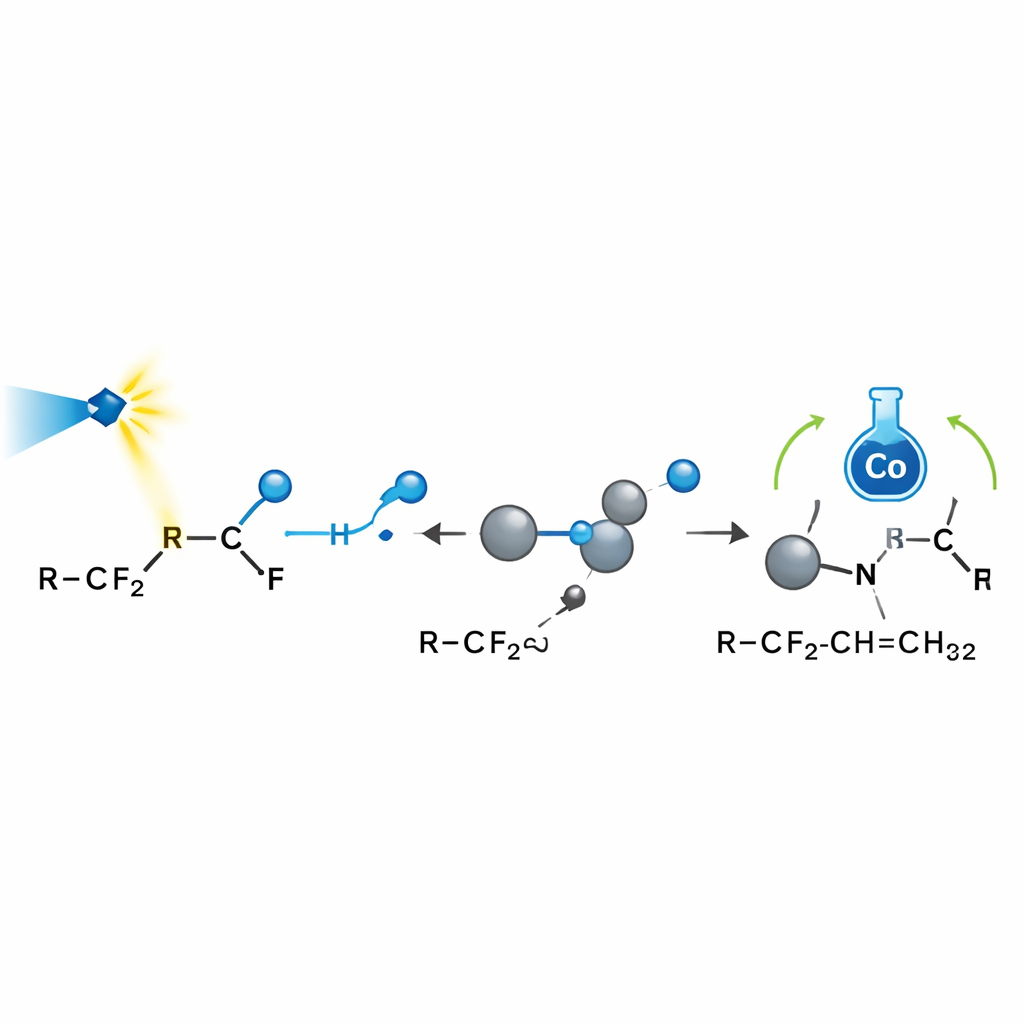
Para entender por que a reação é tão seletiva, a equipe combinou sondas laboratoriais com modelagem computacional. “Armadilhas” químicas para radicais e experimentos de abertura de anéis confirmaram que radicais fluorados são participantes chave. Medidas de spin eletrônico mostraram que o dióxido de carbono também pode ser reduzido a um ânion reativo que ajuda a ativar certas amidas fluoradas. Sinais de ressonância magnética nuclear revelaram que o reagente de boro de fato captura fluoreto livre. Cálculos quântico‑químicos mapearam a paisagem energética de cada etapa, mostrando que, depois que o radical se adiciona a um alceno, o cobalto prefere entregar hidrogênio a um sítio particular porque enfrenta menos bloqueio estérico e se beneficia de interações atrativas favoráveis. Isso explica tanto por que apenas uma posição alílica reage quanto por que os produtos favorecem fortemente um único arranjo geométrico ao redor da dupla ligação.
O que esse avanço significa na prática
Orquestrando luz, um catalisador metálico e um aditivo que liga o fluoreto, este trabalho converte algumas das ligações carbono–flúor mais difíceis em conexões carbono–carbono sob medida sem condições rigorosas ou materiais iniciales elaborados. Em termos práticos, o método transforma fragmentos fluorados extremamente inertes em blocos de construção flexíveis que podem ser ligados a alcenos simples de maneira previsível. Isso abre um caminho para moldar estruturas fluoradas sob medida para fármacos, agroquímicos e materiais avançados, ao mesmo tempo em que oferece novas ferramentas para repensar como substâncias fluoradas persistentes podem ser transformadas em vez de simplesmente toleradas.
Citação: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
Palavras-chave: moléculas fluoradas, catálise fotoredox, catálise por cobalto, reações radicalares, funcionalização de alcenos