Clear Sky Science · it
Defluoroallilazione radicalica di composti polifluoroalchilici con alcheni mediante catalisi sinergica fotoredox/cobalto
Perché modificare molecole ricche di fluoro è importante
I composti ricchi di fluoro sono ovunque nella vita moderna, dai farmaci e dai prodotti per la protezione delle colture ai rivestimenti resistenti alle macchie. La loro efficacia deriva dai legami carbonio–fluoro, tra i più forti in chimica organica, che rendono questi composti straordinariamente stabili nell’organismo e nell’ambiente. Questa stessa robustezza, tuttavia, li rende molto difficili da modificare intenzionalmente. Questo studio introduce un metodo delicato per rompere un legame carbonio–fluoro specifico in catene fluorurate lunghe e sostituirlo con un utile legame carbonio–carbonio, aiutando potenzialmente i chimici a progettare farmaci e materiali migliori a partire da queste molecole ostinate.
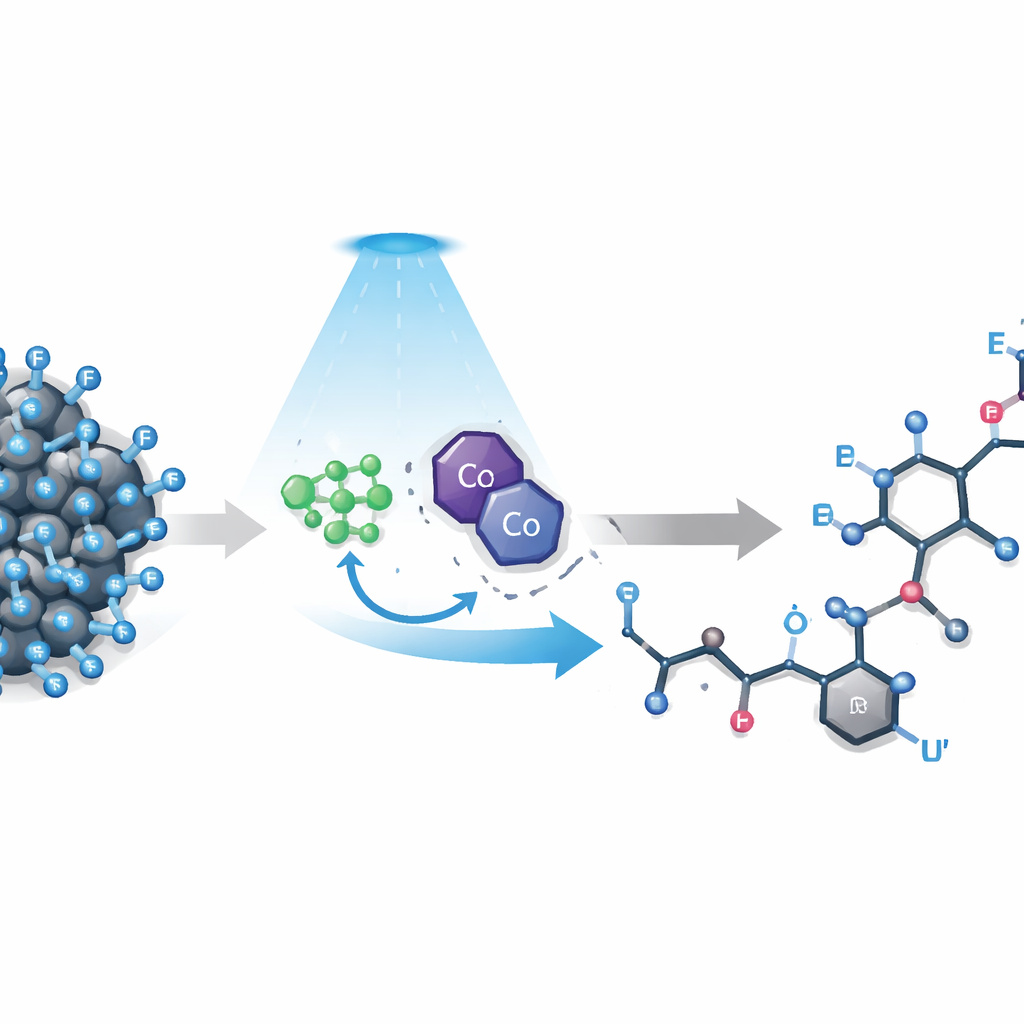
La sfida di spezzare il legame più forte
I composti polifluoroalchilici contengono catene in cui molti atomi di idrogeno sono stati sostituiti dal fluoro. Queste catene rendono le molecole idrorepellenti e chimicamente resistenti, caratteristica apprezzata in tecnologia e medicina ma problema quando i chimici vogliono affinare il loro comportamento. I metodi esistenti tendono a concentrarsi sul gruppo fluorurato più semplice, CF3, o richiedono additivi altamente reattivi e partner di accoppiamento preformati. Le catene più lunghe, comuni nei prodotti reali, sono ancora più difficili da controllare: l’elevata elettronegatività del fluoro destabilizza gli intermedi reattivi, gli ingombranti atomi di fluoro ostacolano l’accesso e gli elettroni possono ridistribuirsi all’indietro annullando i passaggi iniziali. Di conseguenza, i tentativi di rompere un preciso legame carbonio–fluoro spesso portano a miscele confuse o al fallimento completo.
Un approccio a due catalizzatori alimentato dalla luce
Gli autori hanno sviluppato una strategia che impiega due catalizzatori cooperanti e luce visibile per domare queste molecole difficili. Un complesso di iridio sensibile alla luce dona inizialmente un elettrone singolo a un composto polifluoroalchilico, indebolendo quel legame carbonio–fluoro quanto basta perché si rompa e generi un frammento fluorurato a vita breve noto come radicale. Allo stesso tempo, un catalizzatore a base di cobalto modellato sul funzionamento della vitamina B12 guida il punto in cui verrà infine aggiunto un atomo di idrogeno. Un semplice reagente a base di boro funge da “spugna per il fluoruro”, intrappolando il fluoro espulso ed evitando che riconsideri o riporti indietro elettroni. Sotto illuminazione dolce con LED blu, questa rete di assistenti incanala la reazione lungo un percorso produttivo e altamente selettivo.
Costruire nuovi legami con alcheni semplici
Una volta formati, i radicali fluorurati si addizionano ad alcheni comuni—piccole molecole con un doppio legame carbonio–carbonio—creando nuovi legami carbonio–carbonio in un unico passaggio. Il catalizzatore a cobalto quindi trasferisce un atomo di idrogeno a una posizione vicina specifica, fissando un frammento “allilico” e preservando il doppio legame utile. In decine di prove, il metodo ha funzionato su un’ampia gamma di alcheni, compresi terpeni naturali complessi, e su molti diversi materiali di partenza ricchi di fluoro con catene da tre a dieci atomi di carbonio o gruppi ammidici fluorurati. Notevolmente, anche quando gli alcheni contenevano diversi siti allilici C–H quasi identici, la reazione ha scelto una posizione con una selettività superiore a 20 a 1, evitando l’intrico di isomeri che di solito complica questa chimica.
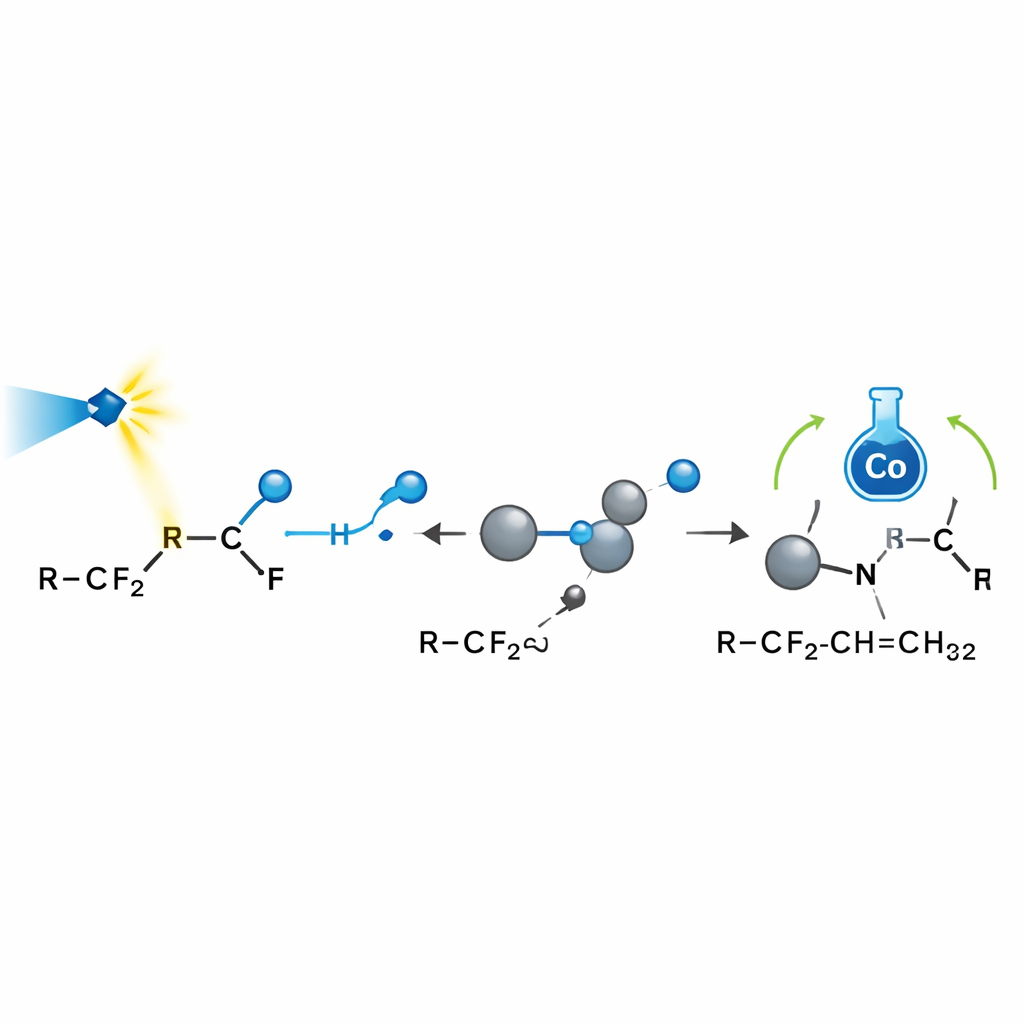
Indagare l’origine della selettività
Per capire perché la reazione è così selettiva, il team ha combinato sondaggi sperimentali con modellizzazione al computer. “Trappole” per radicali e esperimenti di apertura di anelli hanno confermato che i radicali fluorurati sono attori chiave. Misure di risonanza di spin elettronico hanno mostrato che anche l’anidride carbonica può essere ridotta a un anione reattivo che aiuta ad attivare certe ammidi fluorurate. Spettri di risonanza magnetica nucleare hanno rivelato che il reagente al boro cattura effettivamente il fluoruro libero. Calcoli quantomeccanici hanno mappato il paesaggio energetico di ogni passaggio, mostrando che dopo l’addizione del radicale a un alchene il cobalto preferisce fornire l’idrogeno a un sito particolare perché incontra meno ingombro sterico e beneficia di interazioni attrattive favorevoli. Questo spiega sia perché reagisce solo una posizione allilica sia perché i prodotti favoriscono fortemente una singola disposizione geometrica attorno al doppio legame.
Cosa significa questo progresso nella pratica
Orchestrando luce, un catalizzatore metallico e un additivo che lega il fluoruro, questo lavoro trasforma alcuni dei legami carbonio–fluoro più difficili in connessioni carbonio–carbonio su misura senza condizioni dure o materiali di partenza elaborati. In termini pratici, il metodo converte frammenti fluorurati estremamente inertii in blocchi costruttivi flessibili che possono essere attaccati ad alcheni semplici in modo prevedibile. Ciò apre una strada per scaffolds fluorurati su misura per farmaceutici, agrochimici e materiali avanzati, offrendo al contempo nuovi strumenti per ripensare come le sostanze fluorurate persistenti possano essere trasformate piuttosto che semplicemente tollerate.
Citazione: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
Parole chiave: molecole fluorurate, catalisi fotoredox, catalisi al cobalto, reazioni radicaliche, funzionalizzazione degli alcheni