Clear Sky Science · ru
Радикальная дефтороаллилизация полифторированных соединений с алкенами через синергетический фоторедокс/кобальтовый катализ
Почему изменение трудно реагирующих фторсодержащих молекул важно
Химические соединения, насыщенные фтором, повсюду в современной жизни — от лекарств и средств защиты сельского хозяйства до пятноотталкивающих покрытий. Их сила заключается в углеродно‑фторных связях, одних из самых прочных в органической химии, что делает эти соединения необычайно стабильными в организме и в окружающей среде. Однако та же прочность затрудняет их целенаправленную модификацию. В данной работе предложен щадящий способ разорвать одну конкретную углеродно‑фторную связь в длинных фторированных цепях и заменить её полезной углеродно‑углеродной связью, что может помочь химикам проектировать лучшие лекарства и материалы на основе этих упорных молекул.
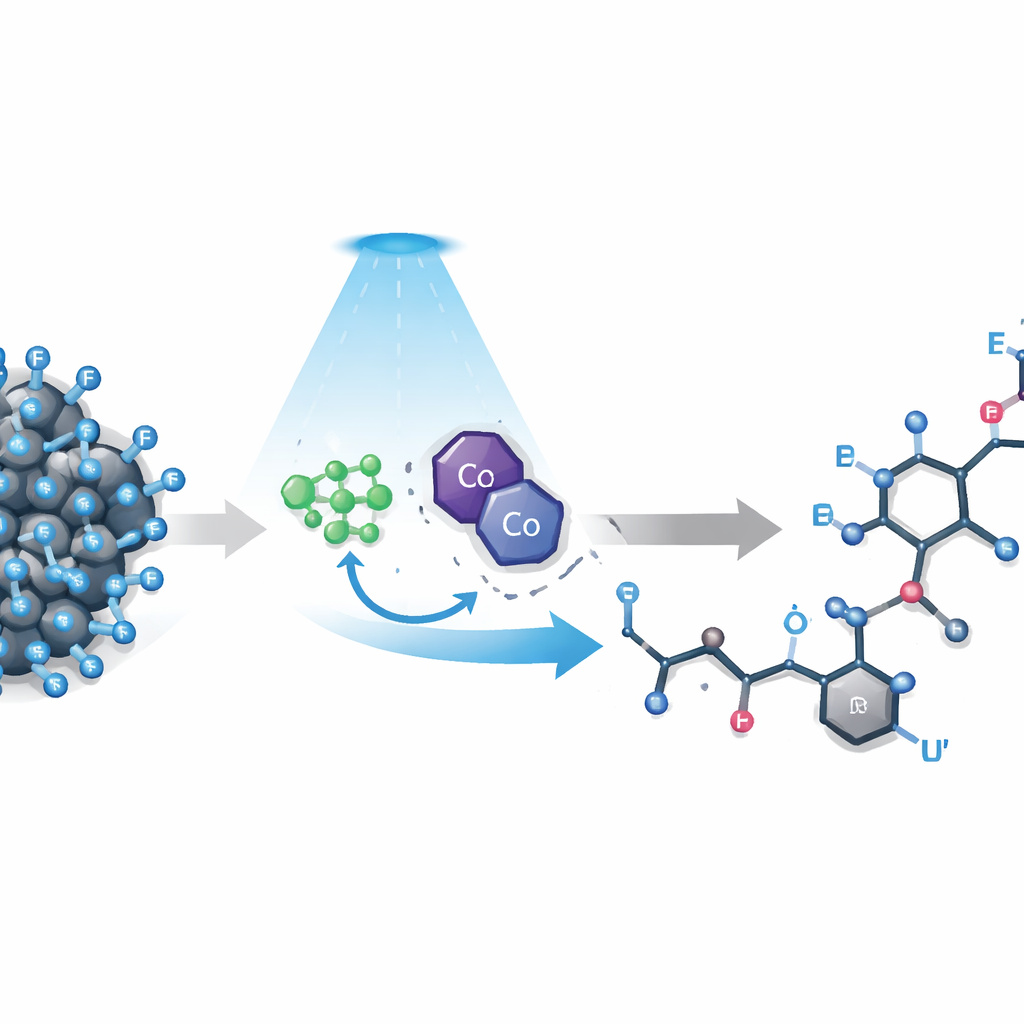
Проблема разрыва самой прочной связи
Полифторалкильные соединения содержат цепи, в которых многие атомы водорода заменены фтором. Эти цепи придают молекулам водоотталкивающие и химически стойкие свойства, что привлекательно для технологий и медицины, но проблематично, когда химикам нужно тонко настроить их поведение. Существующие методы обычно ориентированы на самый простой фторированный фрагмент — CF3 — или требуют крайне активных реагентов и заранее приготовленных компонентов для сшивки. Длинные цепи, характерные для реальных продуктов, ещё труднее контролируются: сильное притяжение фтора дестабилизирует реактивные промежуточные состояния, громоздкие атомы фтора мешают доступу, а электроны могут перетекать обратно и отменять ранние шаги. В результате попытки разорвать выбранную углеродно‑фторную связь часто приводят к сложным смесям или полным неудачам.
Подход с двумя катализаторами, приводимый в действие светом
Авторы разработали стратегию, использующую два взаимодополняющих катализатора и видимый свет для приручения этих трудных молекул. Фотоактивный иридиевый комплекс сначала отдаёт один электрон полифторалкильному соединению, слегка ослабляя одну углеродно‑фторную связь до её разрыва и образования короткоживущего фторированного фрагмента — радикала. Одновременно кобальтовый катализатор, смоделированный по образцу витамина B12, направляет, куда в конечном итоге добавится атом водорода. Простой борсодержащий реагент действует как «губка для фторида», улавливая выброшенный фтор и предотвращая его рекомбинацию или обратную передачу электронов. Под мягким освещением синими светодиодами эта сеть помощников направляет реакцию по продуктивному, высокоселективному пути.
Построение новых связей с простыми алкенами
Образовавшиеся фторированные радикалы присоединяются к обычным алкенам — небольшим молекулам с двойной углеродно‑углеродной связью — создавая новые углеродно‑углеродные связи в один шаг. Затем кобальт переносит атом водорода на конкретную соседнюю позицию, закрепляя «аллильный» фрагмент и сохраняя полезную двойную связь. В десятках экспериментов метод сработал на широком наборе алкенов, включая сложные природные терпены, а также на многих разных фторсодержащих исходных веществах с цепями от трёх до десяти атомов углерода или фторированными амидными группами. Поразительно, что даже когда алкены содержали несколько почти одинаковых аллильных C–H позиций, реакция выбирала одну позицию с селективностью лучше чем 20:1, избегая путаницы из изомеров, которая обычно сопровождает подобную химию.
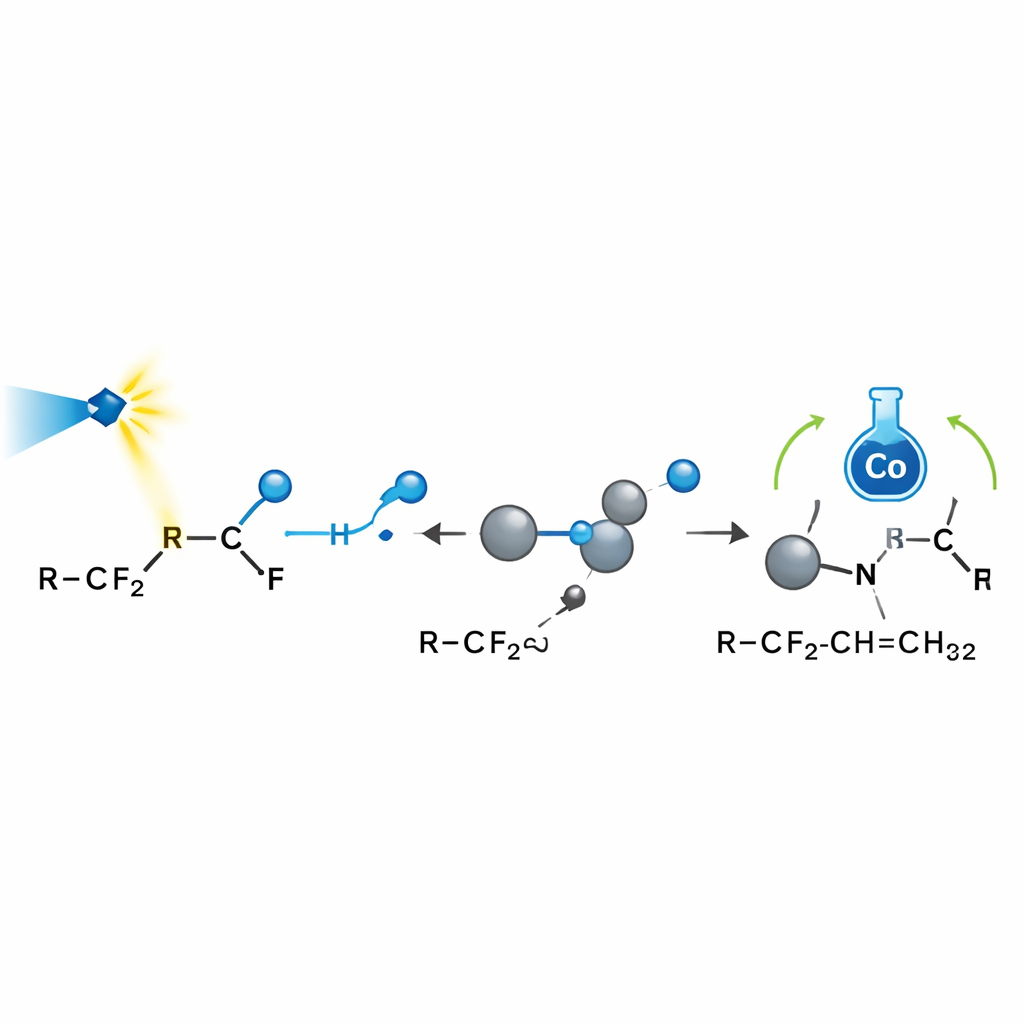
Изучение происхождения селективности
Чтобы понять, почему реакция столь селективна, команда сочетала лабораторные пробы с компьютерным моделированием. Химические «ловушки радикалов» и эксперименты по раскрытию колец подтвердили, что фторированные радикалы являются ключевыми участниками. Измерения электронной спиновой резонанса показали, что углекислый газ также может быть восстановлен до реакционноспособного аниона, который помогает активировать некоторые фторированные амиды. Сигналы ядерного магнитного резонанса выявили, что борсодержащий реагент действительно захватывает свободный фторид. Квантово‑химические расчёты нанесли на карту энергетический ландшафт каждого шага, показав, что после присоединения радикала к алкену кобальт предпочитает доставить водород в одну конкретную позицию, поскольку там меньше стерических помех и действуют благоприятные притягивающие взаимодействия. Это объясняет, почему реагирует лишь одна аллильная позиция и почему продукты сильно предпочтительны в одном геометрическом варианте вокруг двойной связи.
Что значит этот прогресс на практике
Сочетая свет, металлический катализатор и добавку, связывающую фторид, эта работа превращает некоторые из самых прочных углеродно‑фторных связей в «конструкционные» углеродно‑углеродные соединения без жёстких условий или сложных исходных материалов. Проще говоря, метод превращает исключительно инертные фторированные фрагменты в гибкие строительные блоки, которые можно предсказуемо присоединять к простым алкенам. Это открывает путь к созданию фторированных каркасов на заказ для фармацевтики, агрохимии и передовых материалов, а также предлагает новые инструменты для переосмысления того, как устойчивые фторсодержащие вещества можно трансформировать, а не просто выдерживать.
Цитирование: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
Ключевые слова: фторсодержащие молекулы, фоторедокс‑катализ, кобальтовый катализ, радикальные реакции, функционализация алкенов