Clear Sky Science · es
Defluoroalilación radicalaria de compuestos polifluoroalquílicos con alquenos mediante catálisis fotoredox/cobalto sinérgica
Por qué importa transformar moléculas ricas en flúor
Los compuestos cargados de flúor están presentes en la vida moderna: desde fármacos y protectores de cultivos hasta recubrimientos resistentes a manchas. Su potencia proviene de los enlaces carbono–flúor, entre los más fuertes de la química orgánica, lo que hace que estos compuestos sean especialmente estables en el organismo y en el medio ambiente. Esa misma dureza, sin embargo, dificulta su modificación deliberada. Este estudio presenta una forma suave de romper un enlace carbono–flúor específico en cadenas fluoradas largas y sustituirlo por un enlace carbono–carbono útil, lo que podría ayudar a los químicos a diseñar mejores fármacos y materiales a partir de estas moléculas persistentes.
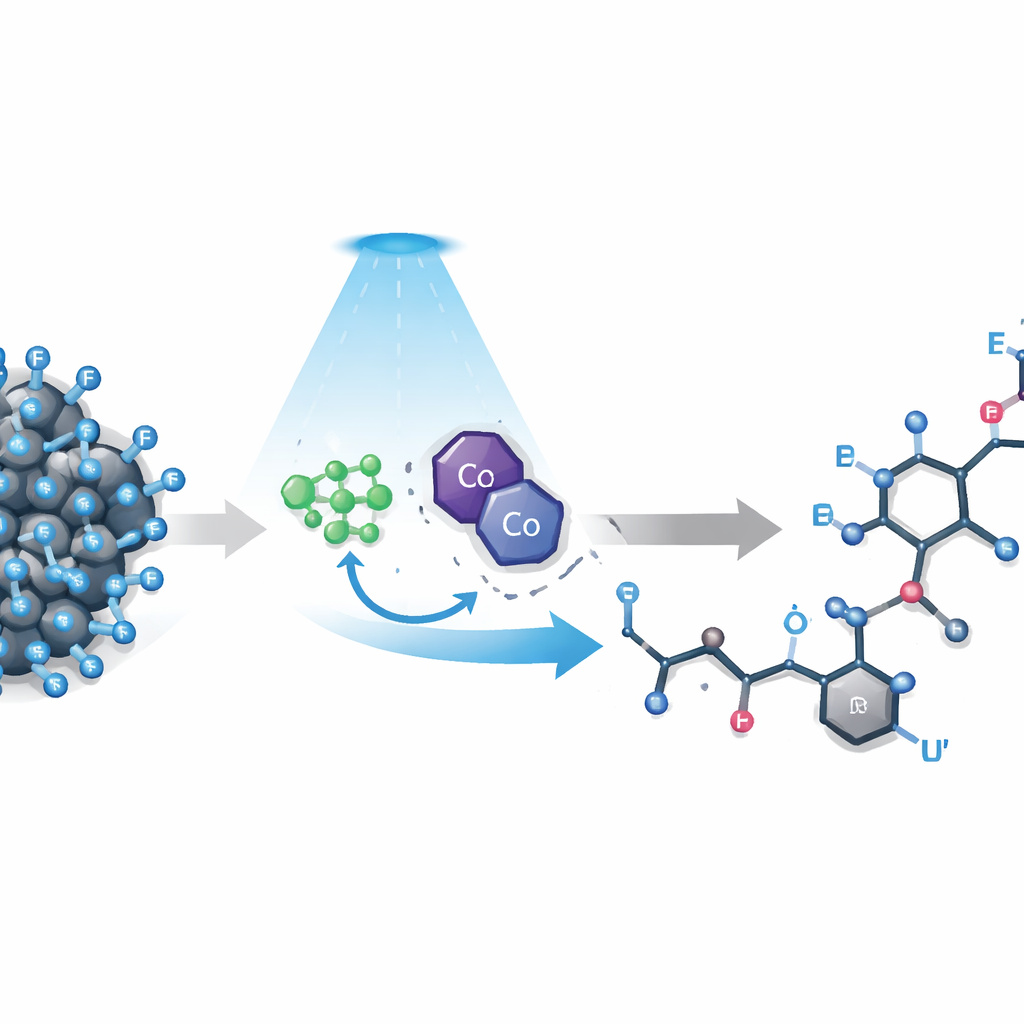
El reto de cortar el enlace más resistente
Los compuestos polifluoroalquílicos contienen cadenas en las que muchos hidrógenos han sido reemplazados por flúor. Estas cadenas confieren a las moléculas propiedades repelentes al agua y gran resistencia química, cualidades atractivas para la tecnología y la medicina pero problemáticas cuando los químicos quieren ajustar su comportamiento. Los métodos existentes se centran en el grupo fluorinado más simple, CF3, o requieren aditivos muy reactivos y socios de acoplamiento preformados. Las cadenas más largas, comunes en productos reales, son aún más difíciles de controlar: la fuerte atracción del flúor desestabiliza los intermedios reactivos, los voluminosos átomos de flúor dificultan el acceso, y los electrones pueden fluir en sentido inverso para deshacer pasos iniciales. En consecuencia, los intentos de romper un enlace carbono–flúor elegido a menudo conducen a mezclas caóticas o fracasan por completo.
Un enfoque con dos catalizadores impulsado por la luz
Los autores desarrollaron una estrategia que combina dos catalizadores cooperantes y luz visible para domar estas moléculas difíciles. Un complejo de iridio fotosensible dona primero un electrón al compuesto polifluoroalquílico, debilitando lo justo un enlace carbono–flúor hasta que se rompe y libera un fragmento fluorinado de corta vida conocido como radical. Al mismo tiempo, un catalizador de cobalto, inspirado en la vitamina B12, guía el lugar donde finalmente se añadirá un átomo de hidrógeno. Un reactivo de boro actúa como una “esponja de fluoruro”, atrapando el flúor expulsado e impidiendo que se recombine o que transporte electrones hacia atrás. Bajo iluminación suave con LED azules, esta red de auxiliares conduce la reacción por una vía productiva y altamente selectiva.
Formar nuevos enlaces con alquenos sencillos
Una vez formados, los radicales fluorados se añaden a alquenos corrientes —pequeñas moléculas con un doble enlace carbono–carbono—, creando nuevos enlaces carbono–carbono en un solo paso. El catalizador de cobalto transfiere luego un átomo de hidrógeno a una posición vecina específica, fijando un fragmento “alílico” mientras se conserva el doble enlace útil. En docenas de ensayos, el método funcionó con una amplia gama de alquenos, incluidos terpenos naturales complejos, y con muchos materiales iniciales ricos en flúor que llevaban cadenas de tres a diez carbonos o grupos amida fluorados. De manera notable, incluso cuando los alquenos contenían varios sitios alílicos C–H casi idénticos, la reacción eligió una posición con una selectividad superior a 20 a 1, evitando el enredo de isómeros que suele complicar esta química.
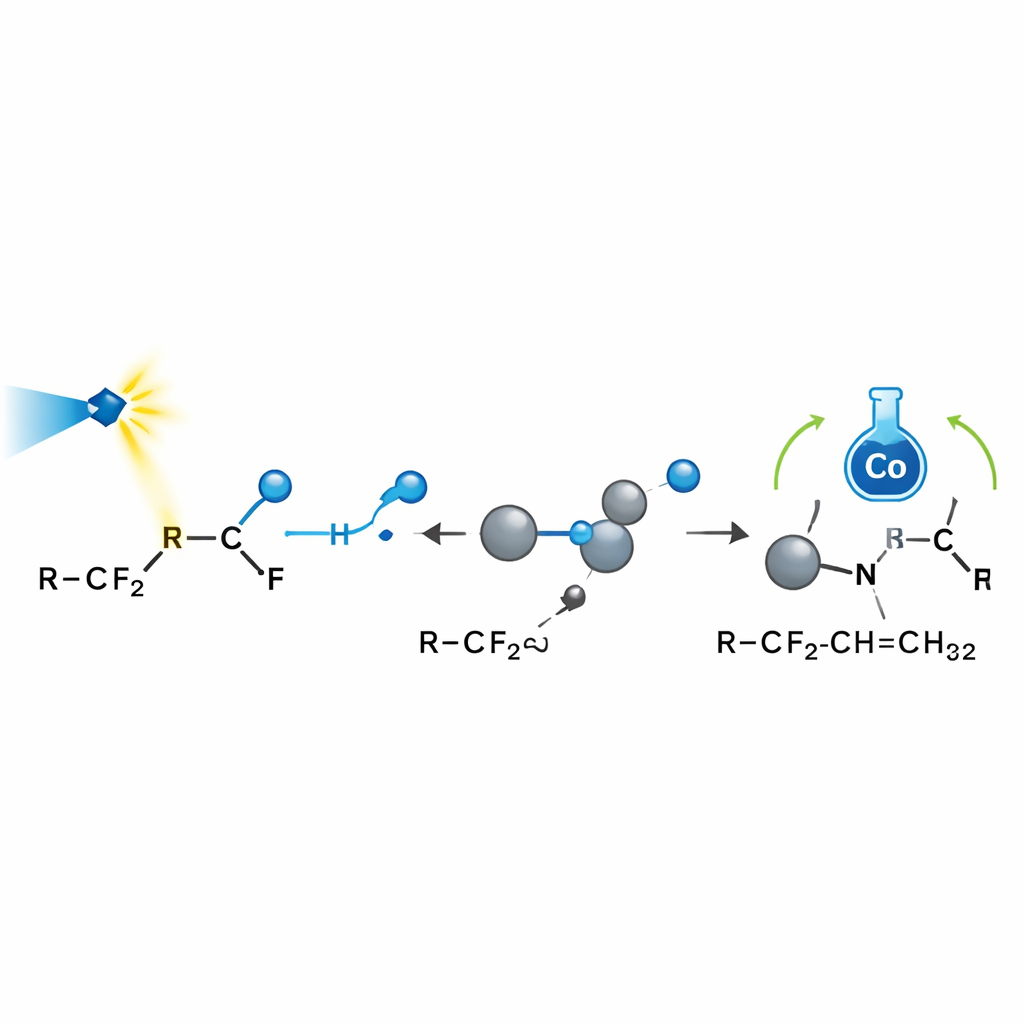
Sondeando el origen de la selectividad
Para entender por qué la reacción es tan selectiva, el equipo combinó sondas de laboratorio con modelado por ordenador. Trampas para radicales y experimentos de apertura de anillos confirmaron que los radicales fluorados son protagonistas clave. Mediciones de spin electrónico mostraron que el dióxido de carbono también puede reducirse a un anión reactivo que ayuda a activar ciertas amidas fluoradas. Señales de resonancia magnética nuclear revelaron que el reactivo de boro efectivamente captura el fluoruro libre. Los cálculos cuántico‑químicos cartografiaron el paisaje energético de cada paso, mostrando que después de que el radical se añade al alqueno, el cobalto prefiere entregar el hidrógeno a un sitio concreto porque afronta menos congestión estérica y se beneficia de interacciones atractivas favorables. Esto explica tanto por qué solo reacciona una posición alílica como por qué los productos favorecen fuertemente una única disposición geométrica alrededor del doble enlace.
Qué significa este avance en la práctica
Al orquestar luz, un catalizador metálico y un aditivo captador de fluoruro, este trabajo convierte algunos de los enlaces carbono–flúor más difíciles en conexiones carbono–carbono diseñables sin condiciones duras ni materiales de partida elaborados. En términos cotidianos, el método transforma fragmentos fluorados extremadamente inertes en bloques de construcción flexibles que pueden unirse a alquenos sencillos de manera predecible. Esto abre una vía para diseñar andamiajes fluorados a medida para farmacéuticos, agroquímicos y materiales avanzados, a la vez que ofrece nuevas herramientas para replantear cómo podrían transformarse las sustancias fluoradas persistentes en lugar de simplemente tolerarlas.
Cita: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
Palabras clave: moléculas fluoradas, catálisis fotoredox, catálisis con cobalto, reacciones radicalarias, funcionalización de alquenos