Clear Sky Science · nl
Radicale defluoroallylering van polyfluoralkylverbindingen met alkenen via synergistische fotoredox/cobaltkatalyse
Waarom het veranderen van hardnekkige fluorrijke moleculen ertoe doet
Fluorrijke chemicaliën zijn alomtegenwoordig in het moderne leven, van geneesmiddelen en gewasbeschermingsmiddelen tot vlekbestendige coatings. Hun kracht komt voort uit koolstof–fluorbindingen die tot de sterkste in de organische chemie behoren, waardoor deze verbindingen buitengewoon stabiel zijn in het lichaam en het milieu. Diezelfde hardheid maakt ze echter moeilijk doelgericht te modificeren. Deze studie introduceert een milde manier om één specifieke koolstof–fluorbinding in lange gefluorineerde ketens door te knippen en te vervangen door een nuttige koolstof–koolstofverbinding, wat chemici kan helpen betere medicijnen en materialen te ontwerpen uit deze koppige moleculen.
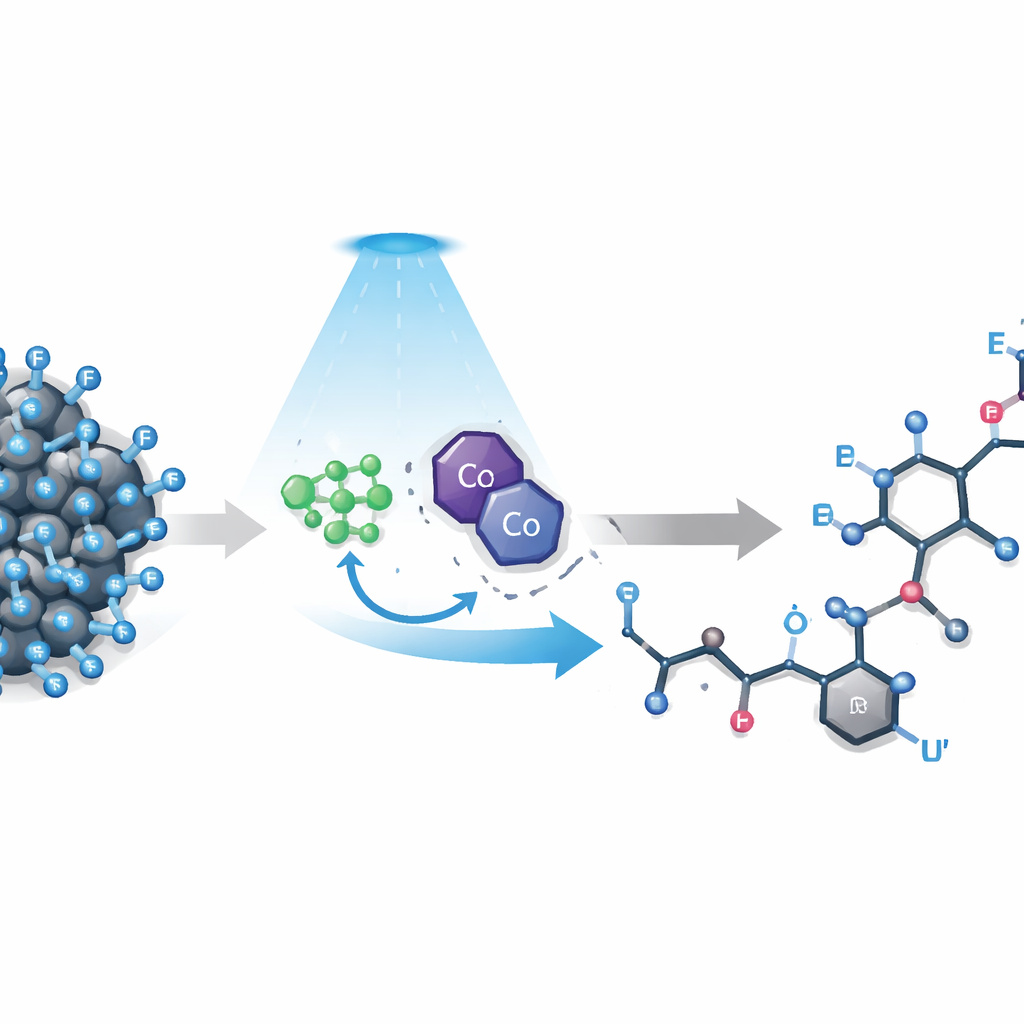
De uitdaging van het verbreken van de sterkste binding
Polyfluoroalkylverbindingen bevatten ketens waarin veel waterstoffen door fluor zijn vervangen. Deze ketens maken moleculen waterafstotend en chemisch veerkrachtig, wat aantrekkelijk is voor technologie en geneeskunde maar problematisch wanneer chemici hun gedrag willen bijsturen. Bestaande methoden concentreren zich doorgaans op de eenvoudigste gefluorideerde groep, CF3, of vereisen sterk reagerende additieven en vooraf gemaakte koppelingpartners. Langere ketens, die vaak in echte producten voorkomen, zijn nog moeilijker te beheersen: de sterke elektronegatieve werking van fluor destabiliseert reactieve tussenproducten, de volumineuze fluoratomen blokkeren toegang, en elektronen kunnen achterwaarts stromen om vroege stappen ongedaan te maken. Daardoor leiden pogingen om één gekozen koolstof–fluorbinding te verbreken vaak tot rommelige mengsels of tot complete mislukking.
Een tweekatalysatorbenadering aangedreven door licht
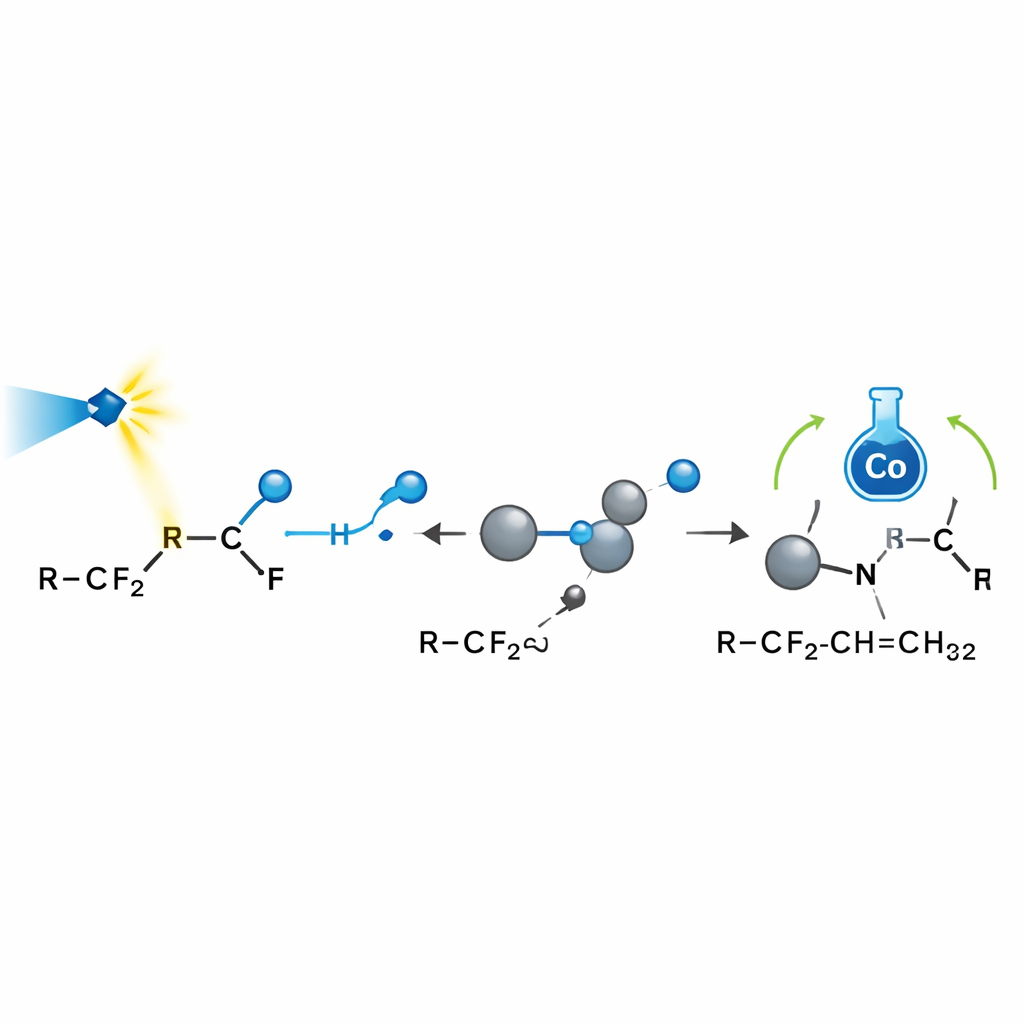
De auteurs ontwikkelden een strategie die twee samenwerkende katalysatoren en zichtbaar licht inzet om deze lastige moleculen te temmen. Een lichtgevoelig iridiumcomplex geeft eerst één elektron af aan een polyfluoroalkylverbinding, waardoor één koolstof–fluorbinding net genoeg verzwakt om te breken en een kortlevend gefluorideerd fragment, een radicaal, vrij te laten. Tegelijk leidt een cobaltkatalysator, geïnspireerd op vitamine B12, waar uiteindelijk een waterstofatoom zal worden toegevoegd. Een eenvoudig boorreagens fungeert als een "fluoride‑spons" die het uitgestoten fluoride vangt en voorkomt dat het weer recombineert of elektronen achterwaarts transporteert. Onder milde blauw‑LED‑belichting kanaliseert dit netwerk van hulpstoffen de reactie langs een productief, zeer selectief pad.
Nieuwe bindingen vormen met eenvoudige alkenen
Eenmaal gevormd voegen de gefluorideerde radicalen zich bij alledaagse alkenen—kleine moleculen met een koolstof–koolstof dubbele binding—en creëren zo in één stap nieuwe koolstof–koolstofverbindingen. De cobaltkatalysator draagt vervolgens een waterstofatoom over naar een specifiek aangrenzend koolstofatoom, waarmee een "allyl"‑fragment wordt vastgelegd terwijl de nuttige dubbele binding behouden blijft. Over tientallen experimenten werkte de methode met een breed scala aan alkenen, inclusief complexe natuurlijke terpenen, en met veel verschillende fluorrijke uitgangsmaterialen met ketens van drie tot tien koolstofatomen of gefluorideerde amidegroepen. Opmerkelijk is dat zelfs wanneer alkenen meerdere bijna identieke allylische C–H‑plaatsen bevatten, de reactie één positie kiest met een selectiviteit beter dan 20‑op‑1, waardoor de reeks isomeren die zulke chemie gewoonlijk lastig maakt, wordt vermeden.
Onderzoeken hoe selectiviteit ontstaat
Om te begrijpen waarom de reactie zo selectief is, combineerde het team laboratoriumproeven met computermodellering. Chemische "radicaalvangers" en ringopeningsproeven bevestigden dat gefluorideerde radicalen sleutelspelers zijn. Elektron‑spinmetingen toonden aan dat kooldioxide ook tot een reactieve anion kan worden gereduceerd dat helpt bepaalde gefluorideerde amiden te activeren. Kernspinresonantiesignalen onthulden dat het boorreagens inderdaad vrij fluoride opvangt. Kwantumchemische berekeningen brachten het energielandschap van elke stap in kaart en toonden aan dat nadat het radicaal zich aan een alkeen heeft gehecht, cobalt de voorkeur geeft aan het afleveren van waterstof aan één specifieke positie omdat daar minder sterische hinder is en er gunstige aantrekkingsinteracties optreden. Dit verklaart zowel waarom slechts één allylische positie reageert als waarom de producten sterk de voorkeur geven aan één geometrische ordening rond de dubbele binding.
Wat deze vooruitgang in de praktijk betekent
Door licht, een metalen katalysator en een fluoridebindend additief te orkestreren, zet dit werk enkele van de hardste koolstof–fluorbindingen om in ontworpen koolstof–koolstofverbindingen zonder harde voorwaarden of ingewikkelde uitgangsmaterialen. In alledaagse termen verandert de methode extreem inerte gefluorideerde fragmenten in flexibele bouwstenen die op een voorspelbare manier aan eenvoudige alkenen kunnen worden gekoppeld. Dit opent een route naar op maat gemaakte gefluorideerde structuren voor geneesmiddelen, agrochemicaliën en geavanceerde materialen, terwijl het ook nieuwe instrumenten biedt om na te denken over hoe persistente gefluorideerde stoffen kunnen worden getransformeerd in plaats van simpelweg geaccepteerd.
Bronvermelding: Ren, D., Deng, S., Wang, Y. et al. Radical defluoroallylation of polyfluoroalkyl compounds with alkenes via synergistic photoredox/cobalt catalysis. Nat Commun 17, 2971 (2026). https://doi.org/10.1038/s41467-026-68840-3
Trefwoorden: gefluorideerde moleculen, fotoredoxkatalyse, cobaltkatalyse, radicalaire reacties, alkeenfunctionalizatie