Clear Sky Science · zh
乳酸介导的NK细胞功能障碍作为乳腺癌的预后标志和治疗靶点
当肿瘤能量反噬免疫系统时
我们的身体持续产生乳酸,这是一种在运动时常让肌肉感到灼热的简单分子。然而在许多癌症中,肿瘤大量产生乳酸,足以重塑其周围环境。本研究展示了乳腺肿瘤中过量乳酸如何悄然抑制自然杀伤(NK)细胞——这些是前线免疫防御者——以及阻断乳酸的转运与信号传导如何可能恢复这些细胞的功能并改善患者预后。
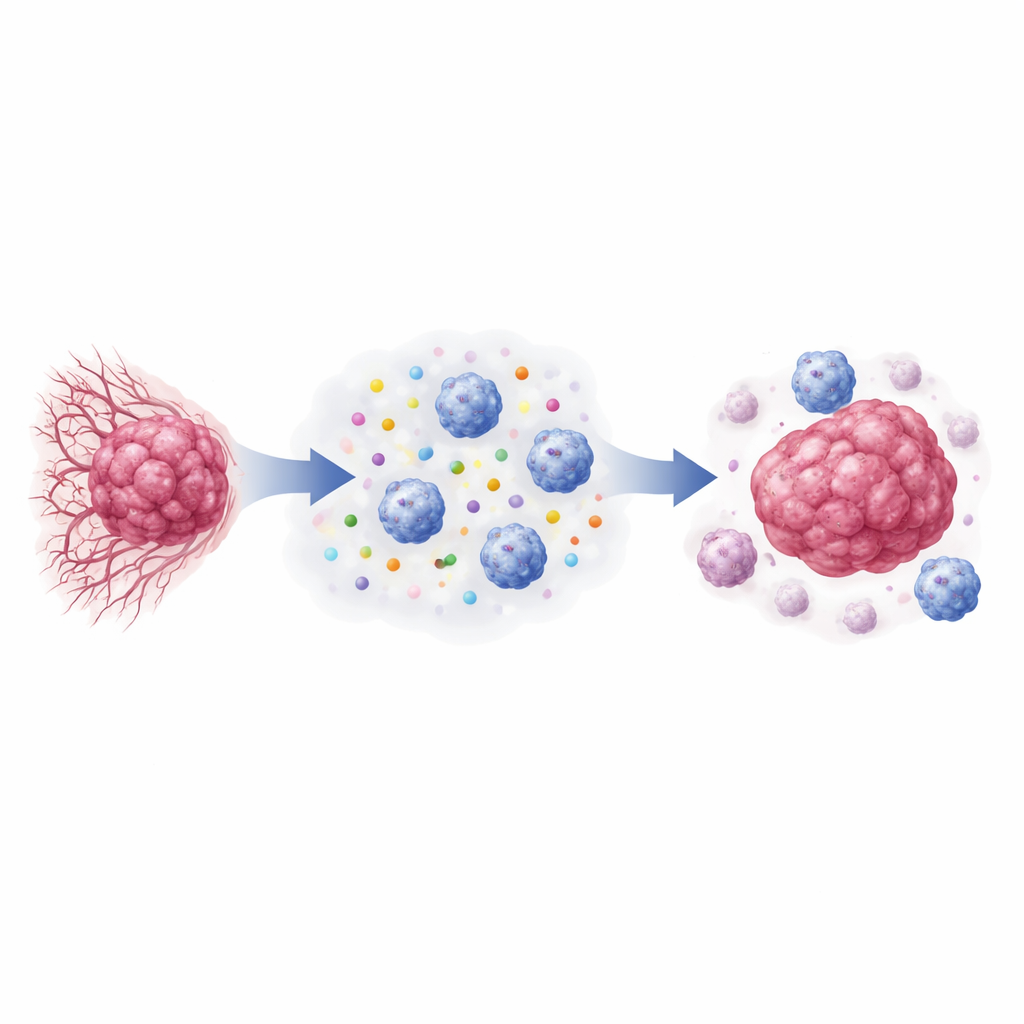
肿瘤化学与患者生存之间的隐秘关联
研究者首先分析了882名乳腺癌女性的基因表达数据。他们考察了驱动肿瘤细胞乳酸产生与感知的基因,以及标记NK细胞激活的基因。具有较高乳酸相关基因活性,尤其是LDHA和编码乳酸受体GPR81的HCAR1的肿瘤,持续表现出较低的NK细胞激活受体表达。即便在校正了年龄、肿瘤大小、激素受体状态等临床因素后,呈现“高乳酸、低NK活性”特征的患者仍有更短的无复发生存期。相反,那些乳酸代谢低而NK激活信号强的肿瘤,患者随时间表现较好。
过量乳酸如何削弱免疫攻击
为了解高乳酸水平对NK细胞的实际影响,研究团队从健康供体分离出NK细胞,并将其暴露于与侵袭性乳腺肿瘤内相似的乳酸浓度中。两天内,NK细胞增殖变慢但并未死亡,显示出一种功能性的“刹车”而非细胞丧失。表面表型指示作战准备的标记以及关键的激活受体下降。细胞内强效杀伤因子干扰素-γ和颗粒酶B的水平也降低。高级成像和代谢测量显示,乳酸重塑了NK细胞的内部代谢:线粒体能量产出减少,氧气消耗下降,脂样分子积累,均为一种迟缓、能量匮乏状态的特征。
阻断招募并压制肿瘤信号
除削弱单个NK细胞外,乳酸还妨碍它们到达肿瘤的位置。在模拟肿瘤三维结构的微流控装置中,NK细胞向浸泡在乳酸中的乳腺癌球体的迁移明显受阻。乳酸丰富通道中的肿瘤结构显示出更少的细胞死亡,表明到达的NK细胞更少且即便到达也效能较差。对信号分子的测量表明乳酸降低了趋化因子CXCL9和CXCL10的产生,这些因子通常有助于引导与激活NK细胞。尽管癌细胞展示了可被NK细胞识别的分子“标志”,但招募不足加上颗粒释放(去颗粒化)受抑,使肿瘤在很大程度上未受到挑战。
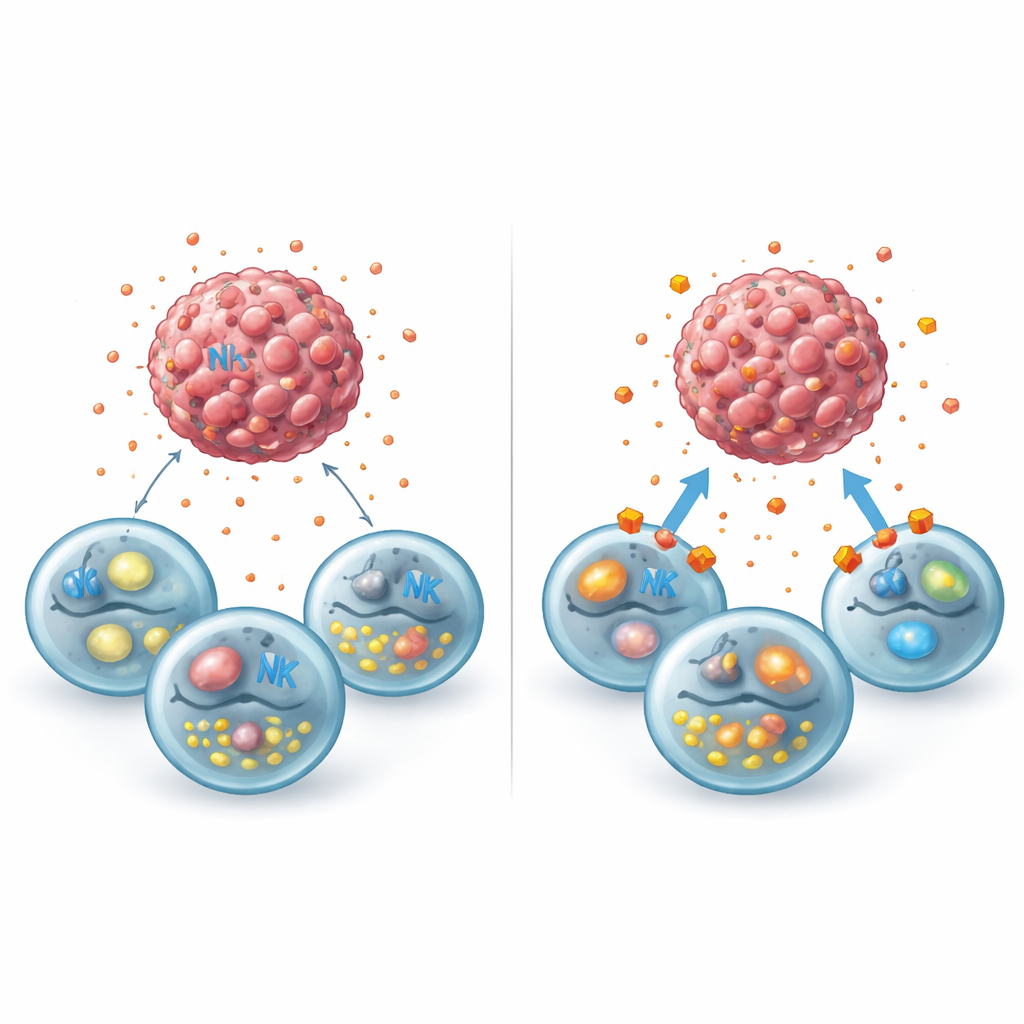
关闭乳酸通路以唤醒防御
研究接着探讨切断乳酸转运是否能消除这种代谢性迷雾。研究者用syrosingopine处理乳腺癌细胞,这是一种阻断两种关键转运蛋白(MCT1和MCT4)以阻止乳酸跨膜转运的药物,并用第二种药物鸡尾酒选择性抑制各转运体。这些处理使乳酸被困在肿瘤细胞内,减少了其释放到环境中,并在所用剂量下并未直接杀死肿瘤。然而,当加入人NK细胞时,情况发生改变:肿瘤球体更明显收缩,细胞内凋亡标志增加,NK细胞即便在被外加乳酸的存在下也恢复了去颗粒化能力。与此同时,对公开数据集的分析显示,在乳腺癌细胞中关闭GPR81乳酸受体会将其重编程为显示更多刺激NK的信号并减少帮助其掩藏或抵抗攻击的分子。
这对未来乳腺癌治疗意味着什么
总体而言,这些发现表明乳酸并非乳腺肿瘤中的单纯代谢“废物”——它是早期免疫防御的主动抑制因子。高乳酸水平及其受体的强烈信号传导有助于营造一种微环境,使NK细胞到达更少、工作效率更低且能量利用不佳。通过阻断乳酸转运或其受体,本研究表明可以恢复NK细胞活性并在现实的三维模型中增加肿瘤细胞死亡。对患者而言,这项工作提示测量乳酸相关基因或能帮助预测预后,而针对乳酸通路的药物未来可能与基于NK细胞的疗法及其他免疫治疗形式结合,将代谢上不利的肿瘤转变为免疫可控的战场。
引用: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
关键词: 乳腺癌, 乳酸代谢, 自然杀伤细胞, 肿瘤微环境, 癌症免疫治疗