Clear Sky Science · fr
La dysfonction des cellules NK médiée par le lactate comme marqueur pronostique et cible thérapeutique dans le cancer du sein
Quand le carburant tumoral se retourne contre le système immunitaire
Notre organisme produit en permanence du lactate, une molécule simple surtout connue pour provoquer la sensation de brûlure musculaire lors de l’exercice. Dans de nombreux cancers, cependant, les tumeurs produisent tellement de lactate qu’elles modifient leur environnement local. Cette étude montre comment un excès de lactate dans les tumeurs mammaires peut silencieusement inhiber les cellules tueuses naturelles (NK) — des défenseurs immunitaires de première ligne — et comment bloquer le transport et les signaux du lactate pourrait réactiver ces cellules et améliorer les résultats pour les patientes.
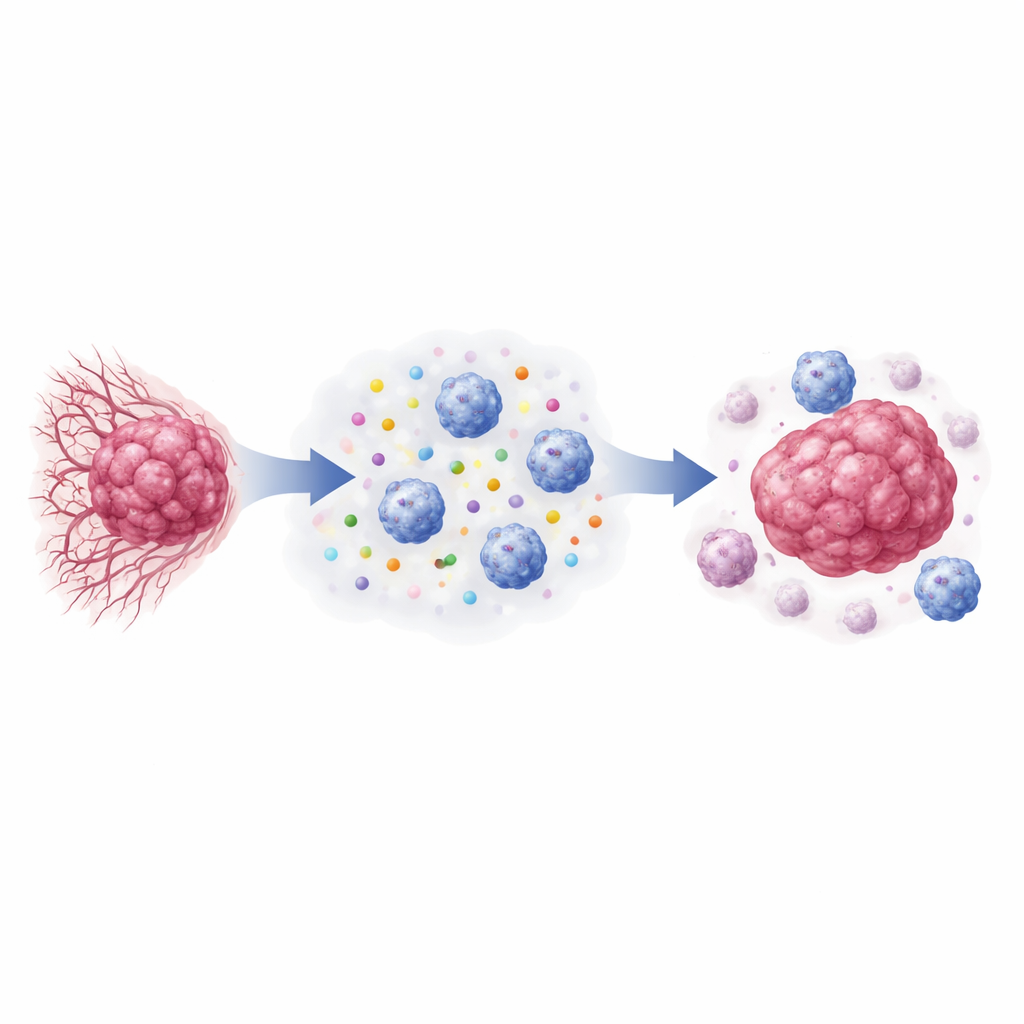
Un lien caché entre la chimie tumorale et la survie des patientes
Les chercheurs se sont d’abord appuyés sur des données d’expression génique de 882 femmes atteintes de cancer du sein. Ils ont examiné les gènes qui gouvernent la production et la détection du lactate dans les cellules tumorales, parallèlement aux gènes marquant l’activation des cellules NK. Les tumeurs présentant une activité plus élevée des gènes liés au lactate, en particulier LDHA et HCAR1 (qui code pour le récepteur du lactate GPR81), affichaient systématiquement une expression moindre des récepteurs d’activation des NK. Les patientes dont les tumeurs présentaient ce profil « fort lactate, faible activité NK » ont connu des périodes sans récidive plus courtes, même après ajustement sur l’âge, la taille tumorale, le statut des récepteurs hormonaux et d’autres facteurs cliniques. En revanche, les femmes dont les tumeurs associaient un métabolisme du lactate faible et des signaux d’activation NK marqués avaient tendance à évoluer plus favorablement dans le temps.
Comment un excès de lactate affaiblit l’attaque immunitaire
Pour comprendre ce que des niveaux élevés de lactate font réellement aux cellules NK, l’équipe a isolé des NK de donneurs sains et les a exposées à des concentrations de lactate comparables à celles observées dans les tumeurs mammaires agressives. Sur deux jours, les NK ont proliféré plus lentement mais n’ont pas péri, révélant une sorte de « frein » fonctionnel plutôt qu’une perte cellulaire massive. Les marqueurs de surface indiquant leur préparation au combat, ainsi que des récepteurs activateurs clés, ont diminué. À l’intérieur des cellules, les niveaux d’effecteurs cytotoxiques puissants, comme l’interféron-gamma et la granzyme B, ont chuté. L’imagerie avancée et les mesures métaboliques ont montré que le lactate remodelait la chimie interne des NK : leurs mitochondries produisaient moins d’énergie, l’utilisation d’oxygène diminuait et des molécules de type lipidique s’accumulaient, autant de signes d’un état ralenti et en manque d’énergie.
Bloquer le recrutement et étouffer les signaux tumoraux
Au-delà de l’affaiblissement des NK individuellement, le lactate gênait aussi leur arrivée au niveau tumoral. Dans de petits dispositifs microfluidiques reproduisant la structure tridimensionnelle des tumeurs, les NK migraient beaucoup moins efficacement vers des sphéroïdes de cancer du sein baignés de lactate. Les structures tumorales dans les canaux riches en lactate montraient beaucoup moins de mort cellulaire, indiquant que moins de NK arrivaient et que celles qui atteignaient la tumeur étaient moins efficaces. Les mesures des molécules de signalisation ont révélé que le lactate réduisait la production des chimiokines CXCL9 et CXCL10, qui aident normalement à guider et activer les NK. Bien que les cellules cancéreuses affichent les « drapeaux » moléculaires nécessaires pour être reconnues par les NK, la combinaison d’un recrutement médiocre et d’une dégranulation amoindrie (libération des granules toxiques) laissait les tumeurs essentiellement sans opposition.
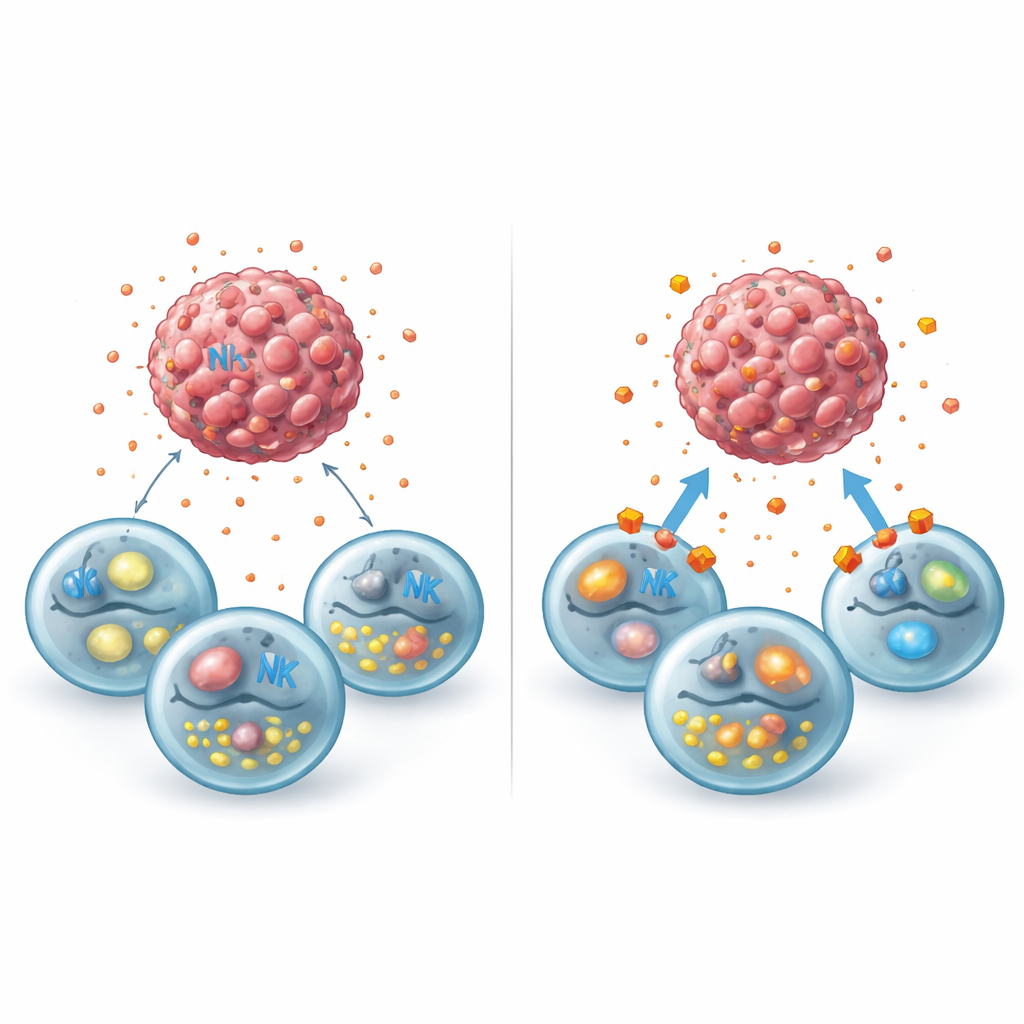
Fermer les voies du lactate pour réveiller les défenses
L’étude a ensuite testé si bloquer le transport du lactate pouvait dissiper ce brouillard métabolique. Les chercheurs ont traité des cellules de cancer du sein avec la syrosingopine, un médicament qui bloque deux transporteurs clés (MCT1 et MCT4) responsables du passage du lactate à travers la membrane cellulaire, ainsi qu’avec un cocktail de médicaments inhibant sélectivement chaque transporteur. Ces traitements ont piégé le lactate à l’intérieur des cellules tumorales, réduit sa libération dans l’environnement et n’ont pas tué directement les tumeurs aux doses utilisées. Lorsque des NK humaines y ont été ajoutées, cependant, le tableau a changé : les sphéroïdes tumoraux ont davantage rétréci, les marqueurs internes d’apoptose ont augmenté et les NK ont retrouvé leur capacité de dégranuler, même en présence d’un apport externe de lactate. Parallèlement, des analyses de jeux de données publics ont montré que l’inactivation du récepteur du lactate GPR81 dans les cellules de cancer du sein les reprogrammait pour afficher davantage de signaux stimulant les NK et moins de molécules les aidant à se cacher ou à résister à l’attaque.
Ce que cela signifie pour le traitement futur du cancer du sein
Dans l’ensemble, ces résultats montrent que le lactate n’est pas seulement un « déchet » métabolique dans les tumeurs mammaires — c’est un suppresseur actif des défenses immunitaires précoces. Des niveaux élevés de lactate et une signalisation forte via son récepteur contribuent à créer un microenvironnement où les NK arrivent moins souvent, fonctionnent moins bien et dépensent mal leur énergie. En bloquant le transport du lactate ou son récepteur, l’étude montre qu’il est possible de restaurer l’activité des NK et d’augmenter la mort des cellules tumorales dans des modèles tridimensionnels réalistes. Pour les patientes, ces travaux suggèrent que mesurer les gènes liés au lactate pourrait aider à prédire le pronostic, et que des médicaments ciblant les voies du lactate pourraient un jour être associés à des thérapies à base de NK et à d’autres formes d’immunothérapie pour transformer des tumeurs métaboliquement hostiles en terrains où le système immunitaire peut reprendre l’avantage.
Citation: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
Mots-clés: cancer du sein, métabolisme du lactate, cellules tueuses naturelles, <keyword>immunothérapie contre le cancer