Clear Sky Science · ru
Дисфункция NK‑клеток, вызванная лактатом, как прогностический маркер и терапевтическая цель при раке груди
Когда топливо опухоли оборачивается против иммунной системы
Наш организм постоянно производит лактат — простую молекулу, наиболее известную тем, что вызывает «жжение» в мышцах при нагрузке. Однако при многих видах рака опухоли вырабатывают лактат в таких больших количествах, что он перестраивает их окружение. В этом исследовании показано, как избыток лактата в опухолях молочной железы тихо выключает клетки‑NK — передовой элемент иммунной защиты — и как блокирование транспорта и сигнальных путей лактата может вернуть этим клеткам активность и улучшить исходы для пациентов.
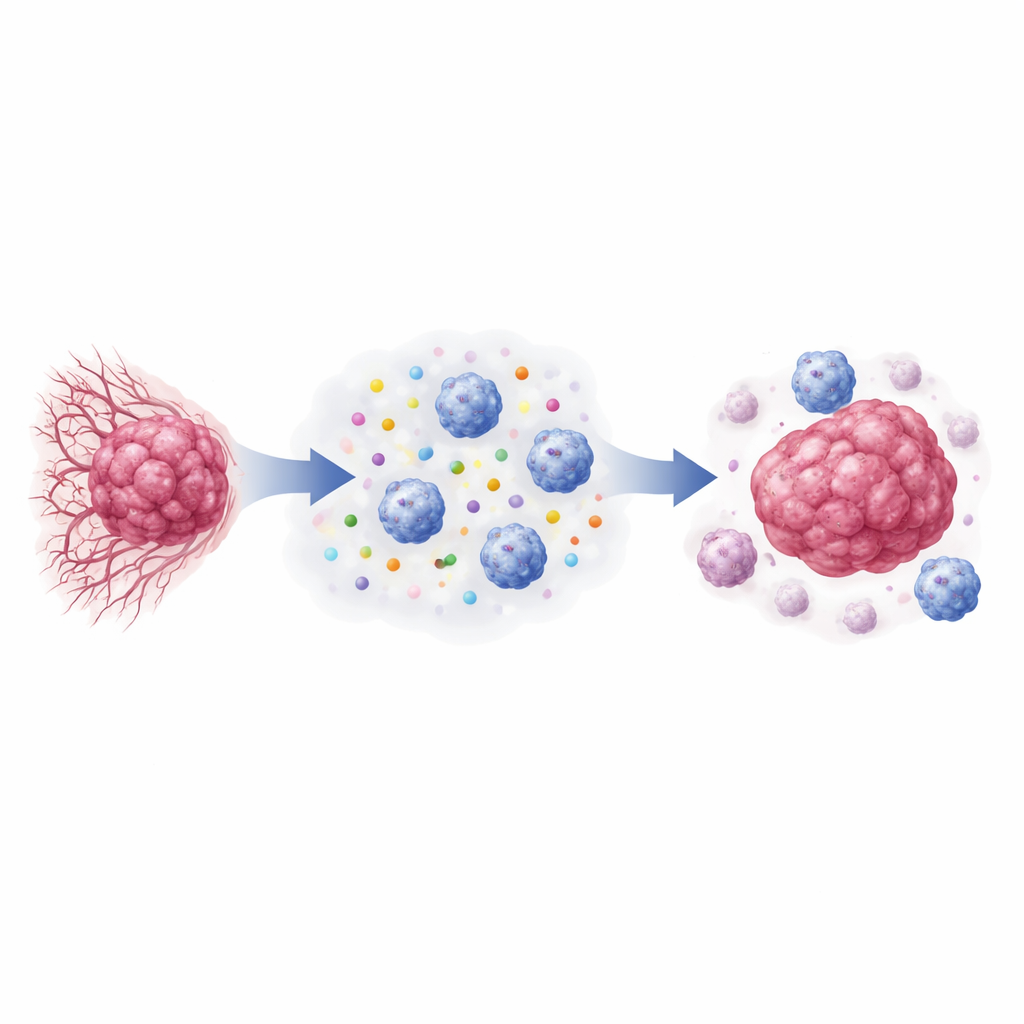
Скрытая связь между химией опухоли и выживаемостью пациентов
Исследователи сначала проанализировали данные экспрессии генов у 882 женщин с раком молочной железы. Они изучали гены, отвечающие за производство и восприятие лактата в опухолевых клетках, а также гены‑маркеры активации NK‑клеток. Опухоли с повышенной активностью лактат‑ассоциированных генов, особенно LDHA и HCAR1 (кодирующий рецептор лактата GPR81), стабильно демонстрировали пониженную экспрессию рецепторов активации NK. Пациентки с опухолями, несущими подпись «высокий лактат, низкая активность NK», имели более короткие безрецидивные интервалы, даже с учётом возраста, размера опухоли, статуса гормональных рецепторов и других клинических факторов. Напротив, у женщин с сочетанием низкого лактатного метаболизма и сильных сигналов активации NK прогноз был более благоприятным.
Как избыток лактата ослабляет иммунную атаку
Чтобы понять, что именно делает высокий уровень лактата с NK‑клетками, команда выделила NK‑клетки у здоровых доноров и подвергла их воздействию концентраций лактата, сопоставимых с таковыми в агрессивных опухолях молочной железы. В течение двух дней NK‑клетки росли медленнее, но не умирали, что указывает на функциональное «торможение», а не на массовую гибель клеток. Поверхностные маркеры готовности к бою и ключевые активирующие рецепторы снижались. Внутри клеток падали уровни мощных цитотоксических молекул — интерферона‑гамма и гранзима B. Продвинутая визуализация и метаболические измерения показали, что лактат перестраивает внутреннюю химию NK: митохондрии вырабатывали меньше энергии, потребление кислорода уменьшалось, накапливались липоподобные молекулы — все признаки вялого, энергетически истощённого состояния.
Блокируя привлечение и приглушая опухолевые сигналы
Кроме того, лактат мешал самому процессу привлечения NK‑клеток к опухоли. В крошечных микрофлюидных устройствах, имитирующих трёхмерную структуру опухоли, NK‑клетки мигрировали значительно менее эффективно к сфероидам рака груди, помещённым в лактатную среду. Структуры опухоли в каналах с высоким лактатом демонстрировали гораздо меньше клеточной гибели, что указывает на то, что меньше NK‑клеток добиралось до цели и те, что добирались, были менее эффективны. Измерения сигнальных молекул показали, что лактат снижает продукцию хемокинов CXCL9 и CXCL10, которые обычно направляют и активируют NK‑клетки. Хотя раковые клетки демонстрировали молекулярные «флажки», необходимые для распознавания NK, сочетание плохого рекрутирования и подавленной дегрануляции (выпуска токсических гранул) оставляло опухоли в значительной степени без вызова.
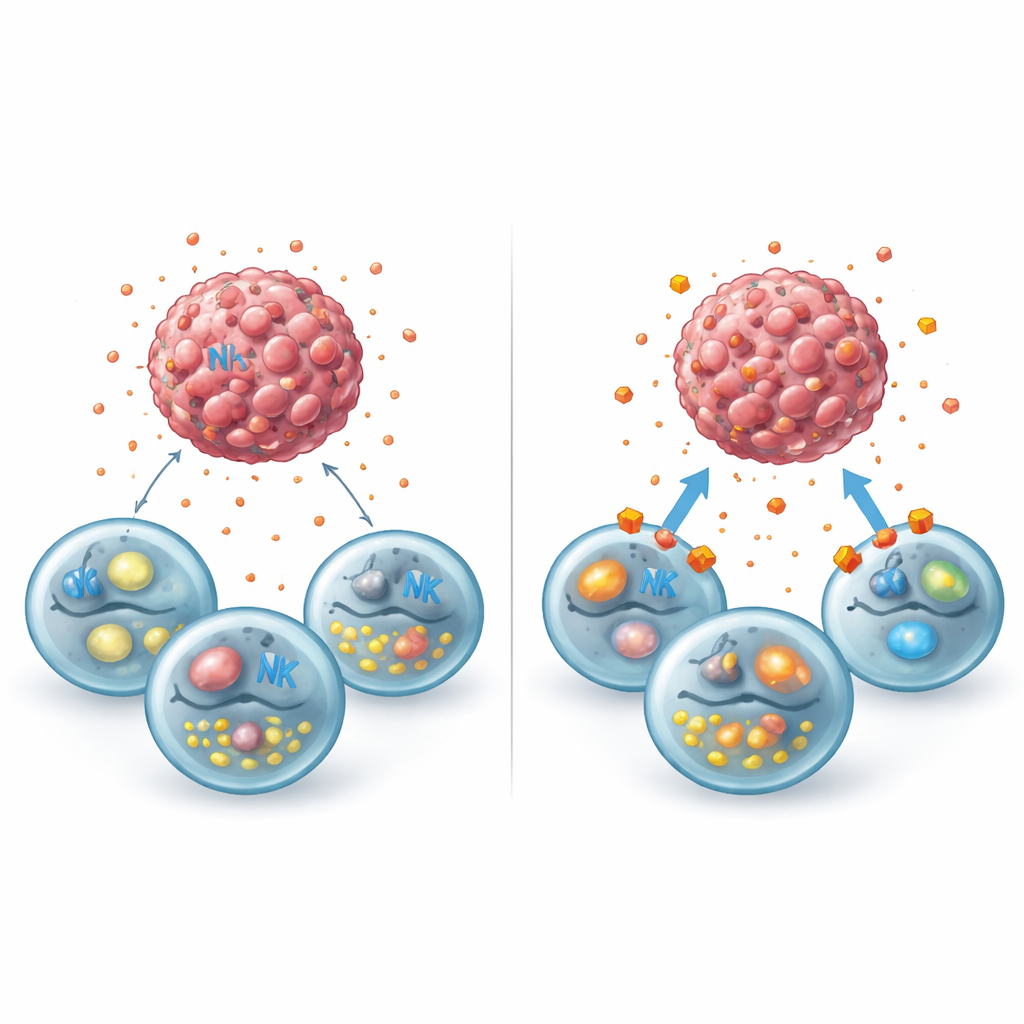
Перекрытие путей лактата, чтобы пробудить защиту
Дальнейшая часть работы задалась вопросом, не сможет ли прерывание транспорта лактата снять этот метаболический туман. Исследователи обработали клетки рака груди сирозингопином — препаратом, блокирующим два ключевых транспортёра (MCT1 и MCT4), ответственных за перенос лактата через мембрану, а также применили второй набор соединений, избирательно ингибирующих каждый транспортер. Эти вмешательства задерживали лактат внутри опухолевых клеток, уменьшали его выброс в окружение и при использованных дозах не убивали опухоли непосредственно. Однако после добавления человеческих NK‑клеток картина изменилась: сфероиды опухолей уменьшались сильнее, внутренние маркёры апоптоза повышались, и NK‑клетки вновь восстанавливали способность к дегрануляции, даже при наличии добавленного лактата. Параллельные анализы общедоступных наборов данных показали, что выключение рецептора лактата GPR81 в клетках рака груди перепрограммирует их так, что они проявляют больше сигналов, стимулирующих NK, и меньше молекул, помогающих скрываться или противостоять атаке.
Что это значит для будущего лечения рака груди
В целом результаты показывают, что лактат — это не просто метаболический «отход» в опухолях молочной железы, а активный подавитель ранней иммунной защиты. Высокие уровни лактата и сильная передача сигнала через его рецептор создают микросреду, в которой NK‑клетки приходят реже, действуют менее эффективно и быстрее теряют энергию. Блокирование транспорта лактата или его рецептора, как показано в исследовании, позволяет восстановить активность NK‑клеток и увеличить гибель опухолевых клеток в реалистичных трёхмерных моделях. Для пациентов это означает, что измерение экспрессии лактат‑связанных генов может помочь прогнозировать исход, а препараты, нацеленные на лактатные пути, возможно, в перспективе дадут эффект в сочетании с NK‑клеточной терапией и другими формами иммунотерапии, превращая метаболически враждебные опухоли в среду, где иммунная система сможет эффективно бороться.
Цитирование: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
Ключевые слова: рак груди, метаболизм лактата, клетки‑естественные киллеры, опухолевый микросреда, иммунотерапия рака