Clear Sky Science · he
דיספונקציית תאי NK ממסלולי לקטאט כסמן פרוגנוסטי ומטרה טיפולית בסרטן השד
כשדלק של הגידול פונה נגד המערכת החיסונית
גופנו מייצר באופן רציף לקטאט, מולקולה פשוטה המוכרת בעיקר כגורם לשרירים לשרוף בזמן פעילות גופנית. עם זאת, ברבים מהגידולים הסרטניים התאים מייצרים כמות כזו של לקטאט שהיא משנה את סביבתם. המחקר הזה מראה כיצד עודף לקטאט בגידולים של השד יכול להשתיק בהדרגה את תאי ה‑NK — חיילי הקו החזית של המערכת החיסונית — וכיצד חסימת תנועת הלקטאט והאותות שלו עשויה להשיב תפקוד לתאים אלה ולשפר את תוצאות המטופלות.
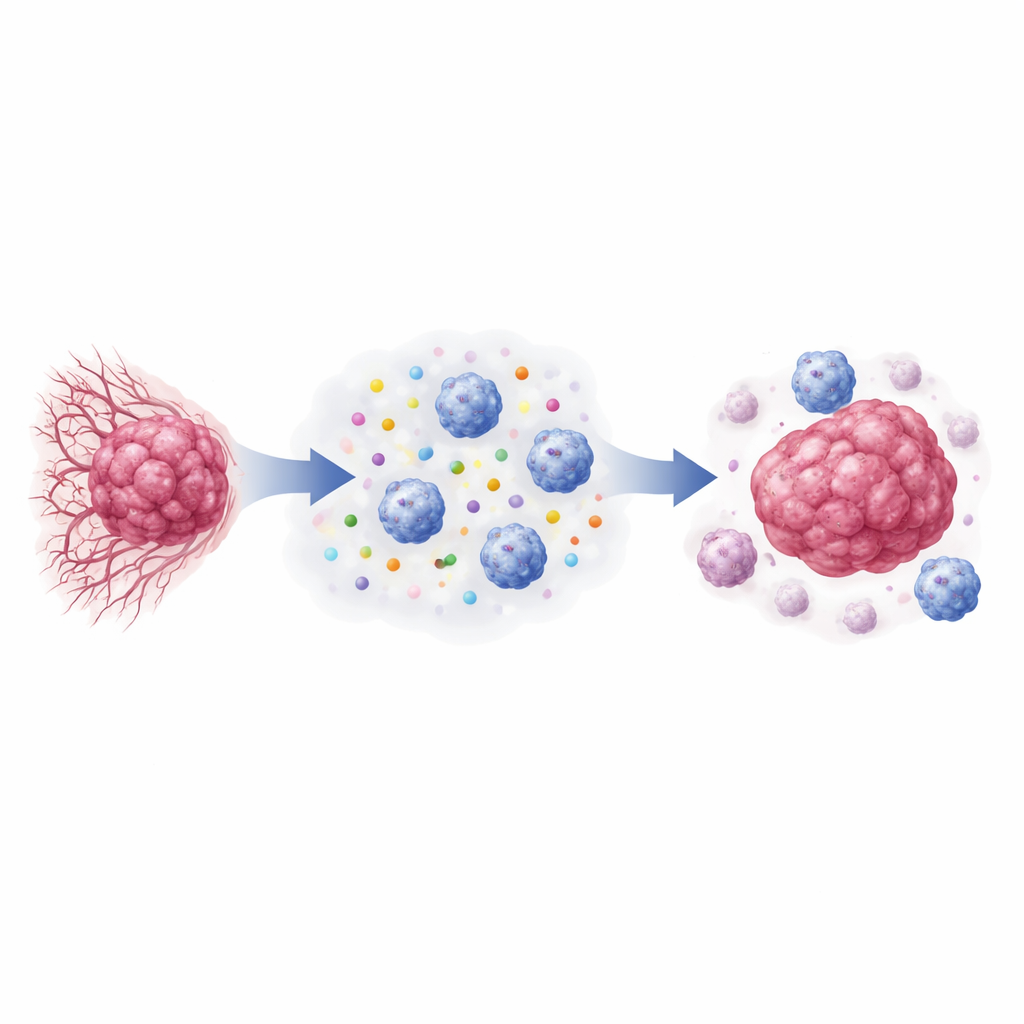
קישור סמוי בין כימיה של הגידול להישרדות המטופלות
החוקרים פנו תחילה לנתוני ביטוי גנים של 882 נשים עם סרטן השד. הם בחנו גנים שמניעים ייצור וחישה של לקטאט בתאי הגידול, לצד גנים שמסמנים הפעלת תאי NK. גידולים שבהם הייתה פעילות גבוהה של גנים הקשורים ללקטאט, במיוחד LDHA ו‑HCAR1 (המקודד לקולטן הלקטאט GPR81), הפגינו בקביעות ביטוי נמוך יותר של קולטנים המפעילים תאי NK. מטופלות שגידוליהן הציגו את החתימה של “לקטאט גבוה, פעילות NK נמוכה” חוו פרקי זמן קצרים יותר ללא חזרת המחלה, גם לאחר התחשבות בגיל, גודל הגידול, מצב קולטני ההורמונים וגורמים קליניים נוספים. לעומת זאת, נשים שגידוליהן שילבו מטבוליזם לקטאט נמוך עם אותות הפעלה חזקים של NK נטו להציג תוצאות טובות יותר לאורך זמן.
כיצד עודף לקטאט מחליש את ההתקפה החיסונית
כדי להבין מה גורמות רמות לקטאט גבוהות לתאי NK, הצוות בודד תאי NK מתורמים בריאים וחשף אותם לריכוזי לקטאט הדומים לאלו שנמצאו בתוך גידולים תוקפניים של השד. במשך יומיים תאי ה‑NK גדלו לאט יותר אך לא מתו, מה שמצביע על מעין “בלימה” תפקודית ולא על אובדן תאים מוחלט. סמני פני שטח שמציינים מוכנות להילחם, וכן קולטנים מפעילים מרכזיים, ירדו. בתוך התאים ירדו רמות הכלים הקטלניים החזקים אינטרפרון‑גמא וגרניזים B. הדמיות מתקדמות ומדידות מטבוליות הראו שלקטאט עיצב מחדש את הכימיה הפנימית של תאי NK: המיטוכונדריה ייצרה פחות אנרגיה, צריכת החמצן פחתה, ומולקולות שומניות הצטברו — כל אלה סימנים למצב איטי וחסר אנרגיה.
חסימת גיוס והשתקת אותות הגידול
מעבר להחלשת תאים בודדים, לקטאט גם הפריע לגיוסם של תאי NK אל הגידול מלכתחילה. במכשירים מיקרופלואידיים חיקוי־תלת־ממד של מבנה הגידול, תאי NK נודדו באופן משמעותי פחות ביעילות לעבר ספירות של סרטן השד שטבלו בלקטאט. המבנים הגידוליים בתעלות עשירות לקטאט הראו מוות תאי נמוך בהרבה, מה שמעיד שפחות תאי NK הגיעו והאלה שכן הגיעו היו פחות יעילים. מדידות של מולקולות איתות הראו שלקטאט הקטין את הייצור של הכרמוקינים CXCL9 ו‑CXCL10, שהן בדרך כלל מסייעות להנחות ולהפעיל תאי NK. אף על פי שתאי הסרטן הציגו את הדגלים המולקולריים המתאימים לזיהוי על ידי NK, השילוב של גיוס לקוי ובלימת שחרור הגרגרים הרעילים השאיר את הגידולים ברובם בלתי מאוימים.
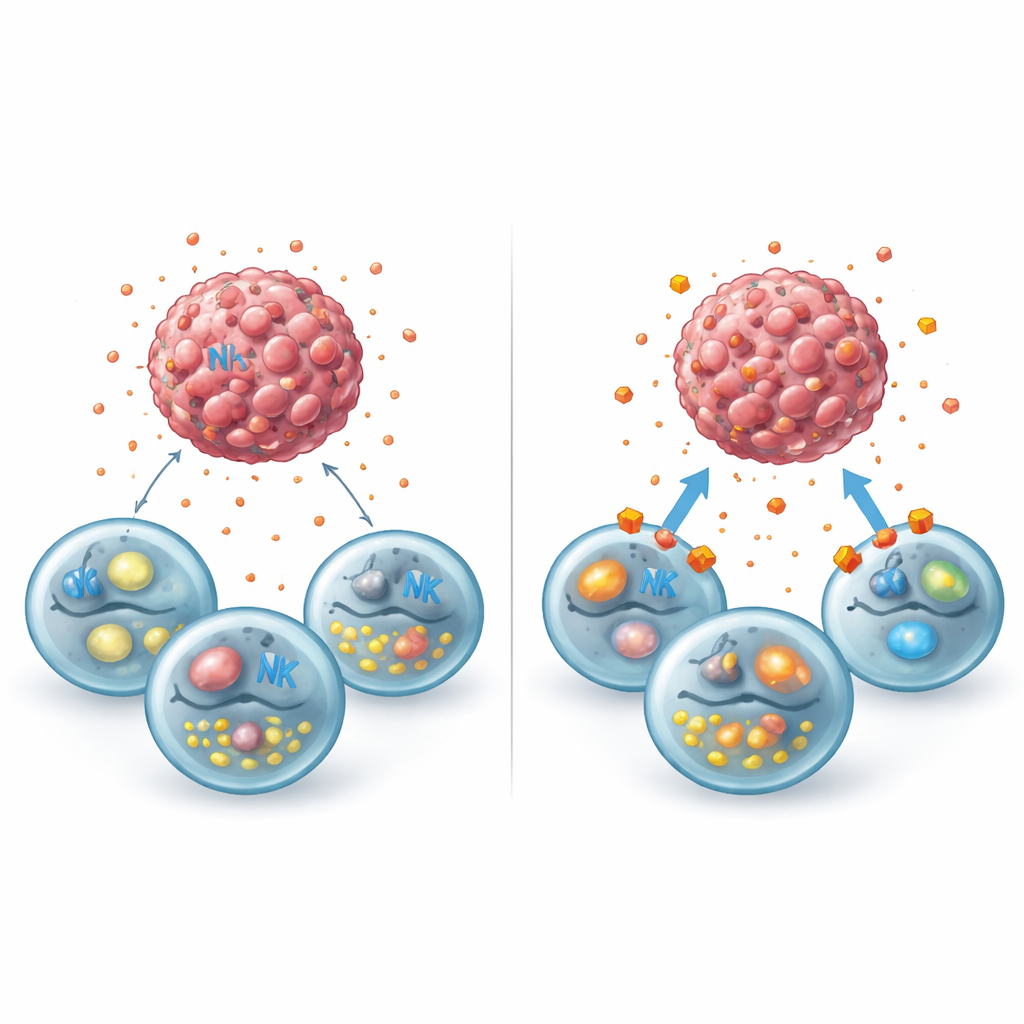
כיבוי נתיבי לקטאט כדי להעיר הגנות
המחקר בדק האם חסימת הובלת הלקטאט יכולה להרומם את הערפל המטבולי הזה. החוקרים הטפלו בתאי סרטן השד בסירוסינגופין, תרופה החוסמת שני חלבוני נשא מרכזיים (MCT1 ו‑MCT4) האחראיים לשינוע לקטאט דרך ממברנת התא, ובקוקטייל תרופתי שני שמעכבת בסלקטיביות כל נשא. טיפולים אלה כלאו את הלקטאט בתוך תאי הגידול, הפחיתו את שחרורו לסביבה ולא הרגו ישירות את הגידולים במינונים שנשתמשו בהם. עם הוספת תאי NK אנושיים התמונה השתנתה: הספירות הגידוליות התקצרו יותר, סמנים פנימיים של אפופטוזה עלו, ותאי NK השיבו את יכולתם להשתלט על שחרור הגרגרים, גם בנוכחות לקטאט חיצוני. במקביל, ניתוחים של מאגרי נתונים ציבוריים הראו שכיבוי קולטן הלקטאט GPR81 בתאי סרטן השד תכנת אותם מחדש כך שיופיעו איתותים שממריצים יותר את ה‑NK ופחות מולקולות המסייעות להסתתר או לעמוד בפני התקפה.
מה משמעות הממצאים לטיפול עתידי בסרטן השד
בסך הכל הממצאים מגלים שלקטאט אינו רק “פסולת” מטבולית בגידולים של השד — הוא מעכב פעיל של ההגנה החיסונית המוקדמת. רמות לקטאט גבוהות ואותות חזקים דרך קולטן הלקטאט יוצרים מיקרו‑סביבה שבה תאי NK מגיעים פחות, עובדים פחות ביעילות ומבזבזים את האנרגיה שלהם באופן גרוע. על‑ידי חסימת הובלת הלקטאט או קולטן זה, המחקר מראה שניתן לשקם את פעילות תאי NK ולהגביר מוות של תאי הגידול במודלים תלת־ממד ריאליסטיים. עבור מטופלות, עבודה זו מצביעה על כך שמדידת גנים הקשורים ללקטאט עשויה לסייע בחיזוי הפרוגנוזה, ושתרופות המטרה את מסלולי הלקטאט עשויות בעתיד להיות משולבות עם טיפולים מבוססי תאי NK וצורות נוספות של אימונותרפיה כדי להפוך גידולים עוינים מבחינה מטבולית לשטחים שבהם המערכת החיסונית יכולה להילחם.
ציטוט: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
מילות מפתח: סרטן השד, מטבוליזם לקטאט, תאי טבעיים קילר (NK), מיקרו־סביבה של הגידול, אימונותרפיה של סרטן