Clear Sky Science · es
Disfunción de células NK mediada por lactato como marcador pronóstico y diana terapéutica en el cáncer de mama
Cuando el combustible tumoral se vuelve contra el sistema inmune
Nuestros cuerpos producen constantemente lactato, una molécula sencilla conocida sobre todo por causar la sensación de ardor en los músculos durante el ejercicio. En muchos cánceres, sin embargo, los tumores generan lactato en cantidades tan grandes que remodelan su entorno. Este estudio muestra cómo el exceso de lactato en los tumores de mama puede silenciar discretamente a las células asesinas naturales (NK), defensoras inmunitarias de primera línea, y cómo bloquear el transporte y las señales del lactato podría reactivar estas células y mejorar los resultados en los pacientes.
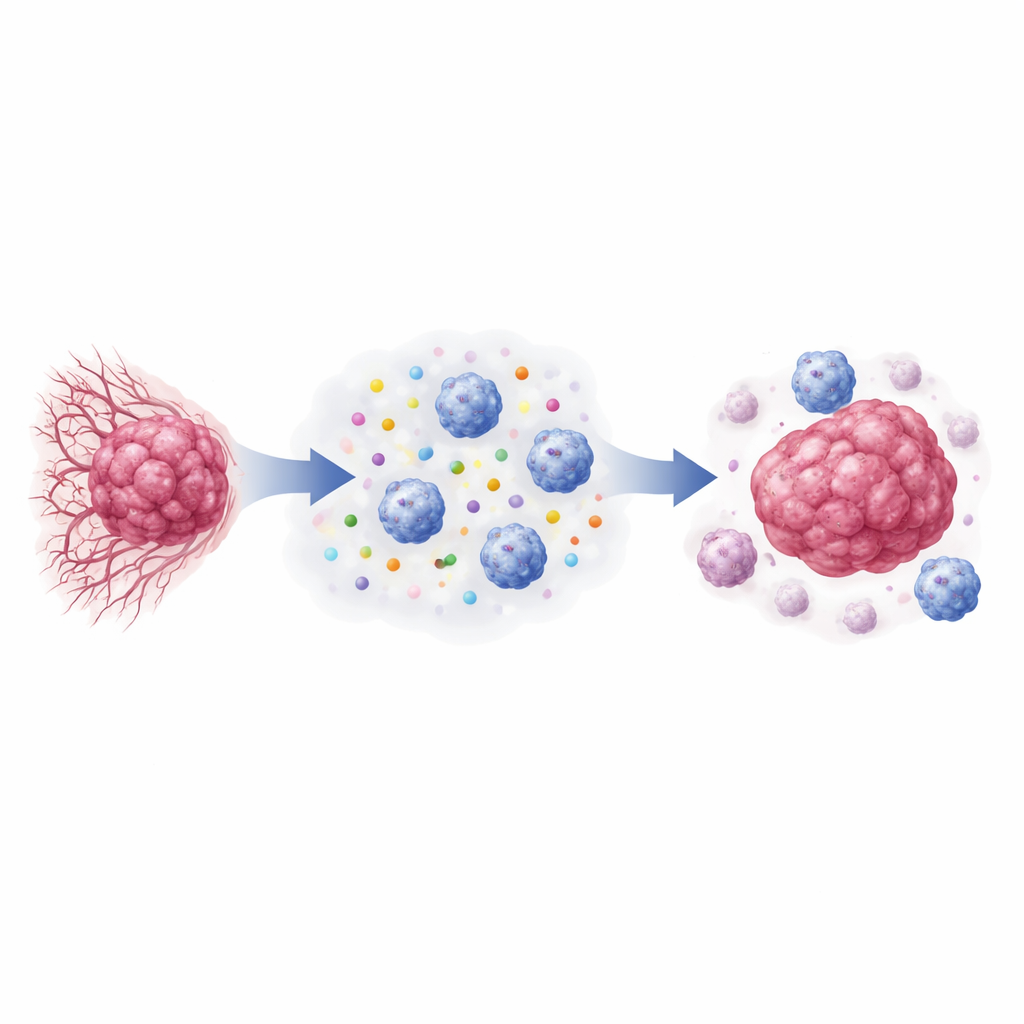
Un vínculo oculto entre la química tumoral y la supervivencia del paciente
Los investigadores recurrieron primero a datos de expresión génica de 882 mujeres con cáncer de mama. Examinaron genes que impulsan la producción y la detección de lactato en las células tumorales, junto con genes que marcan la activación de las células NK. Los tumores con mayor actividad de genes relacionados con el lactato, especialmente LDHA y HCAR1 (que codifica el receptor de lactato GPR81), mostraron de forma consistente una menor expresión de receptores de activación de las NK. Las pacientes cuyos tumores presentaban esta firma de «alto lactato, baja actividad NK» experimentaron periodos más cortos sin recurrencia del cáncer, incluso tras ajustar por edad, tamaño tumoral, estado de receptores hormonales y otros factores clínicos. En contraste, las mujeres cuyos tumores combinaban bajo metabolismo del lactato con fuertes señales de activación de NK tendieron a evolucionar mejor con el tiempo.
Cómo el exceso de lactato debilita el ataque inmune
Para entender qué hacen realmente los altos niveles de lactato a las células NK, el equipo aisló NK de donantes sanos y las expuso a concentraciones de lactato similares a las halladas en tumores de mama agresivos. Durante dos días, las NK crecieron más lentamente pero no murieron, lo que revela una especie de «freno» funcional en lugar de pérdida celular masiva. Los marcadores de superficie que indican disposición para luchar, así como receptores claves de activación, disminuyeron. En el interior de las células, los niveles de herramientas letales como interferón gamma y granzima B cayeron. Imágenes avanzadas y mediciones metabólicas mostraron que el lactato reconfiguró la química interna de las NK: sus mitocondrias produjeron menos energía, el consumo de oxígeno se redujo y se acumularon moléculas de tipo lipídico, todos signos de un estado letárgico y con déficit energético.
Bloquear el reclutamiento y silenciar las señales tumorales
Además de debilitar células NK individuales, el lactato también dificultó su llegada al tumor. En pequeños dispositivos microfluídicos que imitan la estructura tridimensional de los tumores, las NK migraron con mucho menos eficacia hacia esferoides de cáncer de mama bañados en lactato. Las estructuras tumorales en canales ricos en lactato mostraron mucha menos muerte celular, indicando que llegaron menos NK y que las que arribaron fueron menos eficaces. Las mediciones de moléculas de señalización revelaron que el lactato redujo la producción de quimioquinas CXCL9 y CXCL10, que normalmente ayudan a guiar y activar a las NK. Aunque las células cancerosas mostraban las “banderas” moleculares correctas para ser reconocidas por las NK, la combinación de un pobre reclutamiento y una degranulación atenuada (la liberación de gránulos tóxicos) dejó a los tumores en gran medida sin desafío.
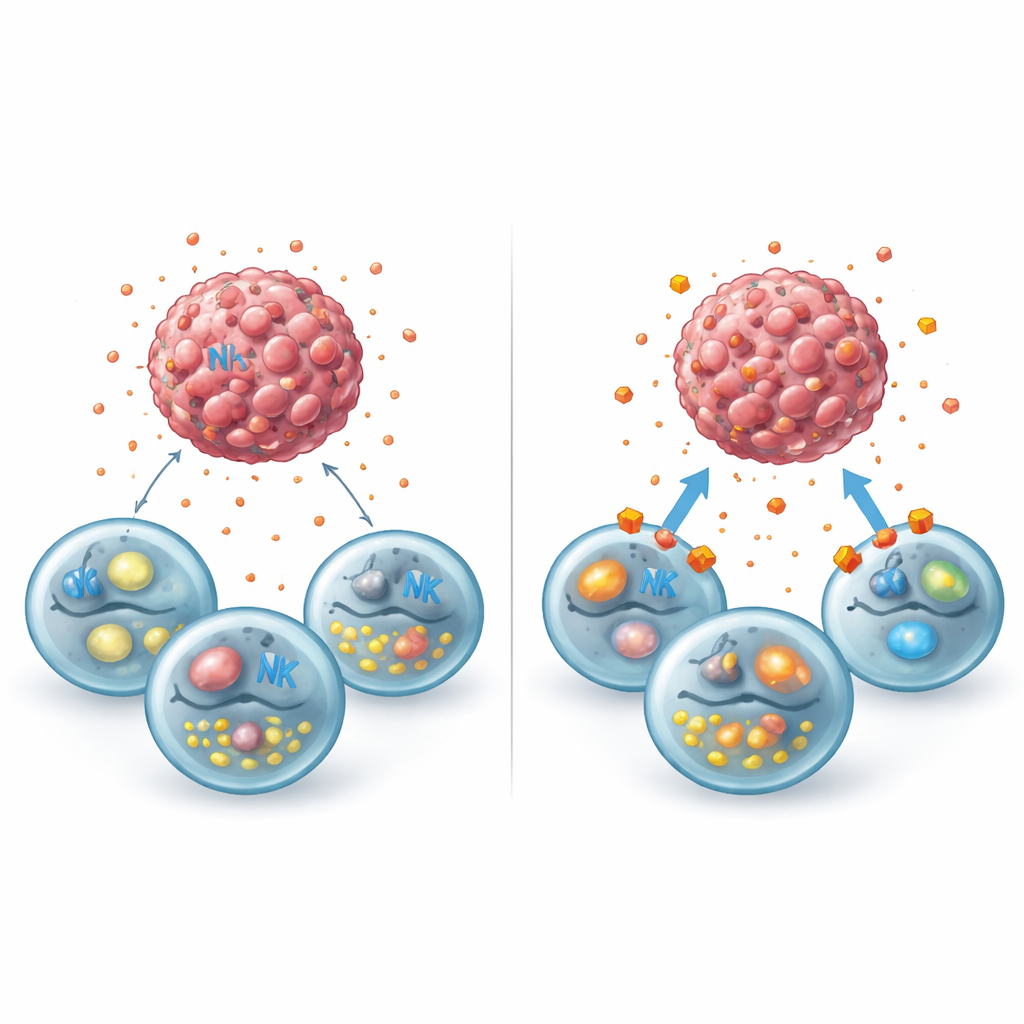
Apagar las vías del lactato para reavivar las defensas
El estudio se preguntó después si cortar el transporte de lactato podría disipar esta niebla metabólica. Los investigadores trataron células de cáncer de mama con sirosingopina, un fármaco que bloquea dos transportadores clave (MCT1 y MCT4) responsables de el transporte de lactato a través de la membrana celular, y con una segunda combinación farmacológica que inhibe selectivamente cada transportador. Estos tratamientos atraparon el lactato dentro de las células tumorales, redujeron su liberación al entorno y no mataron directamente a los tumores a las dosis utilizadas. Sin embargo, al añadirse NK humanas, el panorama cambió: los esferoides tumorales se redujeron más, aumentaron los marcadores internos de apoptosis y las NK recuperaron su capacidad de degranular, incluso en presencia de lactato añadido. Paralelamente, análisis de conjuntos de datos públicos mostraron que apagar el receptor de lactato GPR81 en células de cáncer de mama las reprogramó para mostrar más señales que estimulan a las NK y menos moléculas que les ayudan a ocultarse o resistir el ataque.
Qué implica esto para el tratamiento futuro del cáncer de mama
En conjunto, los hallazgos revelan que el lactato no es solo un «residuo» metabólico en los tumores de mama: es un supresor activo de la defensa inmunitaria temprana. Los niveles altos de lactato y la señalización intensa a través de su receptor contribuyen a crear un microambiente donde las NK llegan con menos frecuencia, trabajan con menos eficacia y agotan su energía más rápidamente. Bloqueando el transporte de lactato o su receptor, el estudio demuestra que es posible restaurar la actividad de las NK y aumentar la muerte de células tumorales en modelos tridimensionales realistas. Para los pacientes, este trabajo sugiere que medir genes relacionados con el lactato podría ayudar a predecir el pronóstico, y que fármacos dirigidos a las vías del lactato podrían algún día combinarse con terapias basadas en NK y otras formas de inmunoterapia para convertir tumores metabólicamente hostiles en un terreno donde el sistema inmune pueda combatirlos.
Cita: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
Palabras clave: cáncer de mama, metabolismo del lactato, células asesinas naturales, microambiente tumoral, inmunoterapia contra el cáncer