Clear Sky Science · pl
Funkcjonalna dysfunkcja komórek NK zależna od mleczanu jako marker prognostyczny i cel terapeutyczny w raku piersi
Kiedy paliwo guza zwraca się przeciw układowi odpornościowemu
W naszych ciałach stale powstaje mleczan, prosty związek najbardziej znany z wywoływania pieczenia mięśni podczas wysiłku. W wielu nowotworach jednak guzy wytwarzają mleczan w tak dużych ilościach, że przekształca on ich otoczenie. Badanie to pokazuje, jak nadmiar mleczanu w rakach piersi może cicho wyłączać komórki natural killers (NK) — pierwszoliniowych obrońców immunologicznych — oraz jak blokowanie transportu i sygnalizacji mleczanu może ożywić te komórki i poprawić wyniki u pacjentek.
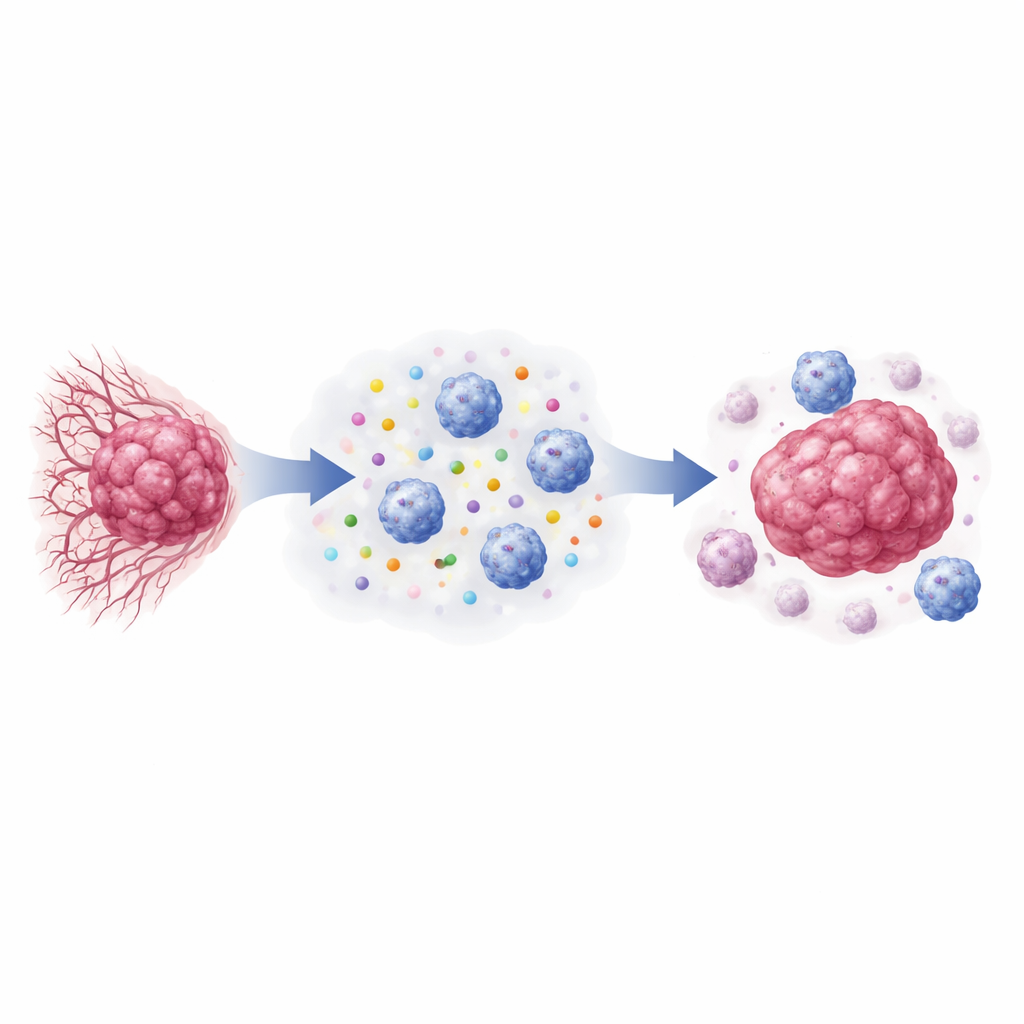
Ukryte powiązanie między chemią guza a przeżywalnością pacjentek
Naukowcy najpierw przeanalizowali dane ekspresji genów od 882 kobiet z rakiem piersi. Zbadali geny odpowiadające za produkcję i rozpoznawanie mleczanu w komórkach nowotworowych oraz geny będące markerami aktywacji komórek NK. Guzy o wyższej aktywności genów związanych z mleczanem, zwłaszcza LDHA i HCAR1 (kodującego receptor mleczanowy GPR81), konsekwentnie wykazywały niższą ekspresję receptorów aktywacji NK. Pacjentki, których guzy miały taki profil „wysoki mleczan, niska aktywność NK”, miały krótsze okresy wolne od nawrotu choroby, nawet po uwzględnieniu wieku, wielkości guza, statusu receptorów hormonalnych i innych czynników klinicznych. W przeciwieństwie do tego kobiety, których guzy łączyły niski metabolizm mleczanu z silnymi sygnałami aktywacji NK, zazwyczaj miały lepsze rokowanie w czasie.
Jak nadmiar mleczanu osłabia atak immunologiczny
Aby zrozumieć, co wysokie stężenia mleczanu robią komórkom NK, zespół wyizolował komórki NK od zdrowych dawców i wystawił je na stężenia mleczanu podobne do tych występujących w agresywnych guzach piersi. W ciągu dwóch dni komórki NK dzieliły się wolniej, ale nie umierały, co wskazuje na rodzaj funkcjonalnego „hamowania”, a nie masowej utraty komórek. Znaczniki powierzchniowe wskazujące gotowość do walki, jak również kluczowe receptory aktywujące, uległy obniżeniu. Wewnątrz komórek zmniejszyły się poziomy silnych narzędzi cytotoksycznych – interferonu gamma i granzymu B. Zaawansowane obrazowanie i pomiary metaboliczne wykazały, że mleczan przekształca wewnętrzną chemię komórek NK: ich mitochondria produkowały mniej energii, spadło zużycie tlenu, a nagromadziły się lipofilne cząsteczki – wszystko to oznaki ospałego, niedożywionego energetycznie stanu.
Blokowanie rekrutacji i wyciszanie sygnałów guza
Ponadto mleczan utrudniał nie tylko funkcję pojedynczych komórek NK, ale też ich przyciąganie do guza. W mikroukładach mikrofluidycznych odwzorowujących trójwymiarową strukturę guzów komórki NK migrowały znacznie mniej efektywnie w kierunku sferoidów raka piersi zanurzonych w mleczanie. Struktury guzopodobne w kanałach bogatych w mleczan wykazywały dużo mniej martwicy komórek, co wskazuje, że mniej komórek NK docierało i te, które docierały, były mniej skuteczne. Pomiary cząsteczek sygnałowych wykazały, że mleczan zmniejszał produkcję chemokin CXCL9 i CXCL10, które normalnie pomagają kierować i aktywować komórki NK. Chociaż komórki nowotworowe prezentowały właściwe molekularne «flagi» do rozpoznania przez NK, połączenie słabej rekrutacji i stłumionej degranulacji (uwalniania toksycznych ziarnistości) pozostawiało guzy w dużej mierze bez wyzwania.
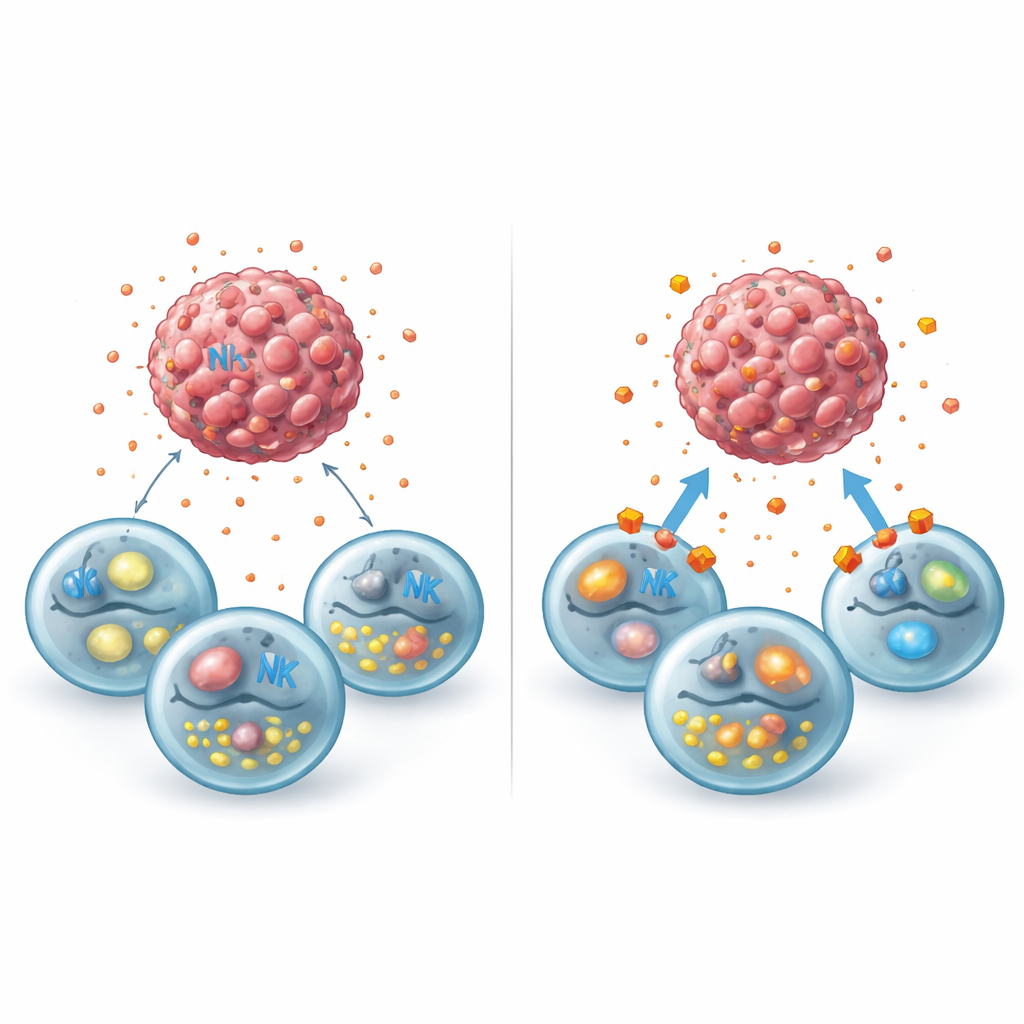
Wyłączanie szlaków mleczanu, by obudzić obronę
Badanie sprawdziło następnie, czy odcięcie transportu mleczanu może podnieść tę metaboliczną mgłę. Naukowcy potraktowali komórki raka piersi syrosingopinem, lekiem blokującym dwa kluczowe białka transportowe (MCT1 i MCT4) odpowiedzialne za przemieszczanie mleczanu przez błonę komórkową, oraz drugim koktajlem leków selektywnie hamujących każdy transporter. Leczenie to uwięziło mleczan wewnątrz komórek nowotworowych, zmniejszyło jego uwalnianie do środowiska i nie zabijało bezpośrednio guzów w zastosowanych dawkach. Po dodaniu ludzkich komórek NK obraz się jednak zmienił: sferoidy nowotworowe kurczyły się bardziej, wzrastały wewnętrzne markery apoptozy, a komórki NK odzyskiwały zdolność degranulacji, nawet w obecności dodanego mleczanu. Równoległe analizy publicznie dostępnych zbiorów danych wykazały, że wyłączenie receptora mleczanowego GPR81 w komórkach raka piersi przeprogramowywało je tak, by prezentowały więcej sygnałów stymulujących NK i mniej molekuł pomagających ukrywać się lub opierać atakowi.
Co to oznacza dla przyszłego leczenia raka piersi
Łącznie wyniki ujawniają, że mleczan nie jest jedynie metabolicznym «odpadem» w guzach piersi — jest aktywnym supresorem wczesnej obrony immunologicznej. Wysokie stężenia mleczanu i silna sygnalizacja przez jego receptor sprzyjają mikrośrodowisku, w którym komórki NK rzadziej docierają, działają mniej wydajnie i słabiej gospodarują energią. Blokując transport mleczanu lub jego receptor, badanie pokazuje, że można przywrócić aktywność NK i zwiększyć śmierć komórek nowotworowych w realistycznych modelach trójwymiarowych. Dla pacjentek praca ta sugeruje, że mierzenie genów związanych z mleczanem może pomóc prognozować rokowanie, a leki celujące w szlaki mleczanowe mogłyby w przyszłości być łączone z terapiami opartymi na komórkach NK i innymi formami immunoterapii, by przekształcić metabolitowo wrogie guzy w teren, na którym układ odpornościowy może skutecznie walczyć.
Cytowanie: Ielpo, S., Barberini, F., Gaiba, A. et al. Lactate-mediated NK cell dysfunction as a prognostic marker and therapeutic target in breast cancer. Cell Death Discov. 12, 200 (2026). https://doi.org/10.1038/s41420-026-03063-5
Słowa kluczowe: rak piersi, metabolizm mleczanu, komórki NK, mikrośrodowisko guza, immunoterapia przeciwnowotworowa