Clear Sky Science · zh
拉佛沙尼通过调节VDAC1扰乱结直肠癌细胞的线粒体稳态
本研究为何重要
结直肠癌是全球最常见且致死率较高的癌症之一。尽管许多治疗方法针对DNA或阻断生长信号,癌细胞常通过改造能量产生与利用方式来幸存。本研究考察了一种旧的兽用药物拉佛沙尼如何被重新定位,用以精确打击癌细胞的“发电站”——线粒体——促使肿瘤细胞走向自我毁灭,同时在很大程度上保留健康组织。
细胞“发电站”承受压力
线粒体是细胞内生成大部分能量并参与决定细胞生死的微小结构。包括结直肠肿瘤在内的癌细胞高度依赖功能良好的线粒体来支持快速生长和扩散。研究者聚焦于一个名为VDAC1的门控蛋白,它位于线粒体外膜,控制能量分子进出。当VDAC1构象改变并聚集时,可形成较大的通道,允许促死因子逸出到细胞质中。
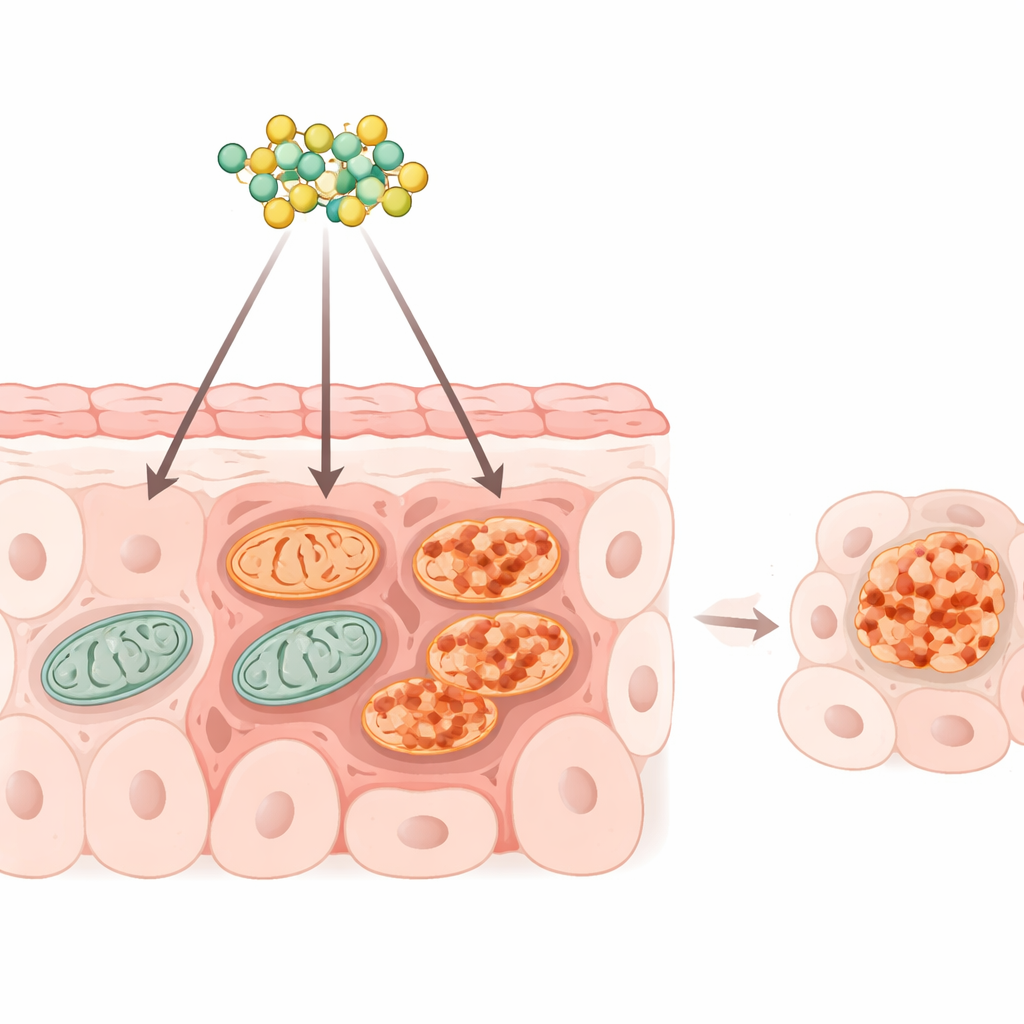
一种老寄生虫药的新靶点
拉佛沙尼最初用于通过破坏寄生虫的能量代谢来杀灭绦虫。早期研究表明它能够抑制结直肠肿瘤生长并在细胞的另一个隔室——内质网——引发应激,但其如何影响人体癌细胞的线粒体尚不清楚。本研究中,研究团队用拉佛沙尼处理结直肠癌细胞系,测量耗氧、能量产生和线粒体膜电位。数分钟内,药物显著降低线粒体呼吸并开始削弱膜电位,但当药物被洗去时,这一早期效应是可逆的,提示这是一种有针对性的扰动而非粗暴的毒害。
从可逆应激到致命损伤
当处理延长到数小时,情况发生变化。通过结合基因表达数据、蛋白质谱和代谢物测量,研究者发现对线粒体组分和通路的广泛且持久的破坏,这些通路负责运输燃料、合成新分子和维持细胞化学平衡。癌细胞未能成功适应,其线粒体膜电位逐渐丧失,且一种称为细胞色素c的关键蛋白从线粒体泄漏到周围液体中——这是程序性细胞死亡的经典早期步骤。不久之后,细胞开始死亡,证实延长的线粒体应激已越过不可逆的临界点。
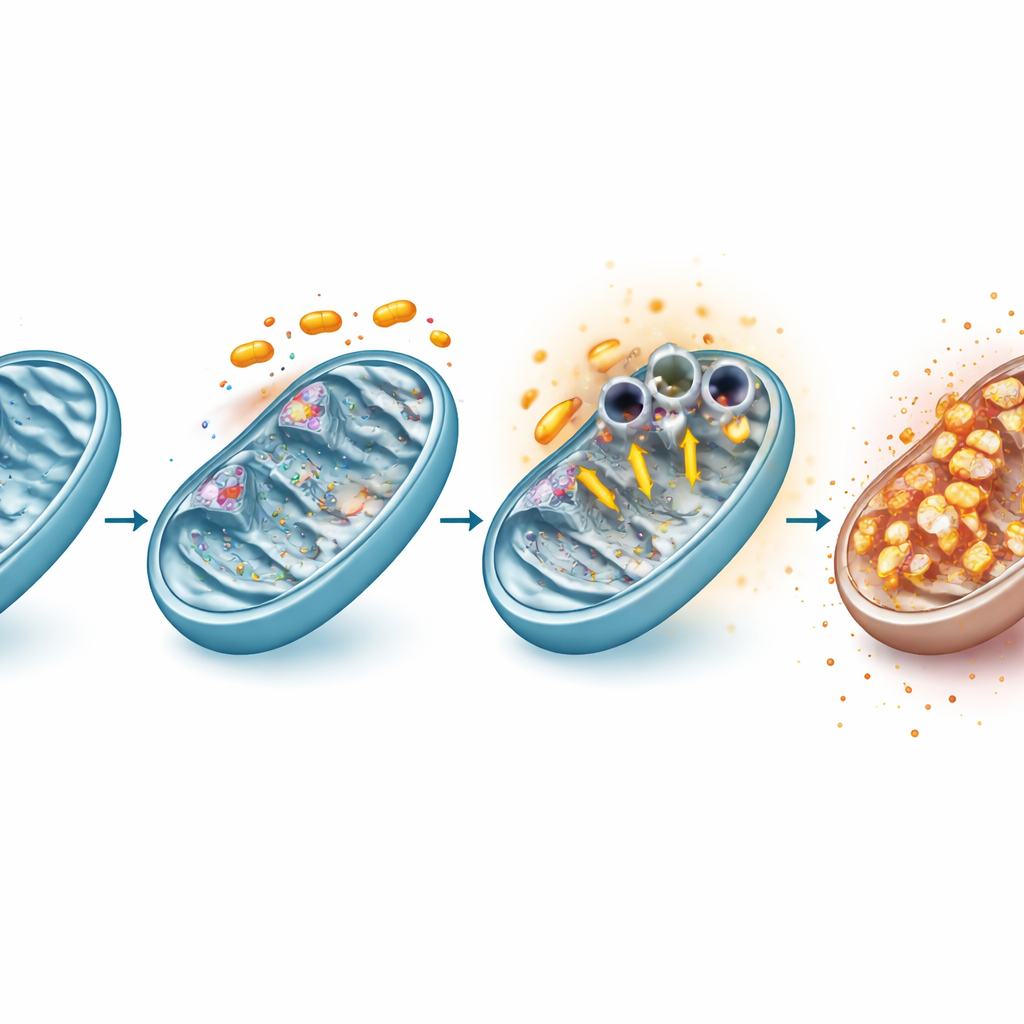
线粒体之门如何被迫打开
深入研究显示,拉佛沙尼直接抑制线粒体能量链中的两个主要蛋白复合体,称为复合体I和复合体III。这种干扰迅速改变细胞的氧化还原平衡,导致活性氧(具有化学活性的氧种)大量产生——尽管随着线粒体内电位崩溃,线粒体本身产生的一种特定副产物超氧化物反而减少。这种氧化还原扰动促使外线粒体膜上的VDAC1分子聚集成更大的结构,有效地打开了宽通道。用抗氧化剂清除活性氧,或药理学抑制VDAC1聚集,均减少了这些通道的打开和线粒体膜电位的丧失,将氧化应激、VDAC1行为与线粒体功能衰竭串联为一条事件链。
超越体外的证据
为测试这些效应在更真实背景下是否发生,研究者转而使用化学诱导结直肠肿瘤的小鼠模型以及来自患者的样本。在小鼠中,拉佛沙尼处理导致肿瘤数量和体积减少,细胞增殖的标志也有所降低。肿瘤组织的详细蛋白质分析显示线粒体蛋白发生广泛变化:参与燃料燃烧和驱动能量链的蛋白趋于下降,而与降解损伤成分和脂肪氧化相关的蛋白上升,暗示细胞在应对能量压力时陷入困境。在来自患者的肿瘤切片和暴露于拉佛沙尼的三维肠类器官中也观察到类似的线粒体蛋白变化,表明这种线粒体扰动在细胞培养、动物模型与人类肿瘤组织中是一致的。
对未来癌症治疗的意义
总体而言,该研究表明拉佛沙尼并非简单地“拔掉电源插头”来终止能量产生;相反,它将结直肠癌细胞的线粒体推入一种长期的功能障碍状态,使其无法逃脱。通过阻断关键的能量链复合体、干扰活性分子的平衡并促使VDAC1门打开,药物触发了一系列可控事件,最终导致线粒体失效和细胞死亡。普通结肠细胞对受压的线粒体依赖较少且具有更大的储备能力,似乎受影响较轻。这些发现提出了一个可能性:通过精确调节线粒体应激——而非彻底摧毁——可以选择性地削弱癌细胞,并支持进一步探索类似拉佛沙尼的化合物作为结直肠癌未来疗法的可行性。
引用: Tomassini, L., Pacifico, T., Serra, M.A. et al. Rafoxanide disrupts mitochondrial homeostasis through VDAC1 modulation in colorectal cancer cells. Cell Death Discov. 12, 142 (2026). https://doi.org/10.1038/s41420-026-02986-3
关键词: 结直肠癌, 线粒体, VDAC1, 活性氧, 药物再利用