Clear Sky Science · pl
Rafoxanide zaburza homeostazę mitochondrialną przez modulację VDAC1 w komórkach raka jelita grubego
Dlaczego to badanie ma znaczenie
Rak jelita grubego jest jednym z najczęstszych i najgroźniejszych nowotworów na świecie. Podczas gdy wiele terapii atakuje DNA lub blokuje sygnały wzrostu, komórki nowotworowe często przetrwają dzięki przestrojeniu sposobu wytwarzania i wykorzystania energii. W tym badaniu zbadano, jak stary lek weterynaryjny — rafoxanide — można ponownie wykorzystać do uderzenia w „elektrownie” nowotworu, czyli mitochondria, w sposób precyzyjny, który skłania komórki guzowe do autodestrukcji, przy jednoczesnym ograniczonym wpływie na tkanki zdrowe.
Elektrownie komórkowe pod presją
Mitochondria to drobne struktury w komórkach, które generują większość energii i pomagają decydować o losie komórki — życiu lub śmierci. Komórki nowotworowe, także te w guzach jelita grubego, w dużym stopniu polegają na prawidłowo działających mitochondriach, aby napędzać szybki wzrost i przerzuty. Badacze skupili się na białku-strażniku o nazwie VDAC1, które znajduje się w zewnętrznej błonie mitochondriów i kontroluje przepływ nośników energii do wnętrza i na zewnątrz. Gdy VDAC1 zmienia konformację i grupuje się, może tworzyć duże otwory pozwalające na ucieczkę czynników promujących śmierć do wnętrza komórki.
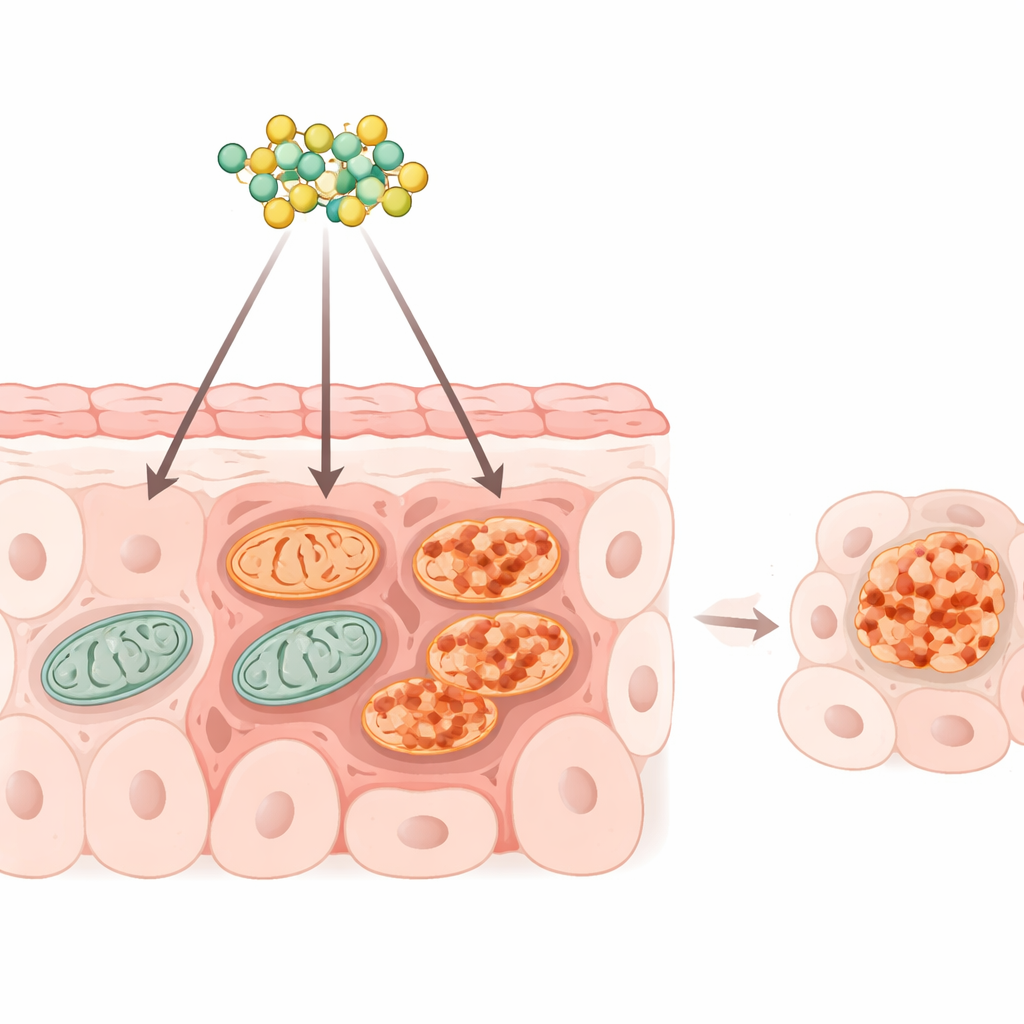
Stary lek przeciw pasożytom z nowym celem
Rafoxanide został pierwotnie opracowany do zabijania pasożytniczych robaków poprzez zakłócanie ich produkcji energii. Wcześniejsze prace wykazały, że może on spowalniać wzrost guzów jelita grubego i wywoływać stres w innym przedziale komórkowym — retikulum endoplazmatycznym, jednak wpływ na mitochondria w komórkach ludzkiego nowotworu pozostawał niejasny. W tym badaniu zespół potraktował linie komórkowe raka jelita rafoxanidem i zmierzył zużycie tlenu, produkcję energii oraz potencjał elektryczny przez błonę mitochondrialną. W ciągu minut lek ostro zmniejszył „oddychanie” mitochondriów i zaczął osłabiać ładunek błony, przy czym ten wczesny efekt był odwracalny po wypłukaniu leku, co sugeruje ukierunkowane zaburzenie, a nie brutalne zatrucie.
Od odwracalnego stresu do trwałego uszkodzenia
Przy przedłużonym czasie leczenia obraz się zmienił. Łącząc dane o aktywności genów, profilach białkowych i pomiarach metabolitów, badacze odkryli szerokie i długotrwałe zakłócenia składników mitochondriów oraz szlaków odpowiedzialnych za transport paliwa, syntezę nowych cząsteczek i utrzymanie równowagi metabolicznej. Komórki nowotworowe nie zdołały przeprowadzić skutecznej adaptacji — ich błona mitochondrialna stopniowo traciła ładunek, a kluczowe białko cytochrom c wydostało się z mitochondriów do otaczającego płynu — klasyczny wczesny krok w programowanej śmierci komórki. Wkrótce potem komórki zaczęły obumierać, co potwierdza, że przedłużony stres mitochondrialny przekroczył punkt, z którego nie było powrotu.
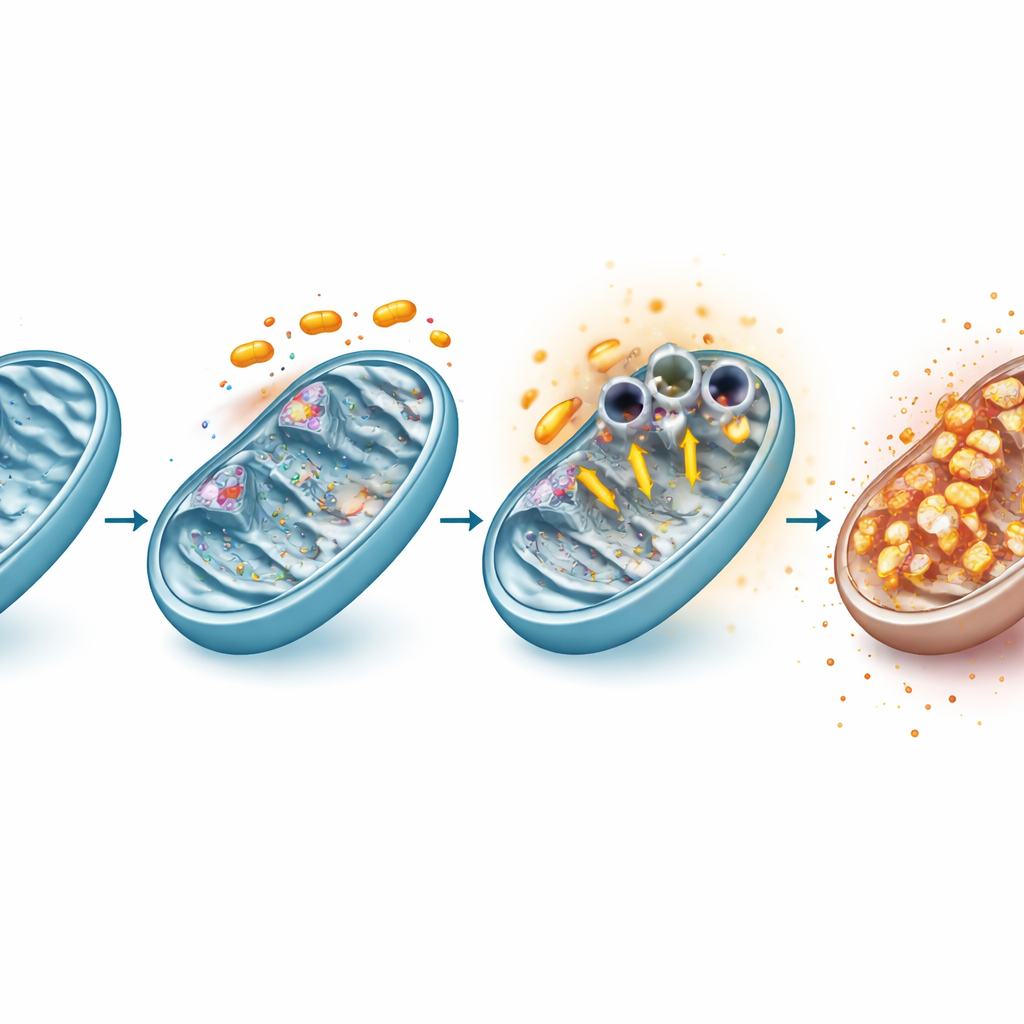
W jaki sposób brama mitochondrialna jest wymuszona na otwarcie
Pogłębiając analizę, zespół wykazał, że rafoxanide bezpośrednio osłabia dwie główne jednostki białkowe łańcucha oddechowego mitochondriów, znane jako kompleksy I i III. To zakłócenie szybko zmieniło równowagę redoks komórki, prowadząc do wybuchu reaktywnych form tlenu — chemicznie reaktywnych postaci tlenu — nawet jeśli mitochondria same wytwarzały mniej określonego produktu ubocznego, nadtlenku superoksydu, z powodu zapadania się ich wewnętrznego ładunku. Ta zaburzenie redoks skłoniło cząsteczki VDAC1 w zewnętrznej błonie mitochondrialnej do grupowania się w większe struktury, skutecznie otwierając szerokie kanały. Zablokowanie reaktywnych form tlenu za pomocą przeciwutleniacza lub farmakologiczne zahamowanie agregacji VDAC1 zmniejszało zarówno otwarcie tych kanałów, jak i utratę ładunku błony mitochondrialnej, łącząc stres oksydacyjny, zachowanie VDAC1 i niewydolność mitochondriów w jeden łańcuch zdarzeń.
Dowody poza hodowlą komórkową
Aby sprawdzić, czy te efekty występują w bardziej realistycznych warunkach, badacze sięgnęli po myszy z chemicznie indukowanymi guzami jelita grubego oraz po próbki pobrane bezpośrednio od pacjentów. U myszy leczenie rafoxanidem prowadziło do mniejszej liczby i rozmiaru guzów oraz zmniejszenia oznak proliferacji komórek. Szczegółowa analiza białkowa tkanek guza ujawniła szerokie przesunięcia w białkach mitochondrialnych: te zaangażowane w spalanie paliwa i funkcjonowanie łańcucha oddechowego wykazywały tendencję do spadku, podczas gdy białka związane z degradacją uszkodzonych składników i utlenianiem tłuszczów wzrastały, sugerując zmagania komórek z deficytem energetycznym. Podobne zmiany białek mitochondrialnych zaobserwowano w wycinkach guza pochodzących od pacjentów oraz w trójwymiarowych organoidach jelitowych wystawionych na rafoxanide, co wskazuje, że to zaburzenie mitochondrialne jest spójne w hodowlach komórkowych, modelach zwierzęcych i tkankach nowotworowych ludzkiego pochodzenia.
Co to oznacza dla przyszłego leczenia raka
Całościowo badanie pokazuje, że rafoxanide nie „wyciąga po prostu wtyczki” z produkcji energii; zamiast tego wpędza mitochondria komórek raka jelita w długotrwały stan dysfunkcji, z którego nie potrafią się wydostać. Poprzez blokowanie kluczowych kompleksów łańcucha oddechowego, zaburzanie równowagi reaktywnych cząsteczek i wymuszanie otwarcia bramy VDAC1, lek uruchamia kontrolowaną sekwencję zdarzeń kończącą się niewydolnością mitochondrialną i śmiercią komórki. Prawidłowe komórki jelita grubego, które są mniej zależne od obciążonych mitochondriów i dysponują większym zapasem rezerw, wydają się być znacznie mniej dotknięte. Te wyniki sugerują, że starannie wyważony stres mitochondrialny — zamiast bezpośredniego niszczenia — może być skutecznym sposobem selektywnego osłabienia komórek nowotworowych i wspierają dalsze badania nad związkami podobnymi do rafoxanidu jako potencjalnymi terapiami raka jelita grubego.
Cytowanie: Tomassini, L., Pacifico, T., Serra, M.A. et al. Rafoxanide disrupts mitochondrial homeostasis through VDAC1 modulation in colorectal cancer cells. Cell Death Discov. 12, 142 (2026). https://doi.org/10.1038/s41420-026-02986-3
Słowa kluczowe: rak jelita grubego, mitochondria, VDAC1, reaktywne formy tlenu, ponowne zastosowanie leków