Clear Sky Science · he
ראפוקסאניד מפר את הומאוסטזת המיטוכונדריה דרך מודולציה של VDAC1 בתאי סרטן המעי הגס
מדוע המחקר הזה חשוב
סרטן המעי הגס הוא אחד הסרטנים הנפוצים והקטלניים ביותר בעולם. בעוד שטיפולים רבים תוקפים DNA או חוסמים אותות גדילה, תאי סרטן לעתים קרובות שורדים על ידי שינוי האופן שבו הם מייצרים ומשתמשים באנרגיה. המחקר הזה בוחן כיצד תרופה וטרינרית ישנה, ראפוקסאניד, יכולה לעבור שימוש מחדש כדי לפגוע ב”תחנות הכוח” של הסרטן – המיטוכונדריות – באופן מדויק שמדחף את תאי הגידול להרס עצמי תוך פגיעה מוגבלת ברקמות בריאות.
תחנות הכוח של התא תחת לחץ
מיטוכונדריות הן מבנים זעירים בתוך התא שמייצרים את רוב האנרגיה של התא ועוזרות להחליט האם התא יחיה או ימות. תאי סרטן, כולל אלה בגידולי המעי הגס, תלויים במידה רבה במיטוכונדריות מתפקדות היטב כדי להזין גדילה מהירה והתפשטות. החוקרים התמקדו בחלבון שער שנקרא VDAC1, שנמצא במעטפת החיצונית של המיטוכונדריה ושולט בזרימת מולקולות נושאות אנרגיה פנימה והחוצה. כאשר VDAC1 משנה צורה ומצטבר, הוא יכול ליצור פתחים גדולים שמאפשרים לגורמים המעודדים מוות לברוח לתוך התא.
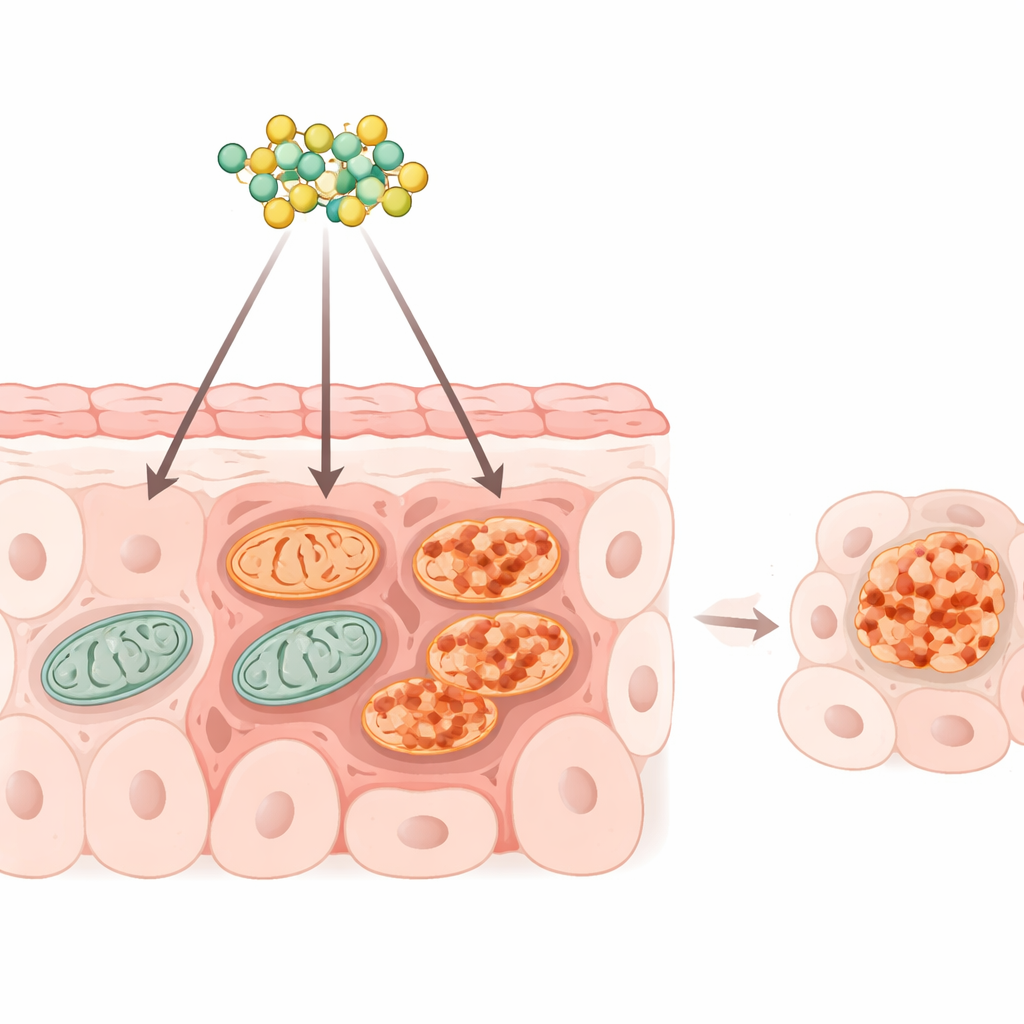
תרופה ישנה לפרזיטים עם מטרה חדשה
ראפוקסאניד פותח במקור להרוג תולעים פרזיטיות על ידי הפרעה לייצור האנרגיה שלהן. מחקרים מוקדמים הראו כי הוא יכול להאט את צמיחת גידולי המעי הגס ולגרום למתח ברכיב אחר בתא, הרשתית האנדופלזמטית, אך לא היה ברור כיצד הוא משפיע על המיטוכונדריות בתאי סרטן אנושיים. במחקר זה הטילה הצוות תרופות על שורות תאים של סרטן המעי הגס ומדדו שימוש בחמצן, ייצור אנרגיה והמטען החשמלי על פני ממברנת המיטוכונדריה. בתוך דקות, התרופה הפחיתה בחדות את נשימת המיטוכונדריה והחלה להחליש את מטען הממברנה, אך ההשפעה המוקדמת הייתה הפיכה כאשר שטפו את התרופה החוצה, מה שמרמז על הפרעה ממוקדת ולא הרעלה בוטה.
ממתח הפיך לנזק קטלני
כאשר הטיפול הורחב לשעות, התמונה השתנתה. בשילוב נתוני פעילות גנטית, פרופילי חלבונים ומדידות מטבוליטים, החוקרים מצאו הפרעות רחבות ועמידות לרכיבים ולמסלולים מיטוכונדריאליים המסייעים בהובלת דלק, בבנייה של מולקולות חדשות ובאיזון הכימיה התאית. תאי הסרטן לא הצליחו להתאים עצמם בהצלחה, ממברנת המיטוכונדריה שלהם איבדה בהדרגה את המטען, וחלבון מרכזי בשם ציטוכרום c דלף מהמיטוכונדריות אל הנוזל המקיף — צעד מוקדם קלאסי בתהליך ההרג המתוכנן של התא. זמן קצר לאחר מכן החלו התאים למות, מה שאישר שמתח מיטוכונדריאלי ממושך חצה נקודת אל חזור.
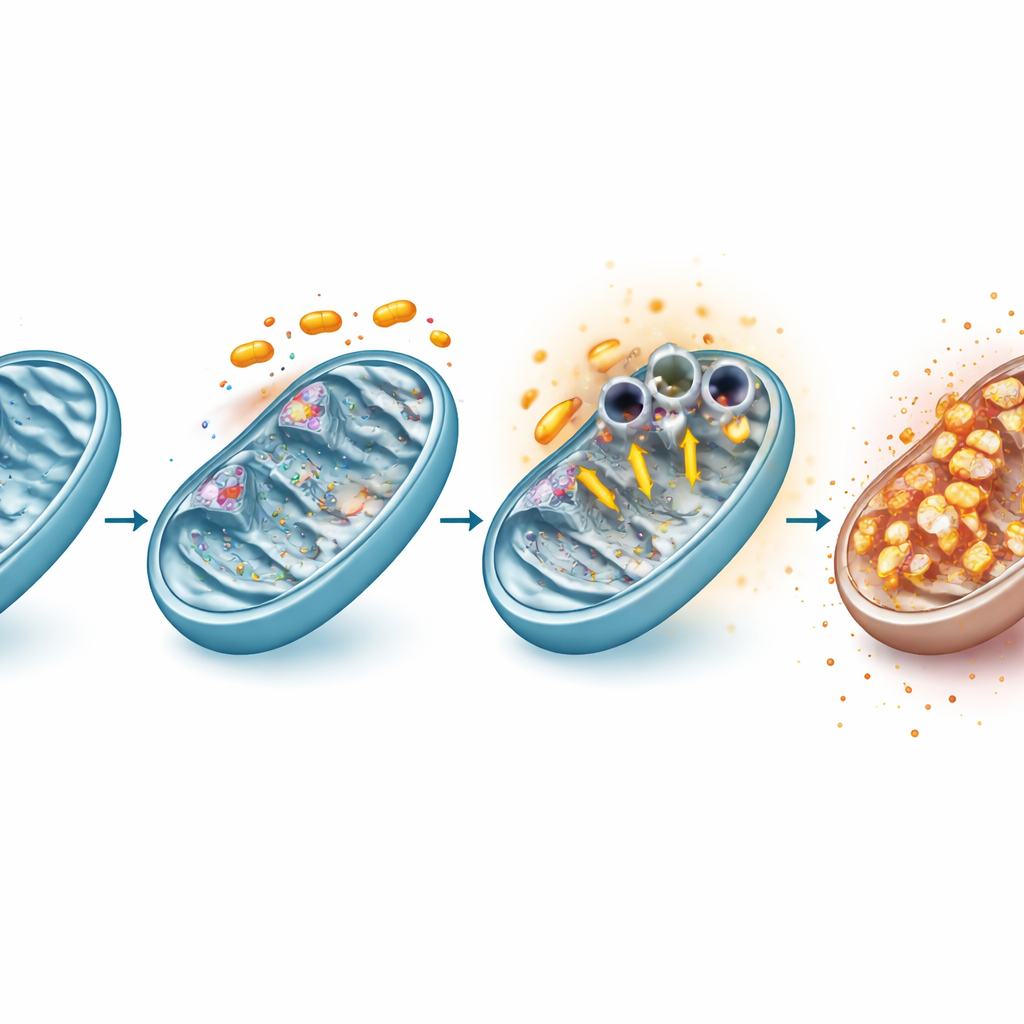
כיצד דחפו את שער המיטוכונדריה לפתיחה
בחינה מעמיקה יותר הראתה כי ראפוקסאניד מדכא ישירות שתי תצברויות חלבונים מרכזיות בשרשרת האנרגיה המיטוכונדריאלית, הידועות כקומפלקסים I ו-III. התערבות זו שינתה במהירות את מאזן החמצון-חיזור בתא, והובילה לפרץ של מולקולות חמצון פעילות — צורות כימיות תגובתיות של חמצן — גם כאשר המיטוכונדריות עצמן ייצרו פחות תוצר ספציפי שנקרא סופרוקסיד בעקבות התמוטטות המטען הפנימי. ההפרעה במאזן החמצון-חיזור דחפה מולקולות VDAC1 בממברנת המיטוכונדריה החיצונית להיערם למבנים גדולים יותר, ובכך פתחה ערוצים רחבים. חסימה של מולקולות חמצון פעילות באמצעות אנטיאוקסידנט, או עיכוב פרמקולוגי של התגבשות VDAC1, הפחיתה הן את פתיחת הערוצים והן את איבוד מטען ממברנת המיטוכונדריה, וקישרה את הלחץ החמצוני, ההתנהגות של VDAC1 וכשל המיטוכונדריה לשרשרת אירועים אחת.
הראיות מעבר לצלחת הפטרי
כדי לבדוק האם ההשפעות האלה מופיעות בהקשרים מציאותיים יותר, פנו החוקרים לעכברים עם גידולי מעי הגס המושרתים כימית ולמדגמים שנלקחו ישירות מחולים. בעכברים, טיפול בראפוקסאניד הוביל לפחות ולעוביים נמוכים יותר של גידולים והפחתה בסימנים של התרבות תאית. ניתוח חלבונים מפורט של רקמת הגידול חשף שינויים רחבים בחלבוני מיטוכונדריה: אלה המעורבים בשריפת דלק ובהפעלת שרשרת האנרגיה נטו לרדת, בעוד חלבונים הקשורים בפירוק רכיבים פגומים ושריפת שומנים עלו, מרמזים על תאים שנאבקים להתמודד עם לחץ אנרגטי. שינויים דומים בחלבוני מיטוכונדריה הופיעו גם באקספלנטים של גידולים שמקורם בחולים ובאורגנואידים תלת-ממדיים של המעי שנחשפו לראפוקסאניד, מה שמעיד על כך שההפרעה המיטוכונדריאלית עקבית בתרביות תאים, במודלים חיות וברקמות גידול אנושיות.
מה משמעות זה לטיפול העתידי בסרטן
בסך הכול, המחקר מראה כי ראפוקסאניד אינו פשוט "מוליך את השידור" של ייצור האנרגיה; במקום זאת, הוא דוחק את מיטוכונדריות תאי סרטן המעי הגס למצב ממושך של תפקוד לקוי שממנו אינן יכולות להיחלץ. על ידי חסימת קומפלקסים מרכזיים בשרשרת האנרגיה, הפרעת מאזן המולקולות התגובתיות והנעת שער VDAC1 לפתיחה, התרופה מפעילה רצף מבוקר שמסתיים בכשל מיטוכונדריאלי ומוות תאי. תאי המעי התקינים, שתלויים פחות במיטוכונדריות תחת לחץ ויש להם קיבולת רזרבית גדולה יותר, נראים פחות מושפעים. ממצאים אלה מעלים את האפשרות כי יצירת מתח מיטוכונדריאלי מכווין — ולא השמדה מוחלטת — יכולה להיות דרך עוצמתית להחליש בחריפות תאי סרטן, ותומכים בחקירה נוספת של תרכובות דמויות ראפוקסאניד כטיפולים עתידיים לסרטן המעי הגס.
ציטוט: Tomassini, L., Pacifico, T., Serra, M.A. et al. Rafoxanide disrupts mitochondrial homeostasis through VDAC1 modulation in colorectal cancer cells. Cell Death Discov. 12, 142 (2026). https://doi.org/10.1038/s41420-026-02986-3
מילות מפתח: סרטן המעי הגס, מיטוכונדריה, VDAC1, מולקולות חימצון פעילות, שימוש מחדש בתרופות