Clear Sky Science · sv
Rafoxanide stör mitokondriell homeostas genom VDAC1-modulation i kolorektala cancerceller
Varför denna studie är viktig
Kolorektal cancer är en av de vanligaste och mest dödliga cancerformerna globalt. Medan många behandlingar angriper DNA eller blockerar tillväxtsignaler överlever cancerceller ofta genom att omprogrammera hur de producerar och använder energi. Denna studie undersöker hur ett gammalt veterinärläkemedel, rafoxanide, kan omdisponeras för att angripa cancerets ”kraftstationer” – mitokondrierna – på ett precist sätt som skjuter tumörceller mot självförintelse samtidigt som friska vävnader i stort sett skonas.
Cellens kraftstationer under press
Mitokondrier är små strukturer i cellerna som genererar det mesta av cellens energi och hjälper till att avgöra om en cell lever eller dör. Cancerceller, inklusive de i kolorektala tumörer, är starkt beroende av välfungerande mitokondrier för att driva snabb tillväxt och spridning. Forskarnas fokus låg på ett grindvaktprotein kallat VDAC1, som sitter i mitokondriens yttre membran och kontrollerar flödet av energibärande molekyler in och ut. När VDAC1 ändrar form och klustras kan det bilda stora öppningar som tillåter dödsfrämjande faktorer att läcka ut i cellen.
En gammal antiparasitmedicin med ett nytt mål
Rafoxanide utvecklades ursprungligen för att döda parasitmaskar genom att störa deras energiproduktion. Tidigare arbete visade att det kan bromsa tillväxten av kolorektala tumörer och utlösa stress i en annan cellulär kompartment, det endoplasmatiska nätverket, men hur det påverkar mitokondrier i mänskliga cancerceller var oklart. I denna studie behandlade teamet kolorektala cellinjer med rafoxanide och mätte syreförbrukning, energiproduktion och den elektriska potentialen över mitokondriemembranet. Inom minuter minskade läkemedlet kraftigt mitokondriernas andning och började försvaga membranets potential, men denna tidiga effekt var reversibel när läkemedlet tvättades bort, vilket tyder på en riktad störning snarare än grov förgiftning.
Från reversibel stress till dödlig skada
När behandlingen förlängdes till timmar förändrades bilden. Genom att kombinera data om genaktivitet, proteinprofiler och metabolitmätningar fann forskarna breda och bestående störningar i mitokondriella komponenter och vägar som hjälper till att förflytta bränsle, bygga nya molekyler och balansera cellens kemi. Cancercellerna lyckades inte genomföra en framgångsrik anpassning, deras mitokondriella membran förlorade gradvis sin potential och ett nyckelprotein kallat cytokrom c läckte från mitokondrierna ut i omgivande vätska – ett klassiskt tidigt steg i programmerad celldöd. Strax därefter började cellerna dö, vilket bekräftar att förlängd mitokondriell stress hade korsat en punkt utan återvändo.
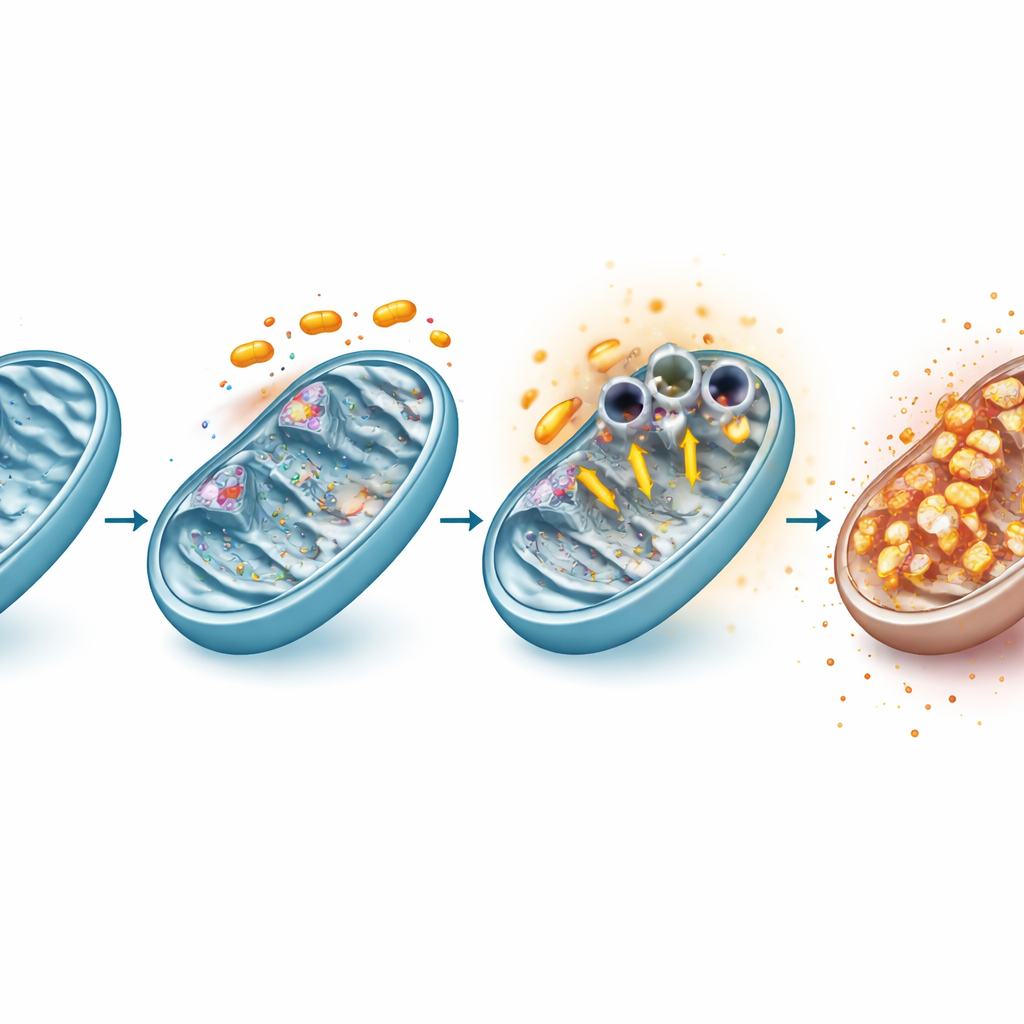
Hur den mitokondriella porten tvingas upp
Vid djupare analyser visade teamet att rafoxanide direkt dämpar två stora proteinkomplex i den mitokondriella andningskedjan, kända som komplex I och III. Denna påverkan förändrade snabbt cellens redoxbalans och ledde till en våg av reaktiva syreradikaler – kemiskt reaktiva former av syre – även om mitokondrierna själva producerade mindre av en viss biprodukt kallad superoxid eftersom deras inre potential kollapsade. Denna redoxstörning drev VDAC1-molekyler i det yttre mitokondriemembranet att klustra till större strukturer, vilket effektivt öppnade vidsträckta kanaler. Att blockera reaktiva syreradikaler med en antioxidant, eller farmakologiskt hämma VDAC1-klustring, minskade både öppningen av dessa kanaler och förlusten av mitokondriemembranpotential, vilket knöt ihop oxidativ stress, VDAC1-beteende och mitokondriell kollaps i en enda händelsekedja.
Bevis bortom odlingsskålen
För att undersöka om dessa effekter uppträder i mer realistiska miljöer vände sig forskarna till möss med kemiskt inducerade kolorektala tumörer och till prover tagna direkt från patienter. Hos möss ledde rafoxanidebehandling till färre och mindre tumörer och minskade tecken på cellproliferation. Detaljerad proteomanalys av tumörvävnad visade breda skiften i mitokondriella proteiner: de som är involverade i förbränning av bränsle och drift av andningskedjan tenderade att minska, medan proteiner kopplade till nedbrytning av skadade komponenter och fettförbränning ökade, vilket antyder att cellerna kämpade med energistress. Liknande förändringar i mitokondriella proteiner framkom i patienthärledda tumörexplantat och tredimensionella intestinorganoider exponerade för rafoxanide, vilket tyder på att denna mitokondriella störning är konsekvent över cellkulturer, djurmodeller och mänsklig tumörvävnad.
Vad detta betyder för framtida cancerbehandling
Sammanfattningsvis visar studien att rafoxanide inte helt enkelt ”drar ur kontakten” för energiproduktion; istället puttar det mitokondrierna i kolorektala cancerceller in i ett förlängt dysfunktionellt tillstånd som de inte kan undkomma. Genom att blockera nyckelkomplex i andningskedjan, rubba balansen av reaktiva molekyler och driva VDAC1-porten att öppnas, sätter läkemedlet igång en kontrollerad sekvens som slutar i mitokondriell kollaps och celldöd. Normala kolonceller, som är mindre beroende av stressade mitokondrier och har större reserver, verkar mycket mindre påverkade. Dessa fynd öppnar för möjligheten att finjusterad mitokondriell stress – snarare än total förstörelse – kan vara ett kraftfullt sätt att selektivt försvaga cancerceller, och de stödjer vidare utforskning av rafoxanide-liknande föreningar som framtida terapier mot kolorektal cancer.
Citering: Tomassini, L., Pacifico, T., Serra, M.A. et al. Rafoxanide disrupts mitochondrial homeostasis through VDAC1 modulation in colorectal cancer cells. Cell Death Discov. 12, 142 (2026). https://doi.org/10.1038/s41420-026-02986-3
Nyckelord: kolorektal cancer, mitokondrier, VDAC1, reaktiva syreradikaler, läkemedelsomdisponering