Clear Sky Science · ar
رافوكسنايد يعطّل توازن الميتوكوندريا عبر تعديل VDAC1 في خلايا سرطان القولون والمستقيم
لماذا تهم هذه الدراسة
يُعد سرطان القولون والمستقيم من أكثر السرطانات شيوعًا وقسوةً على الصعيد العالمي. بينما تستهدف العديد من العلاجات الحمض النووي أو تُعيق إشارات النمو، فإن الخلايا السرطانية غالبًا ما تنجو عن طريق إعادة ترتيب طرق إنتاجها واستهلاكها للطاقة. تستكشف هذه الدراسة كيف يمكن إعادة توظيف دواء بيطري قديم، الرافوكسنايد، لضرب "محطات الطاقة" في السرطان — الميتوكوندريا — بطريقة محددة تدفع خلايا الورم نحو الاندثار الذاتي مع الحفاظ إلى حد كبير على الأنسجة السليمة.
محطات طاقة الخلية تحت الضغط
الميتوكوندريا هي هياكل صغيرة داخل الخلايا تولّد معظم طاقة الخلية وتساعد في تقرير ما إذا كانت الخلية تبقى على قيد الحياة أم تموت. تعتمد الخلايا السرطانية، بما فيها خلايا أورام القولون والمستقيم، بشكل كبير على ميتوكوندريا تعمل جيدًا لتغذية النمو السريع والانتشار. ركّز الباحثون على بروتين حارس يدعى VDAC1، يقع في الغلاف الخارجي للميتوكوندريا ويضبط تدفق الجزيئات الحاملة للطاقة داخلها وخارجها. عندما يتغير شكل VDAC1 ويتجمع، يمكن أن يشكل فتحات كبيرة تسمح لعوامل تحفّز الموت بالخروج إلى داخل الخلية.
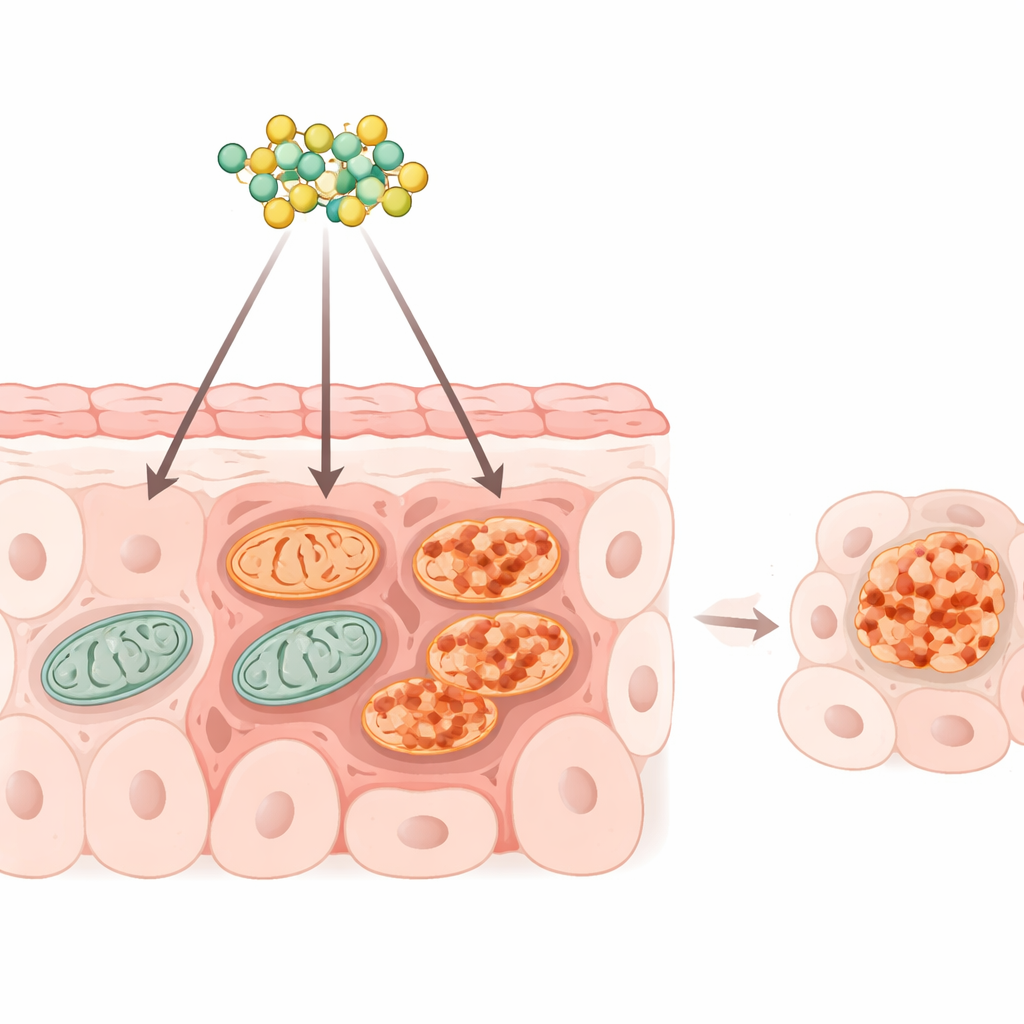
دواء طفيلي قديم وهدف جديد
صُمّم الرافوكسنايد في الأصل لقتل الديدان الطفيلية عن طريق تعطيل إنتاج طاقتها. أظهرت أعمال سابقة أنه يمكن أن يبطئ نمو أورام القولون والمستقيم ويحفز إجهادًا في حجرة أخرى من الخلية، الشبكة الإندوبلازمية، لكن كان من غير الواضح كيف يؤثر على الميتوكوندريا في الخلايا السرطانية البشرية. في هذه الدراسة عالج الفريق خطوط خلايا سرطان القولون والمستقيم بالرافوكسنايد وقيَسوا استهلاك الأكسجين وإنتاج الطاقة والشحنة الكهربائية عبر غشاء الميتوكوندريا. خلال دقائق، خفّض الدواء بشدة تنفّس الميتوكوندريا وبدأ في إضعاف شحنة الغشاء، ومع ذلك كان هذا التأثير المبكر قابلاً للعكس عند غسل الدواء، مما يشير إلى اضطراب مستهدف بدل تسمم كاسح.
من إجهاد قابل للعكس إلى ضرر قاتل
عندما امتدّ العلاج لساعات، تغيّرت الصورة. عبر دمج بيانات النشاط الجيني، ولمحات البروتينات، وقياسات المستقلبات، وجد الباحثون اضطرابات واسعة وطويلة الأمد في مكونات ومسارات الميتوكوندريا التي تساعد على نقل الوقود، وبناء جزيئات جديدة، وموازنة كيمياء الخلية. فشلت الخلايا السرطانية في تكوين تكيف ناجح، ففقد غشاء الميتوكوندريا شحنتَه تدريجيًا، وتسرب بروتين رئيسي يُدعى السيتوكروم c من الميتوكوندريا إلى السائل المحيط — وهو خطوة مبكرة كلاسيكية في الموت المبرمج للخلية. بعدها بوقت قصير بدأت الخلايا تموت، مؤكدة أن الإجهاد الميتوكوندري المطول تجاوز نقطة اللاعودة.
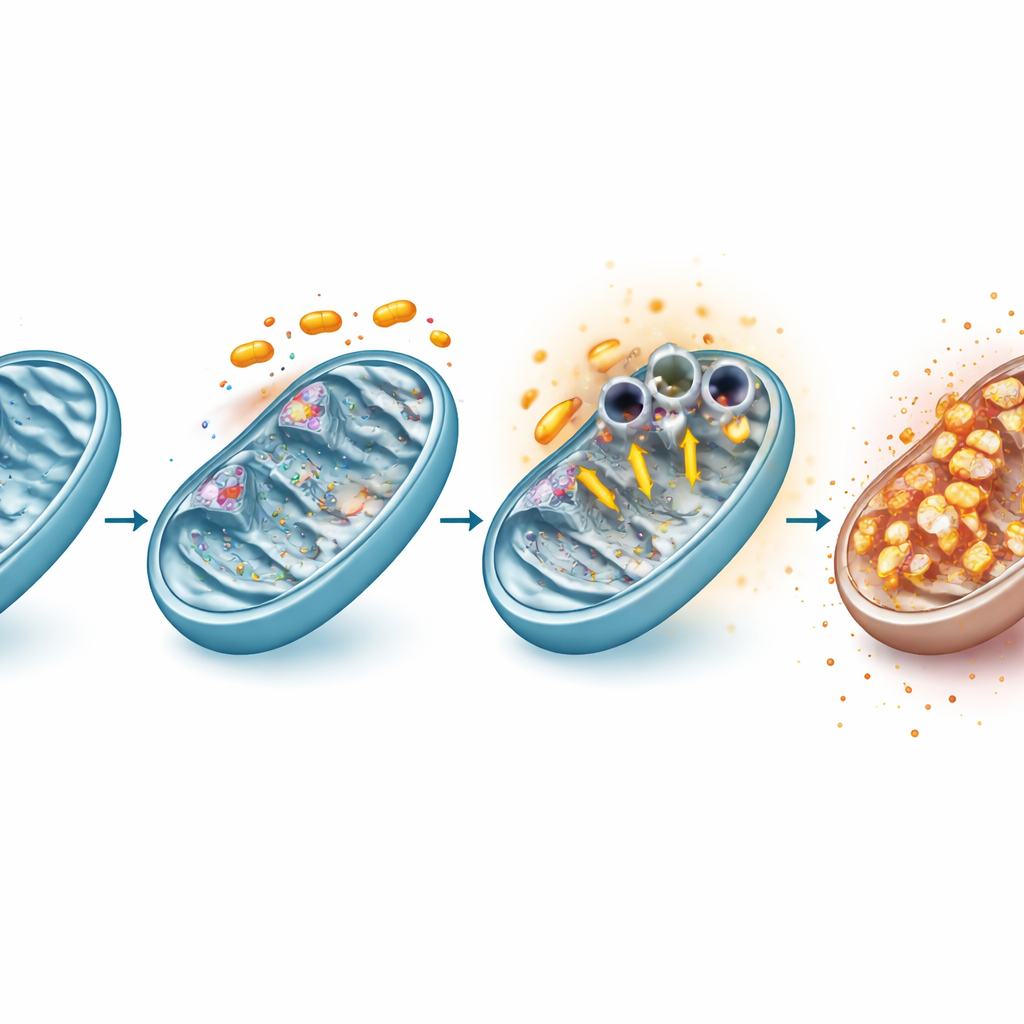
كيف يُجبر بوابة الميتوكوندريا على الانفتاح
بتعمق أكبر، أظهر الفريق أن الرافوكسنايد يثبط مباشرة تجمعين بروتينيين رئيسيين في سلسلة الطاقة الميتوكوندرية، المعروفة بالمركَّبات I وIII. أدى هذا التدخل بسرعة إلى تغيير توازن التأكسد والاختزال في الخلية، مسببًا اندفاعًا من أنواع الأكسجين التفاعلية — أشكال كيميائية نشطة من الأكسجين — حتى مع إنتاج الميتوكوندريا لكمية أقل من منتج ثانوي محدد يسمى الأكسيد الفائق لأن شحنتها الداخلية كانت تنهار. دفعت هذه الاضطرابات التأكسدية جزيئات VDAC1 في الغشاء الخارجي للميتوكوندريا إلى التجمع في تراكيب أكبر، فاتحة قنوات واسعة. أدى حجب أنواع الأكسجين التفاعلية بمضاد للأكسدة، أو تثبيط تجمّع VDAC1 دوائيًا، إلى تقليل كل من فتح هذه القنوات وفقدان شحنة غشاء الميتوكوندريا، رابطًا الإجهاد التأكسدي وسلوك VDAC1 وفشل الميتوكوندريا في سلسلة أحداث واحدة.
أدلة تتجاوز الاختبارات المختبرية
لاختبار ما إذا كانت هذه التأثيرات تحدث في ظروف أكثر واقعية، لجأ الباحثون إلى فئران تحمل أورام قولون ومستقيم محرضة كيميائيًا وإلى عينات مأخوذة مباشرة من المرضى. في الفئران، أدى علاج الرافوكسنايد إلى ظهور أورام أقل حجمًا وعددًا وتقليل علامات تكاثر الخلايا. كشفت تحليلات بروتينية مفصلة لأنسجة الورم تحولات واسعة في بروتينات الميتوكوندريا: تلك المشاركة في حرق الوقود وتشغيل سلسلة الطاقة انخفضت ميلاً، بينما ارتفعت البروتينات المرتبطة بتحلّل المكونات التالفة وحرق الدهون، ما يوحي بأن الخلايا تكافح للتأقلم مع ضغط الطاقة. ظهرت تغيّرات بروتينية ميتوكوندرية مماثلة في مستأصلات أورام مشتقة من المرضى وفي عضيدات معوية ثلاثية الأبعاد معرضة للرافوكسنايد، مشيرة إلى أن هذا الاضطراب الميتوكوندري ثابت عبر مزارع الخلايا ونماذج الحيوانات وأنسجة الأورام البشرية.
ما الذي يعنيه هذا لعلاج السرطان المستقبلي
بشكل عام، تُظهر الدراسة أن الرافوكسنايد لا يقتصر على "فصل القابس" عن إنتاج الطاقة؛ بل يدفع ميتوكوندريا خلايا سرطان القولون والمستقيم إلى حالة مطوّلة من الخلل لا تستطيع الخروج منها. عن طريق حجب مركبات رئيسية في سلسلة الطاقة، وتعطيل توازن الجزيئات التفاعلية، ودفع بوابة VDAC1 إلى الانفتاح، يطلق الدواء سلسلة متحكمًا بها تنتهي بفشل الميتوكوندريا وموت الخلية. تبدو خلايا القولون الطبيعية، التي تعتمد أقل على ميتوكوندريا مجهدة ولديها طاقة احتياطية أكبر، أقل تأثرًا بكثير. تفتح هذه النتائج احتمال أن يكون الإجهاد الميتوكوندري المضبوط — بدلاً من التدمير الكلي — وسيلة فعالة لضعف الخلايا السرطانية بشكل انتقائي، وتدعم مزيدًا من استكشاف مركبات شبيهة بالرافوكسنايد كعلاجات مستقبلية لسرطان القولون والمستقيم.
الاستشهاد: Tomassini, L., Pacifico, T., Serra, M.A. et al. Rafoxanide disrupts mitochondrial homeostasis through VDAC1 modulation in colorectal cancer cells. Cell Death Discov. 12, 142 (2026). https://doi.org/10.1038/s41420-026-02986-3
الكلمات المفتاحية: سرطان القولون والمستقيم, الميتوكوندريا, VDAC1, الجذور الحرة للأكسجين, إعادة توظيف الأدوية