Clear Sky Science · zh
在体外利用肾细胞癌(RCC)细胞系的三维侵袭特性预测其体内转移潜能
为何这项研究重要
当肾癌扩散到其他器官后,治疗难度大幅增加。医生希望尽早分辨哪些肿瘤倾向局限生长、哪些易于远处转移。本研究表明,通过在实验室中将肾癌细胞培养成精心设计的三维微型肿瘤,研究人员能够预测这些癌症在活体动物中扩散的侵袭性。该工作指向了一类体外检测方法,未来可能帮助部分患者避免不必要的治疗,同时识别需要迅速且强化治疗的个体。
打造更接近真实的微型肿瘤
大多数癌症研究仍依赖于在塑料培养皿上生长的二维细胞层。这类方法易于操作,但难以模拟肿瘤在体内的真实行为,因为体内细胞是在三维环境中穿透周围组织的。本研究使用了三种常见的肾癌细胞系,研究者已知它们具有不同的基因和信号学特征。研究人员将每种细胞形成致密的球形簇,然后将这些簇嵌入由胶原和纤维连接蛋白组成的软凝胶中,该凝胶的刚度与真实肾组织相匹配。在为期一周的时间里,他们追踪了癌细胞从球体中逸出并侵入周围凝胶的距离和速度,并绘制了单个细胞的运动轨迹。 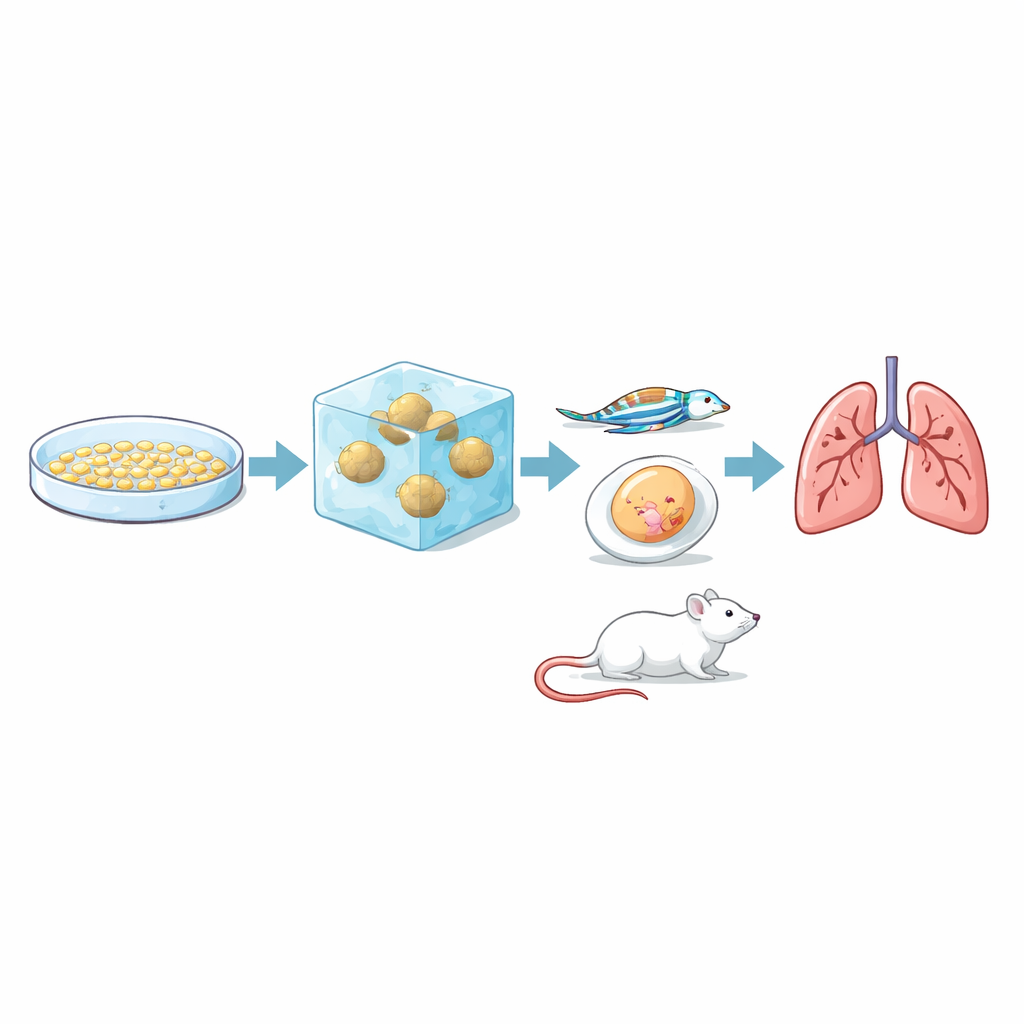
按侵袭欲望对癌细胞进行排序
在这种三维环境中,三种细胞系表现出明显不同的行为。一种称为 RCC10 的细胞系大多保持为紧密的球体,只表现出极少的向外移动。第二种细胞系 786-O 将细胞送入凝胶中,但程度为中等。第三种细胞系 RCC7 最具侵袭性:其细胞大量进入凝胶、覆盖更大区域且移动速度更快。单个 RCC7 和 786-O 细胞的轨迹显示出曲折且探索性的运动,方向频繁改变,而 RCC10 细胞则倾向于更直线且受限的移动。抑制更具侵袭性的球体中的一个关键信号通路(TGFβ 通路)显著降低了它们逃逸进入凝胶的能力,证实该模型对针对侵袭相关机制的药物有响应。
在活体动物中检验预测
关键问题是:这种体外侵袭测试是否真正反映肿瘤在生物体内的行为。为此,团队将相同的三种细胞系注入了能捕捉不同转移阶段的数种动物模型。在鸡胚膜中,三者均能形成肿瘤,但 RCC7 产生了更大、充血且形态更多样的肿块。在透明的斑马鱼胚胎中,研究人员观察到荧光标记的癌细胞通过血管移动:RCC7 与 786-O 细胞比 RCC10 更常黏附在血管壁并渗出到周围组织。在小鼠中,RCC7 与 786-O 细胞可靠地在肺部形成转移灶,其中 RCC7 发生得更快、更广泛,而 RCC10 在研究期间未在肺部检测到可见转移。综合来看,三维凝胶中得到的排序——RCC7 最具侵袭性、786-O 居中、RCC10 最低——与它们在动物体内的表现一致。 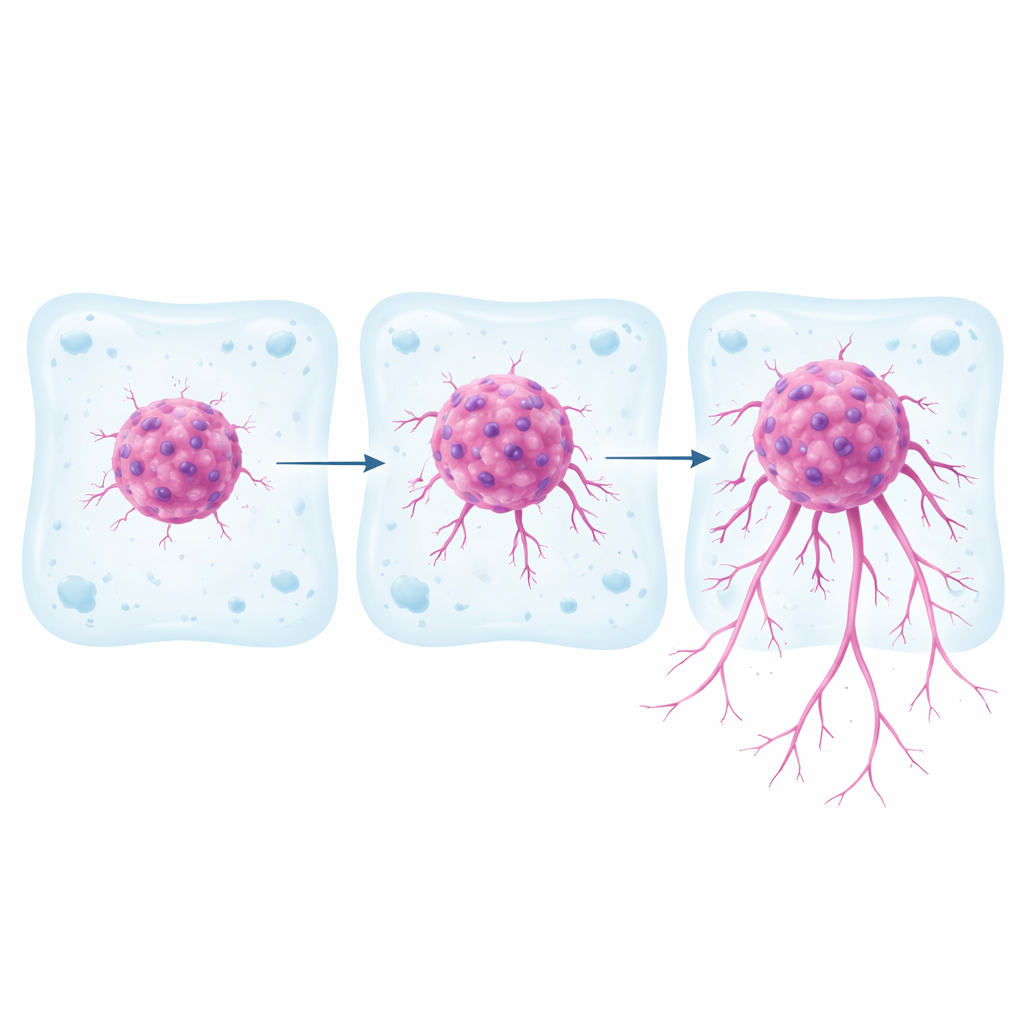
将方法扩展到患者肿瘤
为更贴近临床实际,研究者还从两位病人新鲜肿瘤样本中构建了三维“肿瘤类器官”。在相同的凝胶体系中,高级别病人的肿瘤类器官侵袭迅速并伸出许多探索性分支,而低级别病人的类器官则保持更致密、移动更缓慢。大多数侵袭细胞携带已知的肾癌标记,确认它们来自肿瘤而非周围正常细胞。尽管患者样本数量有限,结果表明,患者肿瘤类器官的三维侵袭行为可能反映其疾病的严重程度。
对患者意味着什么
这项工作表明,一种相对简单的三维体外检测可以映射肾癌细胞在活体动物中扩散的行为。通过观察细胞从现实感较强的微型肿瘤中逸出的距离和动态特征,科学家可以区分低、中、高转移潜能的癌症。未来,这类三维肿瘤类器官测定可与传统显微分级和基因检测结合,帮助医生更好地预测哪些肾癌可能发生转移并据此定制治疗方案。它们也可作为一种更符合伦理且更快速的平台,用于测试旨在阻止癌症扩散的新药物。
引用: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
关键词: 肾癌, 肿瘤类器官, 三维细胞培养, 转移, 肾透明细胞癌