Clear Sky Science · pl
Wykorzystanie właściwości inwazyjnych w 3D linii komórkowych RCC in vitro do przewidywania ich potencjału metastatycznego in vivo
Dlaczego to badanie ma znaczenie
Gdy rak nerek rozprzestrzenia się do innych narządów, leczenie staje się znacznie trudniejsze. Lekarze chcieliby jak najwcześniej wiedzieć, które guzy prawdopodobnie pozostaną miejscowe, a które mają skłonność do rozprzestrzeniania się. To badanie pokazuje, że hodując komórki raka nerek w starannie zaprojektowanych trójwymiarowych mini‑guzach w laboratorium, badacze mogą przewidzieć, jak agresywnie te nowotwory będą rozsiewać się u żywych zwierząt. Praca ta wskazuje drogę do testów laboratoryjnych, które mogłyby w przyszłości oszczędzić niektórym pacjentom niepotrzebnych terapii, a jednocześnie wskazać tych, którzy wymagają szybkiego, intensywnego leczenia.
Tworzenie lepszych mini‑guzów
Większość badań nad rakiem wciąż opiera się na jednowarstwowych hodowlach komórek na plastikowych naczyniach. Są one łatwe w obsłudze, ale słabo odzwierciedlają zachowanie guzów w organizmie, gdzie komórki przemieszczają się przez otaczającą tkankę w trzech wymiarach. W tym badaniu naukowcy pracowali z trzema dobrze znanymi liniami komórkowymi raka nerek, o wcześniej udokumentowanych różnicach genetycznych i sygnałowych. Uformowali każdą linię w zwarte, sferyczne skupiska, a następnie zatopili je w miękkim żelu z kolagenu i fibryonektyny, o sztywności zbliżonej do prawdziwej tkanki nerkowej. Przez tydzień śledzili, jak daleko i jak szybko komórki nowotworowe odrywały się od sferoidu i wnikały w otaczający żel, oraz mapowali trajektorie pojedynczych komórek. 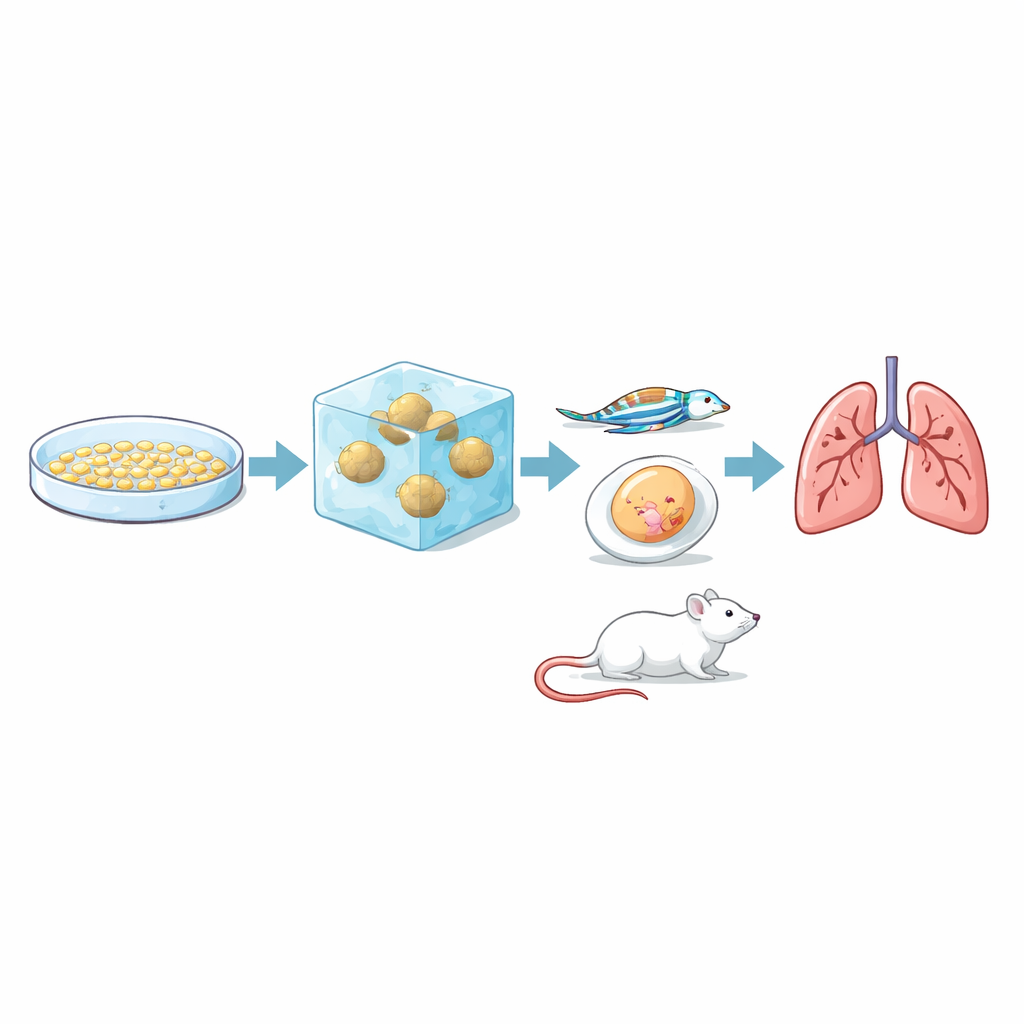
Ocena linii nowotworowych pod względem skłonności do inwazji
W tym trójwymiarowym środowisku trzy linie komórkowe wykazały wyraźnie różne zachowania. Jedna linia, nazwana RCC10, utrzymywała się głównie jako zwarta kula z jedynie minimalnym ruchem na zewnątrz. Druga, 786‑O, wysyłała komórki do żelu, ale w umiarkowanym stopniu. Trzecia linia, RCC7, była najbardziej agresywna: jej komórki penetrowały żel na duże odległości, zajmowały większy obszar i poruszały się z wyższymi prędkościami. Ścieżki poszczególnych komórek RCC7 i 786‑O były kręte i eksploracyjne, z częstymi zmianami kierunku, podczas gdy komórki RCC10 poruszały się bardziej prosto i w ograniczonym zakresie. Zablokowanie kluczowej drogi sygnałowej (szlaku TGFβ) w bardziej inwazyjnych sferoidach znacząco zmniejszyło ich zdolność do ucieczki do żelu, potwierdzając, że model reaguje na leki celujące w mechanizmy związane z inwazją.
Testowanie przewidywań in vivo
Kluczowe pytanie brzmiało, czy ten laboratoryjny test inwazji rzeczywiście odzwierciedla zachowanie guzów w żywych organizmach. Aby to sprawdzić, zespół wszczepił te same trzy linie komórkowe do kilku modeli zwierzęcych odzwierciedlających różne etapy metastazy. W błonach jaj kurzych wszystkie trzy tworzyły guzy, ale RCC7 dała większe, wypełnione krwią i bardziej zróżnicowane masy. W przezroczystych embrionach zebry obserwowano fluorescencyjnie znakowane komórki nowotworowe przemieszczające się przez naczynia krwionośne: komórki RCC7 i 786‑O częściej przyczepiały się do ścian naczyń i przechodziły do otaczającej tkanki niż komórki RCC10. U myszy komórki RCC7 i 786‑O konsekwentnie tworzyły przerzuty w płucach, przy czym RCC7 czyniła to szybciej i bardziej rozlegle, podczas gdy RCC10 nie dała wykrywalnych przerzutów płucnych w okresie trwania badania. Podsumowując, ranking zaobserwowany w żelu 3D — RCC7 najbardziej inwazyjna, 786‑O pośrednia, RCC10 najmniej — odpowiadał ich zachowaniu u zwierząt. 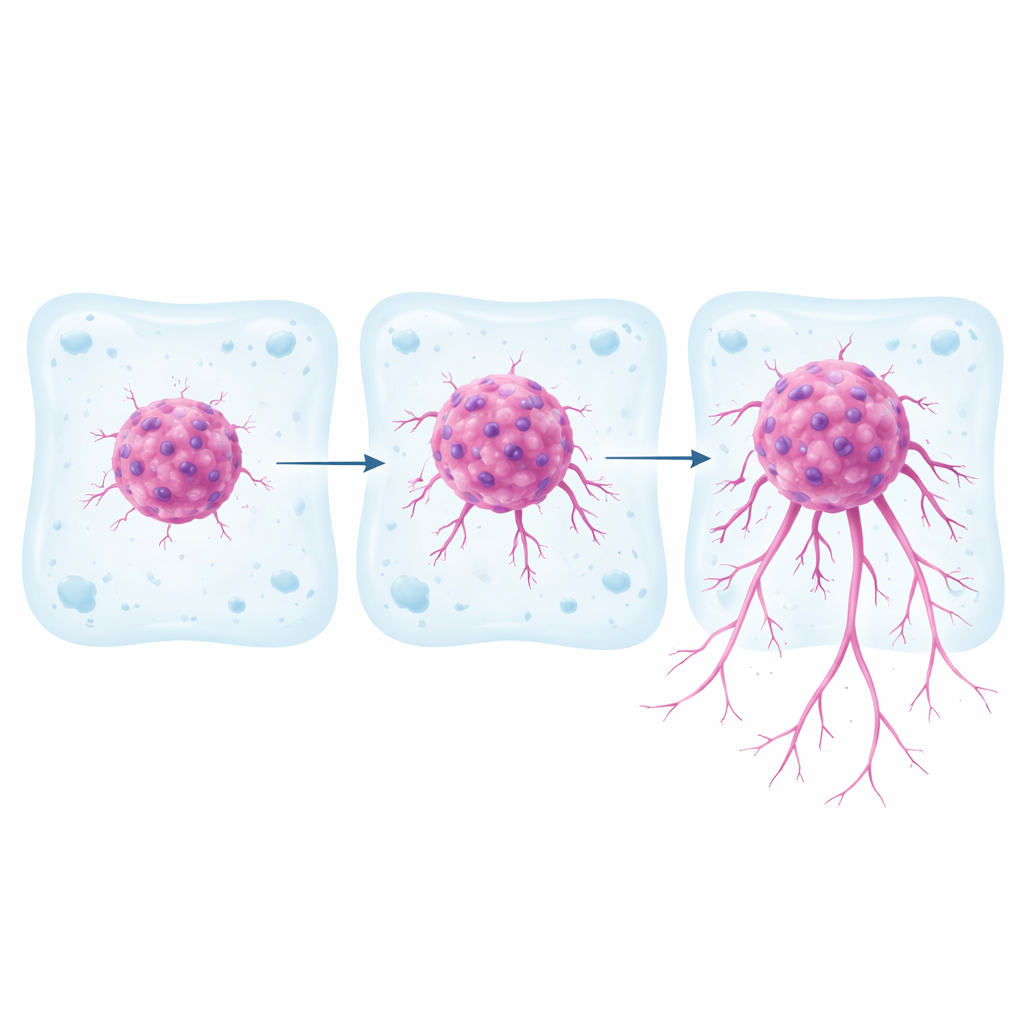
Rozszerzanie podejścia na próbki pacjentów
Aby zbliżyć się do realiów klinicznych, badacze stworzyli także trójwymiarowe „tumoeroidy” z świeżych próbek guzów pobranych od dwóch pacjentów z rakiem nerki o różnym standardowym stopniu zaawansowania patologicznego. Hodowane w tym samym systemie żelowym, tumoroidy pochodzące z guza wyższego stopnia szybko inwadowały i wysyłały wiele eksploracyjnych wypustek, podczas gdy te z guza niższego stopnia pozostawały bardziej zwarte i wolniej poruszały się. Większość komórek inwazyjnych nosiła znany marker raka nerek, co potwierdziło, że pochodziły z guza, a nie z otaczających normalnych tkanek. Choć próbka pacjentów jest niewielka, wyniki sugerują, że zachowanie inwazyjne tumoroidów w 3D może odzwierciedlać powagę choroby u pacjenta.
Co to oznacza dla pacjentów
Praca pokazuje, że stosunkowo prosty test laboratoryjny w 3D może odzwierciedlać, jak komórki raka nerek rozprzestrzeniają się w żywych organizmach. Obserwując, jak daleko i jak dynamicznie komórki uciekają z mini‑guzów w realistycznym żelu, naukowcy mogą rozróżnić nowotwory o niskim, średnim i wysokim potencjale metastatycznym. W przyszłości takie testy tumoroidowe 3D, w połączeniu ze standardowym gradingiem mikroskopowym i badaniami genetycznymi, mogłyby pomóc lekarzom lepiej przewidzieć, które raki nerek mają skłonność do przerzutów i dostosować terapię odpowiednio. Mogłyby też zapewnić etyczniejszą, szybszą platformę do testowania nowych leków mających na celu powstrzymanie rozsiewu raka zanim się rozpocznie.
Cytowanie: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Słowa kluczowe: rak nerki, tumoeroidy, hodowla komórek 3D, przerzuty, raka komórek nerkowych